名校
1 . 下列实验内容可以达到预期实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 将1 mol 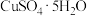 溶解在1 L水中 溶解在1 L水中 | 配制1  的 的 溶液 溶液 |
| B | 将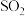 通入酸性 通入酸性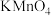 溶液中 溶液中 | 证明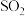 具有漂白性 具有漂白性 |
| C | 加入足量铁屑,充分反应后,过滤 | 除去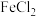 溶液中的少量 溶液中的少量 |
| D | 将木炭与浓硫酸共热,得到的气体通入澄清石灰水 | 检验木炭的氧化产物是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-16更新
|
239次组卷
|
2卷引用:青海省西宁市大通回族土族自治县2021-2022学年高三上学期期中考试化学试题
解题方法
2 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究苯酚与钠的反应 | 在一支干燥的试管里加入 乙醇,再加入约 乙醇,再加入约 苯酚,振荡。再加入绿豆大小的吸干煤油的金属钠 苯酚,振荡。再加入绿豆大小的吸干煤油的金属钠 | 若有连续的气泡产生,则钠与苯酚反应生成氢气 |
| B | 探究蛋白质溶液的性质 | 取蛋白质溶液 于试管中,加入 于试管中,加入 的硫酸铜溶液,再加入3~4滴1%的氢氧化钠溶液,振荡 的硫酸铜溶液,再加入3~4滴1%的氢氧化钠溶液,振荡 | 若有紫玫瑰色沉淀生成,则是蛋白质 |
| C | 探究金属铁在氯气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入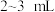 蒸馏水,振荡,迅速滴入5滴 蒸馏水,振荡,迅速滴入5滴 溶液 溶液 | 若溶液无血红色,则固体粉末不为 |
| D | 探究反应条件对化学平衡的影响 | 取一支试管,加入 乙醇溶液和少量氯化钴晶体,振荡使其溶解,再逐滴滴加蒸馏水,至溶液恰好呈粉红色,然后用酒精灯加热该试管。 乙醇溶液和少量氯化钴晶体,振荡使其溶解,再逐滴滴加蒸馏水,至溶液恰好呈粉红色,然后用酒精灯加热该试管。 | 若有粉红色变为蓝色,则说明温度能影响化学平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 为确定Fe和Fe2O3混合物样品的组成,称取该样品27.2g加入200mL盐酸中使其充分溶解,放出氢气的体积为2.24L(折算成标况),向反应后的溶液中加入KSCN颜色无明显变化,测得溶液中氢离子浓度为1.0mol/L(忽略溶液体积变化)。试计算:
(1)样品中铁的质量m(Fe)=___ 。
(2)盐酸的物质的量浓度c(HCl)=___ 。
(1)样品中铁的质量m(Fe)=
(2)盐酸的物质的量浓度c(HCl)=
您最近一年使用:0次
名校
解题方法
4 . 利用某工业废弃固体(成分为 Cu2S 和 FeS2)制备硫酸铜溶液和硫酸亚铁晶体,流程如图所示。

(已知:①固体 B 含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)
(1)操作 I 是____ 。为了提高废弃固体的反应速率,除将固体粉碎、提高温度外,还可以采取的具体措施有____ (写一条)。
(2)写出 FeS2在空气中灼烧的化学方程式_____ 。
(3)溶液 C 中的溶质有_________ (用化学式表示)。
(4)试剂 y 的作用是_____ 。

(已知:①固体 B 含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)
(1)操作 I 是
(2)写出 FeS2在空气中灼烧的化学方程式
(3)溶液 C 中的溶质有
(4)试剂 y 的作用是
您最近一年使用:0次
解题方法
5 . 以硫铁矿(含CuS、 等杂质)为原料制备绿矾晶体的工业流程如图。
等杂质)为原料制备绿矾晶体的工业流程如图。
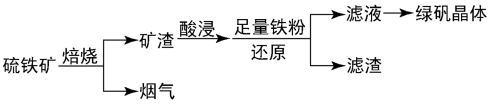
下列有关说法中不正确的是
 等杂质)为原料制备绿矾晶体的工业流程如图。
等杂质)为原料制备绿矾晶体的工业流程如图。
下列有关说法中不正确的是
| A.焙烧硫铁矿时,通过粉碎硫铁矿可加快焙烧速率 |
| B.在矿渣酸浸时,可适当提高酸的浓度以加快反应速率 |
| C.加入铁粉时发生了置换反应 |
| D.将滤液倒入表面皿中加热蒸发结晶,从而获得绿矾晶体 |
您最近一年使用:0次
名校
解题方法
6 . 铁、铜混合粉末a g加入到100 mL Fe(NO3)3和HNO3的混合溶液中,充分反应后,剩余固体质量为b g,将固体过滤后,向滤液(忽略溶液体积变化)中加入100 mL 0.4 mol·L-1 NaOH溶液,滤液中金属离子恰好沉淀完全。下列说法错误的是
| A.剩余固体一定含铜,可能含铁 |
| B.向反应后的固液混合体系中加入稀盐酸,固体一定会继续溶解 |
| C.加入NaOH溶液后最终可观察到红褐色沉淀,可知原滤液中含Fe3+ |
| D.所得滤液中c(NO3-)=0.4 mol·L-1 |
您最近一年使用:0次
2021-06-23更新
|
995次组卷
|
2卷引用:河南省非凡吉创2020-2021学年高一下学期5月调研化学试题
7 . 下列由实验操作和现象推出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 某SO2气体中可能存在CO2,将气体依次通过NaHCO3溶液、品红溶液、澄清石灰水,品红溶液不褪色,澄清石灰水变浑浊 | 该气体中存在CO2 |
| B | 去家用食盐少量,溶于水,加少量淀粉固体,充分搅拌,无明显变化 | 这是一种没有添加碘的食盐 |
| C | 取细铁丝在酒精灯上灼烧至红热,再伸入充满氯气的瓶中,剧烈反应,产生大量红褐色的烟,结束后,加水振荡,使固体充分溶解,再滴加2滴KSCN溶液,溶液未变色 | Fe在Cl2中燃烧生成FeCl2 |
| D | 将钠块融化后,上面倒扣一个充满CO2的集气瓶,剧烈燃烧,产生大量白烟,瓶壁有黑色固体 | 钠置换产生了碳单质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-17更新
|
307次组卷
|
2卷引用:安徽省2021届高三下学期高考最后一卷(5月)理综化学试题
8 . 距离北京2022年冬奥会还有不到一年的时间,各项筹办工作也到了最后的冲刺阶段。冬奥会从场馆建设到场馆运行,绿色可持续的理念贯穿始终。
(1)在汽车尾气处理方面,因汽车排放的尾气中含有大量含氮氧化物而污染大气,造成产生氮的氧化物的主要原因是___ (填字母)
A.燃烧含氮化合物引起的
B.由于汽油得不充分燃烧
C.汽缸中N2被氧化生成的
请写出该反应的化学方程式___ 。
(2)在生活用水方面,延庆赛区各类建筑的节水型生活用水器具普及率达100%,并建有分散和集中污水处理设施,实现生活污水全部收集、处理后再利用。某化工厂排放的污水中含有Mg2+、Fe3+、Cu2+、Hg2+四种离子。某同学设计了从该污水中回收纯净金属铜的方案。
已知:汞会挥发。
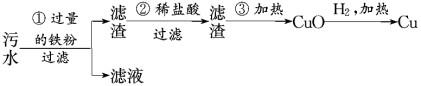
①滤液中主要含有的金属离子为___ 和___ 。
②第②步发生反应的离子方程式为___ 。
③第③步会造成的环境污染问题是___ 。
(1)在汽车尾气处理方面,因汽车排放的尾气中含有大量含氮氧化物而污染大气,造成产生氮的氧化物的主要原因是
A.燃烧含氮化合物引起的
B.由于汽油得不充分燃烧
C.汽缸中N2被氧化生成的
请写出该反应的化学方程式
(2)在生活用水方面,延庆赛区各类建筑的节水型生活用水器具普及率达100%,并建有分散和集中污水处理设施,实现生活污水全部收集、处理后再利用。某化工厂排放的污水中含有Mg2+、Fe3+、Cu2+、Hg2+四种离子。某同学设计了从该污水中回收纯净金属铜的方案。
已知:汞会挥发。

①滤液中主要含有的金属离子为
②第②步发生反应的离子方程式为
③第③步会造成的环境污染问题是
您最近一年使用:0次



