23-24高一上·浙江·期末
解题方法
1 . 某实验小组在实验室进行Fe2+与Fe3+相互转化的实验。
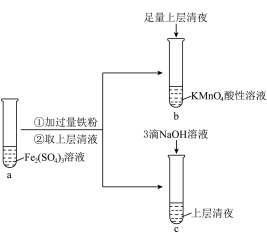
(1)向试管a中加入过量铁粉的离子方程式是___________ 。
(2)试管b中的实验现象是___________ 。
(3)试管c中产生白色沉淀,一段时间后部分沉淀变为红褐色。写出白色沉淀变为红褐色的化学方程式___________ 。
(4)实验小组为探究反应物浓度对Fe(OH)2制备效果的影响,以Fe(OH)2沉淀白色持续时间(t)为指标,t越大,实验效果越好。部分实验数据如下(w表示质量分数):
①实验i、ii、iii的目的是___________ 。
②小组同学通过实验得出结论:其他条件不变时,所用NaOH溶液的浓度越大,实验效果越好,推断的证据是___________ 。

(1)向试管a中加入过量铁粉的离子方程式是
(2)试管b中的实验现象是
(3)试管c中产生白色沉淀,一段时间后部分沉淀变为红褐色。写出白色沉淀变为红褐色的化学方程式
(4)实验小组为探究反应物浓度对Fe(OH)2制备效果的影响,以Fe(OH)2沉淀白色持续时间(t)为指标,t越大,实验效果越好。部分实验数据如下(w表示质量分数):
| 实验 | 序号 | w(FeSO4)/% | w(NaOH)/% | t/s |
 | i | 2.5 | 15 | 149 |
| ii | 5 | 15 | 138 | |
| iii | 10 | 15 | 99 | |
| iv | 5 | 25 | 142 | |
| v | 5 | 35 | 180 |
②小组同学通过实验得出结论:其他条件不变时,所用NaOH溶液的浓度越大,实验效果越好,推断的证据是
您最近一年使用:0次
解题方法
2 . 根据所学知识,下列物质间转化不能通过一步反应实现的是
A.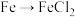 | B. |
C.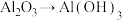 | D.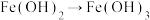 |
您最近一年使用:0次
解题方法
3 . 下列物质长期露置于空气中会变质且不涉及氧化还原反应的是
| A.NaCl | B.NaOH | C.氯水 | D.Fe(OH)2 |
您最近一年使用:0次
2023-03-13更新
|
203次组卷
|
3卷引用:吉林省吉林市普通高中2022-2023学年高一上学期期末考试化学试题
解题方法
4 . 部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是


| A.过量的a在氯气中燃烧,可生成b |
| B.b在反应中既能被氧化,又能被还原 |
| C.可将e的饱和溶液加入沸水中制得d的胶体 |
| D.可存在b→c→d→e→b的循环转化关系 |
您最近一年使用:0次
名校
解题方法
5 . 构建知识网络是一种有效的学习方法,化学学习中的“价一类”二维图就是其中一种,如图所示是铁及其化合物的“价一类”二维图,下列有关叙述或化学方程式书写不正确的是
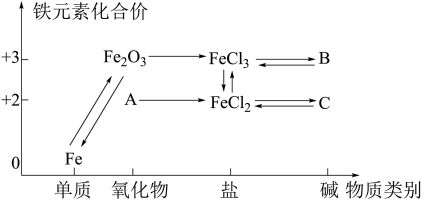

| A.物质A的氧化物不稳定,在空气中受热迅速被氧化 |
B. 可能是 可能是 |
C.C在空气中容易被氧化成B,每 被氧化消耗的氧气为 被氧化消耗的氧气为 |
D. 的反应类型是氧化还原反应 的反应类型是氧化还原反应 |
您最近一年使用:0次
2023-03-07更新
|
340次组卷
|
4卷引用:广东省河源市龙川县第一中学2022-2023学年高一上学期期末考试化学试题
广东省河源市龙川县第一中学2022-2023学年高一上学期期末考试化学试题黑龙江省牡丹江市第二高级中学2023-2024学年高一上学期1月期末化学试题(已下线)第13讲 铁的氧化物和铁的氢氧化物-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)第3讲 铁盐及其亚铁盐
6 . 下列各组转化关系,不能 由一步反应实现的是
A.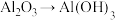 | B. |
C. | D. |
您最近一年使用:0次
2023-03-06更新
|
208次组卷
|
2卷引用:广西南宁市2022-2023学年高一上学期期末考试化学试题
7 . 铁及其化合物在生产生活中有重要用途。某化学兴趣小组同学设计以下实验探究铁及其化合物性质。
Ⅰ.氢氧化亚铁的制备:
A组实验:用NaOH溶液和 溶液直接反应。(如图1)
溶液直接反应。(如图1)
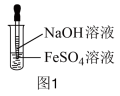
(1)该方法能观察到白色 沉淀,但沉淀颜色快速发生变化,反应方程式为
沉淀,但沉淀颜色快速发生变化,反应方程式为_______ 。
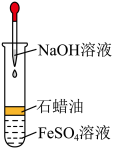
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图2。
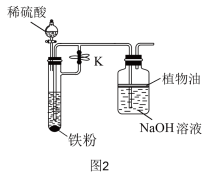
(2)实验时,先_______ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后,_______ (填“打开”或“关闭”)止水夹K,制得白色 沉淀,该方法制得的
沉淀,该方法制得的 沉淀能保持一段时间不变色的原因有
沉淀能保持一段时间不变色的原因有_______ 。
Ⅱ.探究 、
、 的性质:
的性质:
(3)选用0.1mol/L 溶液、0.1mol/L
溶液、0.1mol/L 溶液、KSCN溶液、新制氯水、KI溶液、淀粉溶液,设计实验方案进行实验,完成下列表格。
溶液、KSCN溶液、新制氯水、KI溶液、淀粉溶液,设计实验方案进行实验,完成下列表格。
Ⅰ.氢氧化亚铁的制备:
A组实验:用NaOH溶液和
 溶液直接反应。(如图1)
溶液直接反应。(如图1)
(1)该方法能观察到白色
 沉淀,但沉淀颜色快速发生变化,反应方程式为
沉淀,但沉淀颜色快速发生变化,反应方程式为B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图2。

(2)实验时,先
 沉淀,该方法制得的
沉淀,该方法制得的 沉淀能保持一段时间不变色的原因有
沉淀能保持一段时间不变色的原因有Ⅱ.探究
 、
、 的性质:
的性质:(3)选用0.1mol/L
 溶液、0.1mol/L
溶液、0.1mol/L 溶液、KSCN溶液、新制氯水、KI溶液、淀粉溶液,设计实验方案进行实验,完成下列表格。
溶液、KSCN溶液、新制氯水、KI溶液、淀粉溶液,设计实验方案进行实验,完成下列表格。| 探究内容 | 实验方案 | 实验现象 | 写出离子方程式 |
①探究 具有还原性 具有还原性 | 取少 溶液,加入少量KSCN溶液后,再往溶液中加入少量 溶液,加入少量KSCN溶液后,再往溶液中加入少量 | 溶液先不变红,后变为血红色。 | |
②探究 具有氧化性 具有氧化性 | 取少量 溶液,加入几滴 溶液,加入几滴 | 溶液变蓝 |
您最近一年使用:0次
解题方法
8 . 下列化学方程式书写错误的是
| A.MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O |
B.4Li+O2 2Li2O 2Li2O |
| C.Br2+2KI=2KBr+I2 |
| D.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
您最近一年使用:0次
名校
解题方法
9 . 元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。
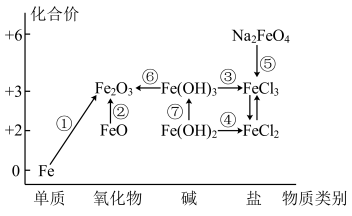
请回答以下问题:
(1) 中Fe的化合价为
中Fe的化合价为_______ 。
(2) 是否为碱性氧化物
是否为碱性氧化物_______ (填是或否),理由:_______ 。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:_______ 。
(4)已知 在强碱溶液中稳定存在,PH越小稳定性越差;则制备
在强碱溶液中稳定存在,PH越小稳定性越差;则制备 时需要在
时需要在_______ (填“酸性”“碱性”或“中性”)环境中进行: 也可以作为净水剂,能与水反应生成具有吸附性的
也可以作为净水剂,能与水反应生成具有吸附性的 胶体,写出其中离子方程式:
胶体,写出其中离子方程式:_______ 。其中检验溶液中 的试剂是
的试剂是_______ 。
(5)FeO、 是合成氨工业生产中所用的
是合成氨工业生产中所用的 催化剂的主要成分。某FeO、
催化剂的主要成分。某FeO、 混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、
混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、 的物质的量之比为
的物质的量之比为_______ 。

请回答以下问题:
(1)
 中Fe的化合价为
中Fe的化合价为(2)
 是否为碱性氧化物
是否为碱性氧化物(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)已知
 在强碱溶液中稳定存在,PH越小稳定性越差;则制备
在强碱溶液中稳定存在,PH越小稳定性越差;则制备 时需要在
时需要在 也可以作为净水剂,能与水反应生成具有吸附性的
也可以作为净水剂,能与水反应生成具有吸附性的 胶体,写出其中离子方程式:
胶体,写出其中离子方程式: 的试剂是
的试剂是(5)FeO、
 是合成氨工业生产中所用的
是合成氨工业生产中所用的 催化剂的主要成分。某FeO、
催化剂的主要成分。某FeO、 混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、
混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
2023-02-26更新
|
375次组卷
|
3卷引用:河南省南阳市镇平县第一高级中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
10 . 铁黄 是一种优质颜料。制备铁黄晶种时,向精制
是一种优质颜料。制备铁黄晶种时,向精制 溶液中滴加氨水(弱碱),先出现白色沉淀,后变为灰绿色。加氨水至
溶液中滴加氨水(弱碱),先出现白色沉淀,后变为灰绿色。加氨水至 时,开始通入空气,溶液
时,开始通入空气,溶液 随时间的变化曲线如图。下列分析不正确的是
随时间的变化曲线如图。下列分析不正确的是
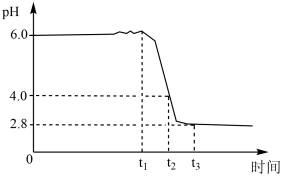
 是一种优质颜料。制备铁黄晶种时,向精制
是一种优质颜料。制备铁黄晶种时,向精制 溶液中滴加氨水(弱碱),先出现白色沉淀,后变为灰绿色。加氨水至
溶液中滴加氨水(弱碱),先出现白色沉淀,后变为灰绿色。加氨水至 时,开始通入空气,溶液
时,开始通入空气,溶液 随时间的变化曲线如图。下列分析不正确的是
随时间的变化曲线如图。下列分析不正确的是
A.产生白色沉淀的离子方程式为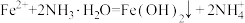 |
B. 发生的主要反应为 发生的主要反应为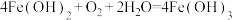 |
C. 发生的主要反应为 发生的主要反应为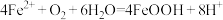 |
D. 后仅发生反应4Fe2++O2+4H+=4Fe3++2H2O 后仅发生反应4Fe2++O2+4H+=4Fe3++2H2O |
您最近一年使用:0次
2023-02-26更新
|
422次组卷
|
4卷引用:福建省厦门市2022-2023学年高一上学期学业水平测试化学试题



