1 . 实验室以(NH4)2CO3和Cu(OH)2为原料制备高纯Cu2(OH)2CO3的方法如下:___________ (答两点)。
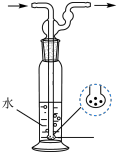
(2)“蒸氨”在如图所示的实验装置中进行。___________ 。
②实验采用三个盛有水的洗气瓶吸收尾气的目的为___________ ;与上图所示洗气瓶相比,采用三个如图所示装置的优点为___________ 。___________ 。
(3)已知:①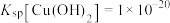 ;
;
②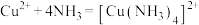
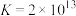 ;
;
③沉淀速率过快时,Cu(OH)2絮状沉淀易裹挟杂质。
以CuSO4∙5H2O固体为原料,补充完整制备纯净Cu(OH)2的实验方案:取一定质量的CuSO4∙5H2O固体分批加入蒸馏水中,搅拌至完全溶解,___________ ,低温烘干。(须使用的试剂:浓氨水、1mol∙L-1 NaOH溶液、0.1mol∙L-1 BaCl2溶液、蒸馏水)
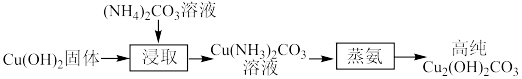
(2)“蒸氨”在如图所示的实验装置中进行。

②实验采用三个盛有水的洗气瓶吸收尾气的目的为
(3)已知:①
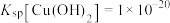 ;
;②
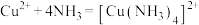
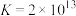 ;
;③沉淀速率过快时,Cu(OH)2絮状沉淀易裹挟杂质。
以CuSO4∙5H2O固体为原料,补充完整制备纯净Cu(OH)2的实验方案:取一定质量的CuSO4∙5H2O固体分批加入蒸馏水中,搅拌至完全溶解,
您最近一年使用:0次
名校
解题方法
2 . 取一定量胆矾晶体(CuSO4·5H2O)加热分解,固体残留率( ) 随温度的变化如图所示:
) 随温度的变化如图所示:
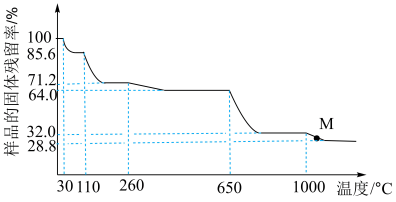
下列说法中不正确的是
 ) 随温度的变化如图所示:
) 随温度的变化如图所示:
下列说法中不正确的是
| A.110°C 时的晶体化学式 CuSO4·3H2O |
B.260°C~ 650°C 过程中的反应方程式为CuSO4·H2O CuSO4+H2O CuSO4+H2O |
| C.已知 650°C 加热至 1000°C ,产物为一种固体与一种气体, 则气体为SO2 |
| D.M 点所得固体是 CuO 与 Cu2O 的混合物 |
您最近一年使用:0次
名校
3 . 秦始皇兵马俑是世界文化遗产,兵马俑表面的彩绘体现了当时彩绘工艺和颜料制作工艺水平,具有极高的历史价值和艺术价值。下列对于兵马俑使用颜料的主要成分与其类别的对应关系正确的是

| 选项 | A | B | C | D |
| 颜色 | 绿色 | 棕红色 | 大红色 | 黑色 |
| 主要成分 | 石绿 | 赭石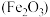 | 朱砂( ) ) | 炭黑(C) |
| 类别 | 碱 | 酸性氧化物 | 电解质 | 有机物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-16更新
|
396次组卷
|
4卷引用:江苏省无锡市第一中学2023-2024学年高一上学期期末考试化学试题
江苏省无锡市第一中学2023-2024学年高一上学期期末考试化学试题北京市中国人民大学附属中学2022-2023学年高一下学期期末考试化学试题河南省唐河县鸿唐高级中学2023-2024学年高三上学期8月月考化学试题(已下线)综合01 期末压轴80题之选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
名校
4 . 回答下列问题:
(1) 可用作有机合成的催化剂。
可用作有机合成的催化剂。 是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
次磷酸 是一种强还原剂,将它加入
是一种强还原剂,将它加入 水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生
水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生 。写出生成CuH的化学方程式:
。写出生成CuH的化学方程式:___________ 。
(2)某同学利用如下图所示装置,测定高炉煤气中CO、 、
、 和
和 的百分组成。
的百分组成。 的盐酸溶液能吸收CO形成
的盐酸溶液能吸收CO形成 。
。
ii.保险粉 和KOH的混合溶液能吸收氧气。
和KOH的混合溶液能吸收氧气。
请回答以下问题:
①G中测出的是___________ (填物质的化学式)的体积。
②F洗气瓶中宜盛放的试剂是___________ 。
(3)工业上可以在酸性介质中用 氧化浸出黄铜矿
氧化浸出黄铜矿 。
。
① 反应后转化为
反应后转化为 、
、 、
、 。将
。将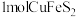 完全转化,理论上所需
完全转化,理论上所需 的物质的量为
的物质的量为___________ 。
②浸出过程中发现, 的反应实际用量远大于理论用量,原因是
的反应实际用量远大于理论用量,原因是___________ 。
③若浸出过程中,溶液中含有少量 ,则会析出黄钠铁矾
,则会析出黄钠铁矾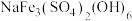 沉淀。写出
沉淀。写出 转化为黄钠铁矾沉淀的离子方程式:
转化为黄钠铁矾沉淀的离子方程式:___________ 。
(1)
 可用作有机合成的催化剂。
可用作有机合成的催化剂。 是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。次磷酸
 是一种强还原剂,将它加入
是一种强还原剂,将它加入 水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生
水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生 。写出生成CuH的化学方程式:
。写出生成CuH的化学方程式:(2)某同学利用如下图所示装置,测定高炉煤气中CO、
 、
、 和
和 的百分组成。
的百分组成。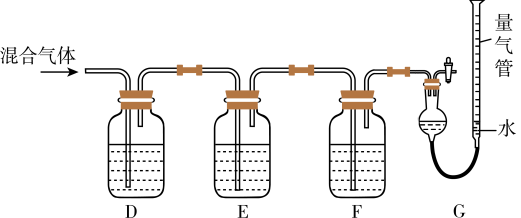
 的盐酸溶液能吸收CO形成
的盐酸溶液能吸收CO形成 。
。ii.保险粉
 和KOH的混合溶液能吸收氧气。
和KOH的混合溶液能吸收氧气。请回答以下问题:
①G中测出的是
②F洗气瓶中宜盛放的试剂是
(3)工业上可以在酸性介质中用
 氧化浸出黄铜矿
氧化浸出黄铜矿 。
。①
 反应后转化为
反应后转化为 、
、 、
、 。将
。将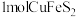 完全转化,理论上所需
完全转化,理论上所需 的物质的量为
的物质的量为②浸出过程中发现,
 的反应实际用量远大于理论用量,原因是
的反应实际用量远大于理论用量,原因是③若浸出过程中,溶液中含有少量
 ,则会析出黄钠铁矾
,则会析出黄钠铁矾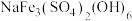 沉淀。写出
沉淀。写出 转化为黄钠铁矾沉淀的离子方程式:
转化为黄钠铁矾沉淀的离子方程式:
您最近一年使用:0次
解题方法
5 . 实验室可用反应 来制备CuI(CuI受热易被氧化)。下列实验装置和操作
来制备CuI(CuI受热易被氧化)。下列实验装置和操作不能 达到实验目的的是
 来制备CuI(CuI受热易被氧化)。下列实验装置和操作
来制备CuI(CuI受热易被氧化)。下列实验装置和操作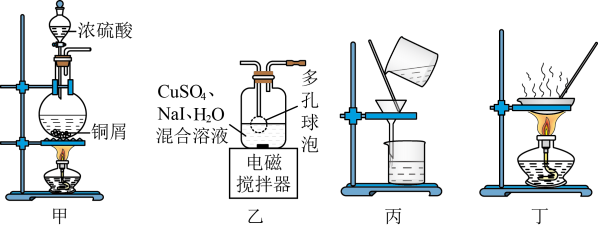
A.用甲装置制备 | B.用乙装置制备CuI |
| C.用丙装置分离出CuI | D.用丁装置干燥CuI固体 |
您最近一年使用:0次
6 . 在指定条件下,下列选项所示的物质间转化均能实现的是
A. |
B.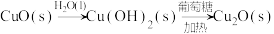 |
C. |
D.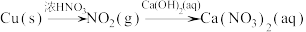 |
您最近一年使用:0次
名校
解题方法
7 . 通常情况下,下列变化通过一步反应不可以实现的是
A.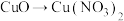 | B.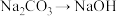 |
C. | D.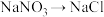 |
您最近一年使用:0次
2023-05-16更新
|
251次组卷
|
2卷引用:江苏省盐城市新丰中学、龙岗中学等五校2022-2023学年高一下学期期中联考化学试题
名校
8 . CuCl常用作有机合成的催化剂,由废铜屑经如下可以转化制得。已知“沉淀”时的反应为[CuCl2]- CuCl↓+2Cl-,Ksp(CuCl)=1×10-6。
CuCl↓+2Cl-,Ksp(CuCl)=1×10-6。
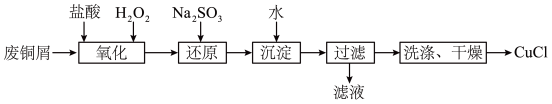
关于转化流程,下列说法正确的是
 CuCl↓+2Cl-,Ksp(CuCl)=1×10-6。
CuCl↓+2Cl-,Ksp(CuCl)=1×10-6。
关于转化流程,下列说法正确的是
| A.“氧化”时每消耗1 mol H2O2,同时生成0.5 mol O2 |
B.“还原”反应的离子方程式为2Cu2++4Cl-+SO +H2O=2[CuCl2]-+SO +H2O=2[CuCl2]-+SO +2H+ +2H+ |
C.SO 与SO 与SO 中“O-S-O”的键角比较:前者>后者 中“O-S-O”的键角比较:前者>后者 |
| D.“滤液”中c(Cu+)=1×10-6 mol·L-1 |
您最近一年使用:0次
名校
解题方法
9 . 氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业,是难溶于水的白色固体,能溶解于硝酸,在潮湿空气中可被迅速氧化。实验室用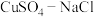 混合液与
混合液与 溶液反应制取CuCl。相关装置及数据如图:
溶液反应制取CuCl。相关装置及数据如图:

回答以下问题:
(1)图甲中仪器1的名称是___________ ;制备过程中 过量会发生副反应生成
过量会发生副反应生成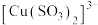 ,为提高产率,仪器2中所加试剂应为
,为提高产率,仪器2中所加试剂应为___________ 。
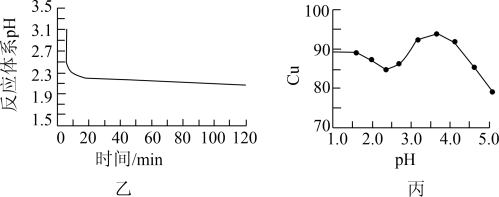
(2)如图乙所示是体系pH随时间变化关系图,写出制备CuCl的离子方程式___________ 。丙图是产率随pH变化关系图,实验过程中往往用 混合溶液代替
混合溶液代替 溶液,其中
溶液,其中 的作用是
的作用是___________ ,为保证较高产率pH应维持在___________ 左右。
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是___________ 。
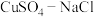 混合液与
混合液与 溶液反应制取CuCl。相关装置及数据如图:
溶液反应制取CuCl。相关装置及数据如图:
回答以下问题:
(1)图甲中仪器1的名称是
 过量会发生副反应生成
过量会发生副反应生成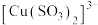 ,为提高产率,仪器2中所加试剂应为
,为提高产率,仪器2中所加试剂应为(2)如图乙所示是体系pH随时间变化关系图,写出制备CuCl的离子方程式
 混合溶液代替
混合溶液代替 溶液,其中
溶液,其中 的作用是
的作用是
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是
您最近一年使用:0次
名校
10 . 废弃的锂离子电池中含有多种金属元素,需回收处理。柠檬酸因具有酸性和较好的络合性,可用于浸出金属离子并得到柠檬酸浸出液。下图是某小组研究从柠檬酸浸出液中分离出铜并制备碱式碳酸铜[xCuCO3∙yCu(OH)2∙zH2O]的制备流程。

(1)在“调pH分离铜”的步骤中,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小于理论分析结果,可能的原因为_______ 。
(2)在“还原法沉铜”的步骤中,利用抗坏血酸(C6H8O6)能有效的将Cu(II)还原成金属Cu。抗坏血酸(C6H8O6)易被氧化为脱氢抗坏血酸(C6H6O6);且受热易分解。
①抗坏血酸还原Cu(OH)2的离子方程式为:_______ 。
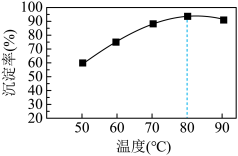
②某实验小组研究了相同条件下温度对Cu沉淀率的影响。从如图可以看出,随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降,下降可能的原因是_______ 。
(3)将所得铜粉制备为CuSO4溶液后再制备碱式碳酸铜。已知碱式碳酸铜的产率随起始n(Na2CO3)与n(CuSO4)的比值和溶液pH的关系如图所示。
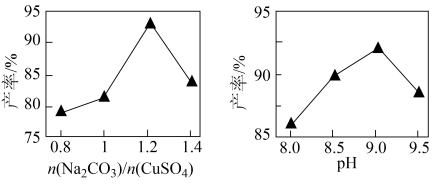
①补充完整由0.5mol/L CuSO4溶液制取碱式碳酸铜的实验方案:向烧杯中加入30mL0.5mol/LNa2CO3溶液,将烧杯置于70℃的水浴中,_______ ,低温烘干,得到碱式碳酸铜。(实验中可选用的试剂或仪器:0.1mol/LBaCl2溶液、0.1mol/LNaOH溶液、0.1mol/L盐酸、pH计)
②实验时发现,若反应时溶液pH过大,所得碱式碳酸铜的产率偏低,但产品中Cu元素含量偏大,原因是_______ 。
③称取9.55g碱式碳酸铜[xCuCO3∙yCu(OH)2∙zH2O]产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。则该产品的化学式为_______ 。

(1)在“调pH分离铜”的步骤中,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小于理论分析结果,可能的原因为
(2)在“还原法沉铜”的步骤中,利用抗坏血酸(C6H8O6)能有效的将Cu(II)还原成金属Cu。抗坏血酸(C6H8O6)易被氧化为脱氢抗坏血酸(C6H6O6);且受热易分解。
①抗坏血酸还原Cu(OH)2的离子方程式为:
②某实验小组研究了相同条件下温度对Cu沉淀率的影响。从如图可以看出,随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降,下降可能的原因是

(3)将所得铜粉制备为CuSO4溶液后再制备碱式碳酸铜。已知碱式碳酸铜的产率随起始n(Na2CO3)与n(CuSO4)的比值和溶液pH的关系如图所示。

①补充完整由0.5mol/L CuSO4溶液制取碱式碳酸铜的实验方案:向烧杯中加入30mL0.5mol/LNa2CO3溶液,将烧杯置于70℃的水浴中,
②实验时发现,若反应时溶液pH过大,所得碱式碳酸铜的产率偏低,但产品中Cu元素含量偏大,原因是
③称取9.55g碱式碳酸铜[xCuCO3∙yCu(OH)2∙zH2O]产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。则该产品的化学式为
您最近一年使用:0次
2023-03-27更新
|
596次组卷
|
2卷引用:江苏省海安高级中学2022-2023学年高三下学期3月月考化学试题



