1 . 氯化亚铜(CuCl)是一种易水解的白色固体。以低品位铜矿砂(主要成分CuS)为原料制备CuCl的工艺流程如图所示。
(1)“酸溶1”时,CuS作_______ (填“氧化剂”或“还原剂”)。
(2)“除锰”时,Cu2+转化为Cu(NH3)4CO3,Mn2+转化为MnCO3沉淀。沉锰的反应化学方程式为_______ 。将生成的MnCO3分离出来的实验操作为_______ 。
(3)“酸溶2”投料后,以一定的速率搅拌反应,可提高铜浸出率的措施有_______ (只答一种方法)。
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生_______ 气体。
(5)“洗涤”应先用稀盐酸洗涤,其目的是_______ 。

(1)“酸溶1”时,CuS作
(2)“除锰”时,Cu2+转化为Cu(NH3)4CO3,Mn2+转化为MnCO3沉淀。沉锰的反应化学方程式为
(3)“酸溶2”投料后,以一定的速率搅拌反应,可提高铜浸出率的措施有
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生
(5)“洗涤”应先用稀盐酸洗涤,其目的是
您最近一年使用:0次
名校
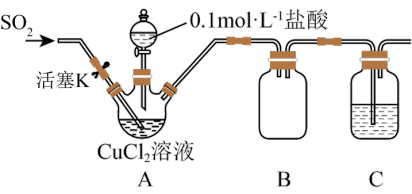
2 . 氯化亚铜(CuCl)是一种重要的化工原料,化学小组用如图装置(部分夹持装置略去)制备CuCl。
②在酸性条件下,某些中间价态的离子能发生自身氧化还原反应。
实验步骤:
I.打开分液漏斗活塞,向三颈瓶中加盐酸调pH至2~3,打开活塞K,通入SO2,溶液中产生白色沉淀,待反应完全后,再通一段时间气体。
Ⅱ.将反应混合液过滤、洗涤、干燥得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)装置B的作用是_______ ,置C中的试剂为_______ 。
(2)步骤I中通入SO2发生反应的离子方程式是_______ 。
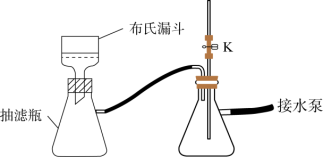
(3)步骤Ⅱ中采用抽滤法过滤的主要目的是:_____ ;抽滤采用下图装置。滤完毕需进行下列操作,从实验安全角度考虑,你认为最合理的第一步操作为_______ (填标号)。
(4)某小组同学发现,将分液漏斗中的0.1 mol·L-1盐酸换为6 mol·L-1盐酸,通入SO2,最终未得到白色沉淀。对此现象有如下猜想:
猜想一:Cl-浓度过大,与CuCl发生反应查阅资料知: CuCl+Cl- CuCl
CuCl ,据此设计实验:将上述未得到沉淀的溶液
,据此设计实验:将上述未得到沉淀的溶液__________ (填操作),若观察到有白色沉淀析出,证明猜想一正确。
猜想二:________ 。设计验证猜想二是否成立的实验方案:________ 。
②在酸性条件下,某些中间价态的离子能发生自身氧化还原反应。
实验步骤:
I.打开分液漏斗活塞,向三颈瓶中加盐酸调pH至2~3,打开活塞K,通入SO2,溶液中产生白色沉淀,待反应完全后,再通一段时间气体。
Ⅱ.将反应混合液过滤、洗涤、干燥得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)装置B的作用是
(2)步骤I中通入SO2发生反应的离子方程式是
(3)步骤Ⅱ中采用抽滤法过滤的主要目的是:
(4)某小组同学发现,将分液漏斗中的0.1 mol·L-1盐酸换为6 mol·L-1盐酸,通入SO2,最终未得到白色沉淀。对此现象有如下猜想:
猜想一:Cl-浓度过大,与CuCl发生反应查阅资料知: CuCl+Cl-
 CuCl
CuCl ,据此设计实验:将上述未得到沉淀的溶液
,据此设计实验:将上述未得到沉淀的溶液猜想二:
您最近一年使用:0次
解题方法
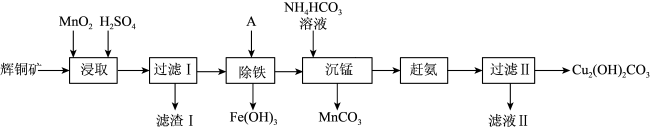
3 . 用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备难溶于水的碱式碳酸铜的流程如下:
(1)下列措施能加快浸取速率的是___________ 。(填字母)
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)滤渣I中的主要成分是MnO2、S、SiO2,写出“浸取”反应中生成S的离子方程式:___________ 。
(3)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是___________。
(4)“沉锰”(除Mn2+)过程中有关反应的离子方程式为___________ 。
(5)滤液Ⅱ所含溶质主要是___________ (填化学式)。

(1)下列措施能加快浸取速率的是
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)滤渣I中的主要成分是MnO2、S、SiO2,写出“浸取”反应中生成S的离子方程式:
(3)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是___________。
| A.CO2 | B.CuO | C.氨水 | D.HCl |
(4)“沉锰”(除Mn2+)过程中有关反应的离子方程式为
(5)滤液Ⅱ所含溶质主要是
您最近一年使用:0次
名校
4 . 下列物质的俗称与化学式不对应的是
A.胆矾— | B.生石膏— |
C.小苏打— | D.铁红— |
您最近一年使用:0次
2021-01-05更新
|
171次组卷
|
2卷引用:海南省儋州市第二中学2020-2021学年高一下学期3月月考化学试题
5 . 向CuSO4溶液中滴加氨水至过量,下列叙述正确的是
| A.先出现沉淀,后沉淀溶解变为无色溶液 |
| B.离子方程式为Cu2+ + 4NH3·H2O = [Cu(NH3)4]2+ + 4H2O |
| C.Cu2+与 NH3中的氮原子以π键结合 |
| D.NH3分子中∠HNH为109º28ˊ |
您最近一年使用:0次
2020-10-12更新
|
3760次组卷
|
13卷引用:2020年海南省高考化学试卷(新高考)
2020年海南省高考化学试卷(新高考)(已下线)2020年海南卷化学高考真题变式题1-8福建省厦门集美中学2021-2022学年高二下学期第一次月考化学试题天津市静海区四校2021-2022学年高三上学期12月阶段性检测化学试题(已下线)第10讲 金属材料及金属矿物的开发利用(练)-2023年高考化学一轮复习讲练测(全国通用)河南省南阳市第六完全学校高级中学2021-2022学年高二下学期4月月考化学试题福建省厦门市国祺中学2021-2022学年高三上学期第二次月考化学试题山东省菏泽市单县二中2021-2022学年高二下学期开学考试 化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)广东省汕头市2022-2023学年高二下学期7月期末考试化学试题(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第7讲 配合物与超分子北京市第一六一中学2021-2022学年高三上学期期中考试化学试题
解题方法
6 . 我国古代在冶炼金属方面成就显著,请回答:
(1)商代司母戊鼎属于_____ (选填“青铜”、“铁合金”或“铝合金”)制品。
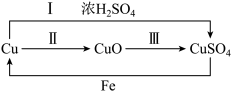
(2)下图为铜及其化合物之间的转化关系(反应条件略去):
①上述转化常伴随颜色的变化,紫红色的铜与氧气反应生成______ 色的氧化铜;
②“曾青得铁则化为铜”体现了我国古代湿法炼铜的原理,其中的反应有:Fe + CuSO4 = FeSO4 + Cu,由此可知铁比铜的金属活动性________ (选填写“强”或“弱”);
③为验证铜和浓硫酸反应生成的气体,将气体通入品红溶液,观察到的现象是_______ ;
④由上图可知,制备硫酸铜可以用途径甲(反应Ⅰ)或途径乙(反应Ⅱ+Ⅲ),从环保角度考虑,应选择途径________ (选填“甲”或“乙”),理由是_____ 。
(1)商代司母戊鼎属于
(2)下图为铜及其化合物之间的转化关系(反应条件略去):

①上述转化常伴随颜色的变化,紫红色的铜与氧气反应生成
②“曾青得铁则化为铜”体现了我国古代湿法炼铜的原理,其中的反应有:Fe + CuSO4 = FeSO4 + Cu,由此可知铁比铜的金属活动性
③为验证铜和浓硫酸反应生成的气体,将气体通入品红溶液,观察到的现象是
④由上图可知,制备硫酸铜可以用途径甲(反应Ⅰ)或途径乙(反应Ⅱ+Ⅲ),从环保角度考虑,应选择途径
您最近一年使用:0次



