1 . 氯化铜晶体(CuCl2·2H2O)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗制氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:

已知:氯化亚砜( 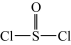 )熔点-101℃,沸点76℃,易水解。回答下列问题:
)熔点-101℃,沸点76℃,易水解。回答下列问题:
(1)为避免引入杂质,试剂x可选用___________ (填字母)
a.KMnO4溶液 b.Cl2水 c.Br2水 d.H2O2溶液
(2)溶液C中加入试剂y可以调节溶液pH,控制pH的取值范围为______~________________ ,从而除去Fe3+而不引入杂质。试剂y可选用下列物质中的___________ (填字母)
a.Cu b.CuO c.Cu2(OH)2CO3 d.NaOH
(3)SOCl2与水反应的化学方程式为___________ 。
(4)SOCl2与CuCl2·2H2O混合并加热,可得到无水CuCl2的原因是__________________ 。

| Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全的pH | 3.2 | 9.0 | 6.7 |
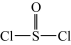 )熔点-101℃,沸点76℃,易水解。回答下列问题:
)熔点-101℃,沸点76℃,易水解。回答下列问题:(1)为避免引入杂质,试剂x可选用
a.KMnO4溶液 b.Cl2水 c.Br2水 d.H2O2溶液
(2)溶液C中加入试剂y可以调节溶液pH,控制pH的取值范围为______~_____
a.Cu b.CuO c.Cu2(OH)2CO3 d.NaOH
(3)SOCl2与水反应的化学方程式为
(4)SOCl2与CuCl2·2H2O混合并加热,可得到无水CuCl2的原因是
您最近半年使用:0次
名校
2 . 工业上,处理低品位黄铜矿[二硫化亚铁铜( )含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(
)含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾( )和胆矾(
)和胆矾( ),相关流程如下图。
),相关流程如下图。
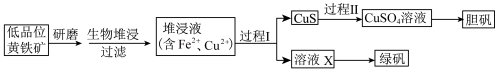
资料:①生物堆浸使用的氧化亚铁硫杆菌(T。f细菌)在pH1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
(1)生物堆浸前,需先将矿石进行研磨,目的是___________ 。
(2)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为: 。第二阶段反应为
。第二阶段反应为 继续被氧化转变成
继续被氧化转变成 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)生物堆浸过程中,应控制溶液的pH在___________ 范围内。
(4) 在过程Ⅰ中被还原为
在过程Ⅰ中被还原为 。
。
①若过程Ⅰ中只加入一种试剂,在下列常见还原剂中可选择___________ 。
a. b.
b. c.
c. d.Cu
d.Cu
② 做还原剂时,通常被氧化为
做还原剂时,通常被氧化为 。过程Ⅰ中若加入
。过程Ⅰ中若加入 固体,则发生反应的离子方程式有
固体,则发生反应的离子方程式有___________ 、___________ (忽略该过程中所有涉及配合物的反应)。
③为判断堆浸液中 是否被完全还原,可取少量溶液X,向其中加入
是否被完全还原,可取少量溶液X,向其中加入___________ (填试剂的化学式),观察溶液颜色变化。
(5)向过程Ⅰ所得固体中加入___________ (填试剂的化学式),过滤,可得CuS固体。然后加 和稀硫酸,CuS
和稀硫酸,CuS完全溶解 ,用离子方程式表示 的作用是
的作用是___________ 。
 )含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(
)含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾( )和胆矾(
)和胆矾( ),相关流程如下图。
),相关流程如下图。
资料:①生物堆浸使用的氧化亚铁硫杆菌(T。f细菌)在pH1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
 |  |  | |
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
(1)生物堆浸前,需先将矿石进行研磨,目的是
(2)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:
 。第二阶段反应为
。第二阶段反应为 继续被氧化转变成
继续被氧化转变成 ,反应的离子方程式为
,反应的离子方程式为(3)生物堆浸过程中,应控制溶液的pH在
(4)
 在过程Ⅰ中被还原为
在过程Ⅰ中被还原为 。
。①若过程Ⅰ中只加入一种试剂,在下列常见还原剂中可选择
a.
 b.
b. c.
c. d.Cu
d.Cu②
 做还原剂时,通常被氧化为
做还原剂时,通常被氧化为 。过程Ⅰ中若加入
。过程Ⅰ中若加入 固体,则发生反应的离子方程式有
固体,则发生反应的离子方程式有③为判断堆浸液中
 是否被完全还原,可取少量溶液X,向其中加入
是否被完全还原,可取少量溶液X,向其中加入(5)向过程Ⅰ所得固体中加入
 和稀硫酸,CuS
和稀硫酸,CuS 的作用是
的作用是
您最近半年使用:0次
3 . 下图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。
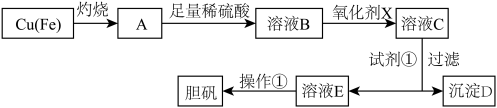
部分正离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)铜原子的价电子排布式为___________ 。
(2)若恰好完全沉淀时, 的浓度为
的浓度为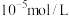 ,则常温下氢氧化铜的
,则常温下氢氧化铜的
___________ (用科学计数法表示)。
(3)溶液B中含有的金属离子有___________ (填离子符号)。
(4)下列物质中可以做氧化剂X的是___________(不定项)。
(5)试剂①可通过调节pH除去 。沉淀D的化学式为
。沉淀D的化学式为___________ ,试剂①可以选择___________ (填化学式),操作时需控制pH值的范围为___________ 。
(6)写出实验室配制 溶液的方法:
溶液的方法:___________ 。
(7)溶液E经过操作①可得到胆矾,操作①为___________ 、___________ 、过滤、洗涤、干燥。

部分正离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |  |  |  |
| 开始沉淀 | 2.7 | 7.5 | 4.4 |
| 完全沉淀 | 3.7 | 9.7 | 6.7 |
(1)铜原子的价电子排布式为
(2)若恰好完全沉淀时,
 的浓度为
的浓度为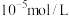 ,则常温下氢氧化铜的
,则常温下氢氧化铜的
(3)溶液B中含有的金属离子有
(4)下列物质中可以做氧化剂X的是___________(不定项)。
A. | B. | C. | D.氧气 |
(5)试剂①可通过调节pH除去
 。沉淀D的化学式为
。沉淀D的化学式为(6)写出实验室配制
 溶液的方法:
溶液的方法:(7)溶液E经过操作①可得到胆矾,操作①为
您最近半年使用:0次
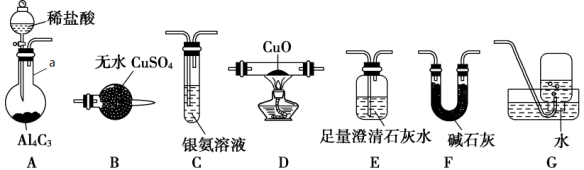
4 . 甲烷在加热条件下可还原氧化铜,某化学小组利用如图装置探究其反应产物。
查阅资料:①CO能与银氨溶液反应:
②Cu2O为红色,能发生反应: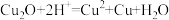
(1)仪器a的名称是___________ ,装置A中反应的化学方程式为___________ 。
(2)按气流方向各装置从左到右的连接顺序为A→F→D→___________→___________→___________→G(填字母编号)。___________
(3)已知气体产物中含有CO,则装置C中可观察到的现象是___________ ;装置F的作用为___________ 。
(4)当反应结束后,装置D处试管中固体全部变为红色。
①设计简单实验证明红色固体中含有 :
:___________ 。
②若红色固体为单质,且产物中含碳氧化物的物质的量之比为 ,则D处发生的反应化学方程式是
,则D处发生的反应化学方程式是___________ 。

查阅资料:①CO能与银氨溶液反应:

②Cu2O为红色,能发生反应:
(1)仪器a的名称是
(2)按气流方向各装置从左到右的连接顺序为A→F→D→___________→___________→___________→G(填字母编号)。
(3)已知气体产物中含有CO,则装置C中可观察到的现象是
(4)当反应结束后,装置D处试管中固体全部变为红色。
①设计简单实验证明红色固体中含有
 :
:②若红色固体为单质,且产物中含碳氧化物的物质的量之比为
 ,则D处发生的反应化学方程式是
,则D处发生的反应化学方程式是
您最近半年使用:0次
名校
解题方法
5 . 氯化亚铜(CuCl)是白色粉末,微溶于水,酸性条件下不稳定,易生成金属Cu和Cu2+,广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuC12•2H2O制备CuCl,并进行相关探究。下列说法不正确的是
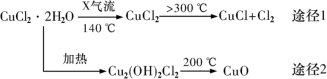
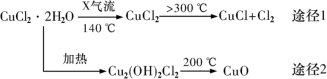
| A.途径1中产生的Cl2可以回收循环利用 |
B.途径2中200℃时反应的化学方程式为:Cu2(OH)2Cl2 2CuO+2HCl↑ 2CuO+2HCl↑ |
C.CuCl与稀硫酸反应的离子方程式为:2CuCl+4H++SO =2Cu2++2Cl-+SO2↑+2H2O =2Cu2++2Cl-+SO2↑+2H2O |
| D.X气体是HCl,目的是抑制CuCl2•2H2O加热过程可能的水解 |
您最近半年使用:0次
2021-03-17更新
|
478次组卷
|
14卷引用:浙江省淳安县汾口中学2020-2021学年高二3月月考化学试题
浙江省淳安县汾口中学2020-2021学年高二3月月考化学试题江西省南昌市第二中学2020届高三第四次月考化学试题江西省顶级名校2020届高三第四次联考化学试题浙江省宁波市效实中学2020届高三上学期第一次模拟考试化学试题江西省南昌市新建县第一中学2020届高三上学期第二次月考化学试题山西省晋中市平遥县和诚中学2020届高三上学期12月月考化学试题江西省南昌市进贤一中2019-2020学年高一上学期第二次月考化学试题2020届高三《新题速递·化学》12月第02期(考点01-06)黑龙江省哈尔滨师范大学附属中学2020-2021学年高三上学期开学考试化学试题江西省南昌市第二中学2021届高三上学期第三次考试化学试题(已下线)【南昌新东方】2. 南昌二中 左佳鑫浙江省宁波市慈溪市2021届高三适应性测试化学试题北京市昌平区新学道临川学校2021届高三上学期期末考试化学试题江西省宜春市丰城市第九中学2021-2022学年高三上学期第三次月考化学试题
20-21高三上·浙江绍兴·期中
解题方法
6 . I.由三种元素组成的化合物A,其相对分子质量小于200,按如下流程进行实验。气体B为红棕色混合物,气体D能使带火星的木条复燃,溶液E为蓝色,固体C为混合物,固体F为紫红色。

请回答:
(1)组成A的三种元素是_______ 。(填元素符号),A的化学式是________ 。
(2)固体A加热分解的化学方程式是________ 。
(3)若固体G的组成与A类似,且隔绝空气加热后红棕色气体与带火星木条复燃气体的物质的量为8:1,该反应的化学方程式是。___________ 。
II.某兴趣小组为制取并验证二氧化硫的性质进行相关实验,实验装置如图所示。请回答:
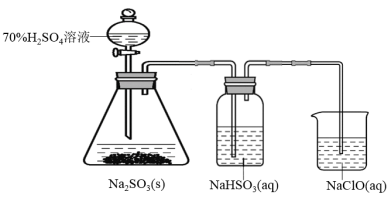
(1)饱和NaHSO3溶液的作用是___________ 。
(2)写出烧杯中过量的NaClO溶液吸收SO2的离子反应方程式___________ 。

请回答:
(1)组成A的三种元素是
(2)固体A加热分解的化学方程式是
(3)若固体G的组成与A类似,且隔绝空气加热后红棕色气体与带火星木条复燃气体的物质的量为8:1,该反应的化学方程式是。
II.某兴趣小组为制取并验证二氧化硫的性质进行相关实验,实验装置如图所示。请回答:

(1)饱和NaHSO3溶液的作用是
(2)写出烧杯中过量的NaClO溶液吸收SO2的离子反应方程式
您最近半年使用:0次
名校
解题方法
7 . 绿色植物标本用醋酸铜[(CH3COO)2Cu]处理后颜色更鲜艳、稳定。某化学小组制备醋酸铜晶体并测定产品中铜的含量,实验如下。
Ⅰ.醋酸铜晶体的制备中

(1)用离子方程式表示过程①产物中OH-的来源:___________ ;
(2)过程②对应的化学方程式是:___________ 。
Ⅱ.测定产品中铜的含量
i.取ag醋酸铜产品放入带磨口塞子的锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产Cul沉淀,溶液呈棕黄色;
ii.用b mol·L -1Na2S2O3标准溶液滴定i中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;(已知:2 +I2=
+I2= +2I-)
+2I-)
iii.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
iv.继续用Na2S2O3标准溶液滴定中浊液至终点,消耗标准溶液vmL。
已知:①Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②Cul易吸附I2,被吸附的I2不与淀粉发 CuSCN生显色反应。难溶于水且不吸附I2
(3)i中发生反应的离子方程式是_________ ;
(4)醋酸铜产品中铜元素的质量分数是_______ 。
Ⅰ.醋酸铜晶体的制备中

(1)用离子方程式表示过程①产物中OH-的来源:
(2)过程②对应的化学方程式是:
Ⅱ.测定产品中铜的含量
i.取ag醋酸铜产品放入带磨口塞子的锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产Cul沉淀,溶液呈棕黄色;
ii.用b mol·L -1Na2S2O3标准溶液滴定i中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;(已知:2
 +I2=
+I2= +2I-)
+2I-)iii.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
iv.继续用Na2S2O3标准溶液滴定中浊液至终点,消耗标准溶液vmL。
已知:①Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②Cul易吸附I2,被吸附的I2不与淀粉发 CuSCN生显色反应。难溶于水且不吸附I2
(3)i中发生反应的离子方程式是
(4)醋酸铜产品中铜元素的质量分数是
您最近半年使用:0次
名校
解题方法
8 . 以铜片(含少量杂质铁)为原料制取Cu(NO3)2溶液的实验流程如图:
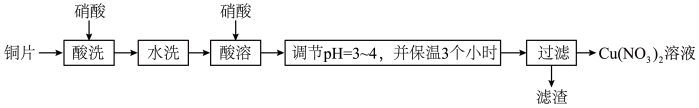
(1)“酸洗”的目的是除去铜片表面难溶的Cu2(OH)2SO4,写出“酸洗”时反应的离子方程式:___ 。
(2)“水洗”后检验铜片表面是否洗涤干净的方法是___ 。
(3)“酸溶”时的装置如图所示,烧杯内所发生的反应为:
NO+NO2+2OH-=2NO2-+H2O
2NO2+2OH-=NO2-+NO3-+H2O
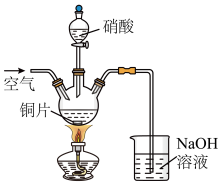
①“酸溶”时为防止反应过于剧烈,可以采取的方法有___ 和___ 。
②通入空气的作用是___ 、___ 。
(4)“调节pH=3~4,并保温3个小时”的目的是___ 。
(5)烧杯中所得溶液经多步处理得到NaNO3固体。设计以烧杯中所得溶液为原料,制取NaNO3固体的实验方案:___ 。
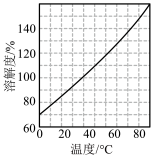
[已知3NaNO2+2HNO3=3NaNO3+2NO↑+H2O;NaNO3的溶解度随温度变化如图所示。实验中必须使用的试剂:硝酸和NaOH溶液]。

(1)“酸洗”的目的是除去铜片表面难溶的Cu2(OH)2SO4,写出“酸洗”时反应的离子方程式:
(2)“水洗”后检验铜片表面是否洗涤干净的方法是
(3)“酸溶”时的装置如图所示,烧杯内所发生的反应为:
NO+NO2+2OH-=2NO2-+H2O
2NO2+2OH-=NO2-+NO3-+H2O

①“酸溶”时为防止反应过于剧烈,可以采取的方法有
②通入空气的作用是
(4)“调节pH=3~4,并保温3个小时”的目的是
(5)烧杯中所得溶液经多步处理得到NaNO3固体。设计以烧杯中所得溶液为原料,制取NaNO3固体的实验方案:
[已知3NaNO2+2HNO3=3NaNO3+2NO↑+H2O;NaNO3的溶解度随温度变化如图所示。实验中必须使用的试剂:硝酸和NaOH溶液]。

您最近半年使用:0次
2020-05-09更新
|
129次组卷
|
2卷引用:江苏省南京市第九中学2023-2024学年高二上学期期末化学试卷
9 . 铜及其化合物在生产生活中有广泛应用
(1)工业上以黄铜矿(CuFeS2) 为原料,采用火法熔炼工艺生产铜的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑ 该反应的氧化剂是
6Cu+SO2↑ 该反应的氧化剂是________________ ,验证SO2的方法是________________ 。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜。温度控制在50℃~60℃的原因有:①加快反应速率;②___________ 。在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热,可生成CuC1沉淀,写出生成CuCl的离子方程式______________ 。
(3)碱式碳酸铜在有机催化剂、烟火制造和颜料、农药生产中有广泛的应用。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备碱式碳酸铜的流程如下:
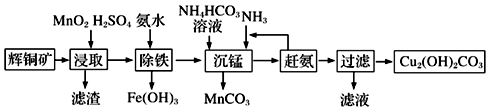
①辉铜矿在浸取前要富集与粉碎,粉碎的好处是___________ 。
②浸取过程中可得到一种黄色单质,写出浸取时主要反应的化学方程式___________ 。
③“除铁”这一步反应在25℃进行,加入氨水调节溶液pH为4后,溶液中铜离子最大浓度不超过_________ mol/L。(已知Ksp[Cu(OH)2]=2.2×10-20)
(1)工业上以黄铜矿(CuFeS2) 为原料,采用火法熔炼工艺生产铜的中间过程会发生反应:2Cu2O+Cu2S
 6Cu+SO2↑ 该反应的氧化剂是
6Cu+SO2↑ 该反应的氧化剂是(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜。温度控制在50℃~60℃的原因有:①加快反应速率;②
(3)碱式碳酸铜在有机催化剂、烟火制造和颜料、农药生产中有广泛的应用。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备碱式碳酸铜的流程如下:

①辉铜矿在浸取前要富集与粉碎,粉碎的好处是
②浸取过程中可得到一种黄色单质,写出浸取时主要反应的化学方程式
③“除铁”这一步反应在25℃进行,加入氨水调节溶液pH为4后,溶液中铜离子最大浓度不超过
您最近半年使用:0次
2018-08-30更新
|
297次组卷
|
2卷引用:【全国省级联考】广东省2017-2018学年高二第二学期期末检测理科综合化学试题



