1 . 加强废旧金属的回收和再利用,是合理开发和利用金属资源的主要途径之一。下图是从镀铜废电路板中回收金属铜的一种工艺流程(各过程需控制适宜条件)。
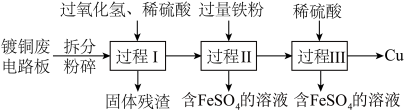
(1)上述流程中,为加快化学反应速率而采取的措施是______ 。
(2)过程Ⅰ中,Cu溶解,过氧化氢的作用是______ 。
(3)过程Ⅱ中,获得Cu的反应的离子方程式为______ 。
(4)过程Ⅲ的目的是______ 。

(1)上述流程中,为加快化学反应速率而采取的措施是
(2)过程Ⅰ中,Cu溶解,过氧化氢的作用是
(3)过程Ⅱ中,获得Cu的反应的离子方程式为
(4)过程Ⅲ的目的是
您最近一年使用:0次
2020-08-04更新
|
300次组卷
|
5卷引用:江苏省宿迁市泗阳县桃州中学2020-2021学年高二上学期第一次调研考试化学试题
解题方法
2 . 某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu(NO3)2的部分工艺流程如图所示:
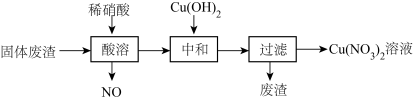
(1)写出CuO、Cu2O分别与稀硝酸反应的离子方程式为:______ 、______ 。
(2)酸溶时,反应温度不宜超过70℃,其主要原因是______ ,若保持反应温度为70℃,欲加快反应速率可采取的措施为______ (写出一种即可)。
(3)过滤后所得废渣的主要成分的化学式为______ 。
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为______ 。由Cu(NO3)2溶液制Cu(NO3)2·6H2O晶体的操作方法是:蒸发浓缩、______ 、过滤、冰水洗涤、______ 。

(1)写出CuO、Cu2O分别与稀硝酸反应的离子方程式为:
(2)酸溶时,反应温度不宜超过70℃,其主要原因是
(3)过滤后所得废渣的主要成分的化学式为
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为
您最近一年使用:0次
3 . 氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl微溶于水,不溶于稀酸,可溶于Cl-浓度较大的体系,在潮湿的空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
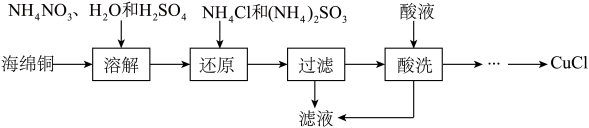
(1)基态铜原子核外电子排布式为:________ 。
(2)为了提高溶解速率,可以适当加热到60~70℃,还可以采用的措施为________ 。
(3)溶解步骤的温度控制在60~70℃,温度不宜过高的原因是________ 。该步骤中Cu 与NH4NO3反应的离子方程式为 (N元素被还原到最低价)_________________ 。
(4)还原步骤发生反应的离子方程式为______________________ 。
(5)滤液的主要成分为__________ (写化学式)。
(6)酸洗时,可选用稀硫酸或稀盐酸,但不能用浓盐酸的原因是_________________ 。

(1)基态铜原子核外电子排布式为:
(2)为了提高溶解速率,可以适当加热到60~70℃,还可以采用的措施为
(3)溶解步骤的温度控制在60~70℃,温度不宜过高的原因是
(4)还原步骤发生反应的离子方程式为
(5)滤液的主要成分为
(6)酸洗时,可选用稀硫酸或稀盐酸,但不能用浓盐酸的原因是
您最近一年使用:0次
名校
4 . 实验室以海绵铜(主要成分为Cu和CuO)为原料制取CuCl的主要流程如图所示。
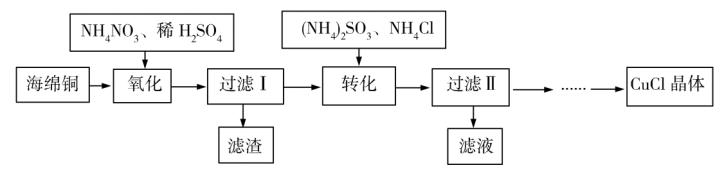
已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60℃~70℃,原因是___ 。
(2)写出“转化”过程中的离子方程式___ 。
(3)“过滤Ⅱ”所得滤液经蒸发浓缩、降温结晶、过滤等操作获得(NH4)2SO4晶体,可用作化学肥料。“过滤Ⅱ”所得滤渣主要成分为CuCl,用乙醇洗涤的优点是___ 。
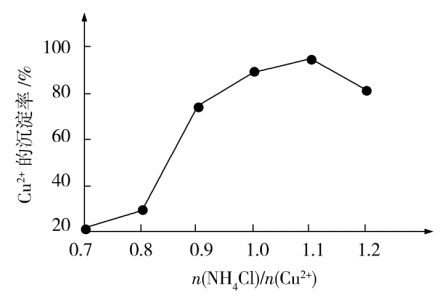
(4)氯化铵用量 与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是___ 。
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:___ 。(实验中可选试剂:0.1mol·L-1盐酸、10mol·L-1盐酸、蒸馏水、无水乙醇)

已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60℃~70℃,原因是
(2)写出“转化”过程中的离子方程式
(3)“过滤Ⅱ”所得滤液经蒸发浓缩、降温结晶、过滤等操作获得(NH4)2SO4晶体,可用作化学肥料。“过滤Ⅱ”所得滤渣主要成分为CuCl,用乙醇洗涤的优点是
(4)氯化铵用量
 与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:
您最近一年使用:0次
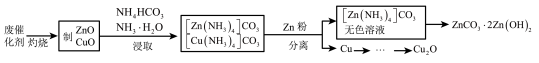
5 . 实验室以合成氨(低温变换的)废催化剂(主要含Zn、Cu的单质和氧化物)为原料制取ZnCO3·2Zn(OH)2和Cu2O,其实验流程如图:
(1)“灼烧”时,需用的硅酸盐质仪器除玻璃棒、酒精灯外,还有___ 和___ 。
(2)“浸取”时,生成[Zn(NH3)4]CO3的离子方程式为___ 。
(3)加“Zn粉”时,为使Zn粉不过量太多{已知:溶液中[Cu(NH3)4]2+呈深蓝色},合适的操作方法及依据的现象是___ ;分离出的铜粉中混有少量Zn,提纯铜粉的方案是__ 。
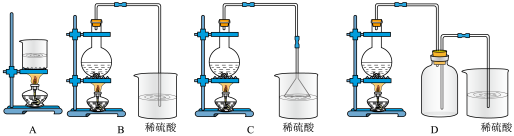
(4)已知反应:[Zn(NH3)4]2+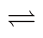 Zn2++4NH3,K=3.5×10-10,由[Zn(NH3)4]CO3溶液制取ZnCO3·2Zn(OH)2,可采用的装置是
Zn2++4NH3,K=3.5×10-10,由[Zn(NH3)4]CO3溶液制取ZnCO3·2Zn(OH)2,可采用的装置是___ (填字母)。
(5)设计以提纯后的铜粉为原料制取Cu2O的实验方案:向烧杯中加入计量的铜粉,__ ,静置、冷却、过滤、水洗及干燥[已知在约50℃时,发生反应:Cu+H2O2+H2SO4=CuSO4+2H2O。实验中必须使用的试剂:稀硫酸、葡萄糖溶液、10%的NaOH溶液和15%的H2O2溶液]。

(1)“灼烧”时,需用的硅酸盐质仪器除玻璃棒、酒精灯外,还有
(2)“浸取”时,生成[Zn(NH3)4]CO3的离子方程式为
(3)加“Zn粉”时,为使Zn粉不过量太多{已知:溶液中[Cu(NH3)4]2+呈深蓝色},合适的操作方法及依据的现象是
(4)已知反应:[Zn(NH3)4]2+
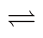 Zn2++4NH3,K=3.5×10-10,由[Zn(NH3)4]CO3溶液制取ZnCO3·2Zn(OH)2,可采用的装置是
Zn2++4NH3,K=3.5×10-10,由[Zn(NH3)4]CO3溶液制取ZnCO3·2Zn(OH)2,可采用的装置是
(5)设计以提纯后的铜粉为原料制取Cu2O的实验方案:向烧杯中加入计量的铜粉,
您最近一年使用:0次
名校
解题方法
6 . 某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu(NO3)2的部分工艺流程如图所示:
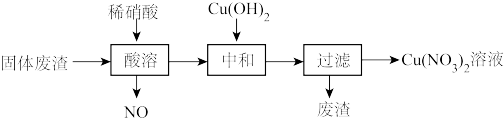
(1)Cu与稀硝酸反应的离子方程式为___ 。
(2)酸溶时,反应温度不宜超过70℃,其主要原因是___ ,若保持反应温度为70℃,欲加快反应速率可采取的措施为___ (写出一种即可)。
(3)过滤后所得废渣的主要成分的化学式为___ 。
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为___ ,由Cu(NO3)2溶液制备Cu(NO3)2晶体的操作方法是:蒸发浓缩、冷却结晶、过滤、___ 、___ 。

(1)Cu与稀硝酸反应的离子方程式为
(2)酸溶时,反应温度不宜超过70℃,其主要原因是
(3)过滤后所得废渣的主要成分的化学式为
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为
您最近一年使用:0次
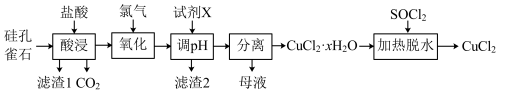
7 . 以硅孔雀石[主要成分为CuCO3·Cu(OH)2、CuSiO3·2H2O,含SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如图:
已知:SOCl2+H2O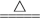 SO2↑+2HCl↑
SO2↑+2HCl↑
(1)“酸浸”时盐酸与CuCO3·Cu(OH)2反应的化学方程式为___ 。为提高“酸浸”时铜元素的浸出率,可以采取的措施有:①适当提高盐酸浓度;②适当提高反应温度;③___ 。
(2)“氧化”时发生反应的离子方程式为___ 。
(3)“滤渣2”的主要成分为___ (填化学式);“调pH”时,pH不能过高,其原因是___ 。

已知:SOCl2+H2O
 SO2↑+2HCl↑
SO2↑+2HCl↑(1)“酸浸”时盐酸与CuCO3·Cu(OH)2反应的化学方程式为
(2)“氧化”时发生反应的离子方程式为
(3)“滤渣2”的主要成分为
您最近一年使用:0次
名校
解题方法
8 . 以铜片(含少量杂质铁)为原料制取Cu(NO3)2溶液的实验流程如图:
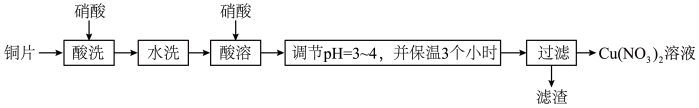
(1)“酸洗”的目的是除去铜片表面难溶的Cu2(OH)2SO4,写出“酸洗”时反应的离子方程式:___ 。
(2)“水洗”后检验铜片表面是否洗涤干净的方法是___ 。
(3)“酸溶”时的装置如图所示,烧杯内所发生的反应为:
NO+NO2+2OH-=2NO2-+H2O
2NO2+2OH-=NO2-+NO3-+H2O
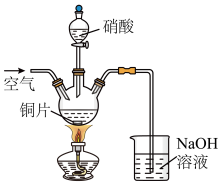
①“酸溶”时为防止反应过于剧烈,可以采取的方法有___ 和___ 。
②通入空气的作用是___ 、___ 。
(4)“调节pH=3~4,并保温3个小时”的目的是___ 。
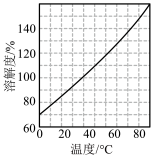
(5)烧杯中所得溶液经多步处理得到NaNO3固体。设计以烧杯中所得溶液为原料,制取NaNO3固体的实验方案:___ 。
[已知3NaNO2+2HNO3=3NaNO3+2NO↑+H2O;NaNO3的溶解度随温度变化如图所示。实验中必须使用的试剂:硝酸和NaOH溶液]。

(1)“酸洗”的目的是除去铜片表面难溶的Cu2(OH)2SO4,写出“酸洗”时反应的离子方程式:
(2)“水洗”后检验铜片表面是否洗涤干净的方法是
(3)“酸溶”时的装置如图所示,烧杯内所发生的反应为:
NO+NO2+2OH-=2NO2-+H2O
2NO2+2OH-=NO2-+NO3-+H2O

①“酸溶”时为防止反应过于剧烈,可以采取的方法有
②通入空气的作用是
(4)“调节pH=3~4,并保温3个小时”的目的是
(5)烧杯中所得溶液经多步处理得到NaNO3固体。设计以烧杯中所得溶液为原料,制取NaNO3固体的实验方案:
[已知3NaNO2+2HNO3=3NaNO3+2NO↑+H2O;NaNO3的溶解度随温度变化如图所示。实验中必须使用的试剂:硝酸和NaOH溶液]。

您最近一年使用:0次
2020-05-09更新
|
139次组卷
|
2卷引用:江苏省如皋中学2020届高三阶段检测化学试题
2020·江苏·模拟预测
解题方法
9 . 实验室以海绵铜(主要成分为Cu和CuO)为原料制取CuCl的主要流程如图所示。
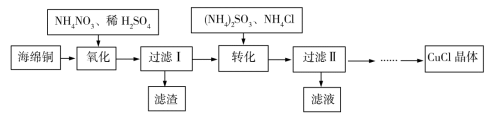
已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60~70℃,原因是____________________ 。
(2)写出“转化”过程中的离子方程式____________________ 。
(3)“过滤Ⅱ”所得滤液经__________ 、__________ 、过滤等操作获得(NH4)2SO4晶体,可用作化学肥料。“过滤Ⅱ”所得滤渣主要成分为CuCl,用乙醇洗涤的优点是________________ 。
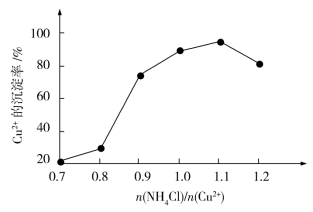
(4)氯化铵用量[ ]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是__________ 。
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:__________ 。(实验中可选试剂:0.1 mol·L−1盐酸、10 mol·L−1盐酸、蒸馏水、无水乙醇)

已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60~70℃,原因是
(2)写出“转化”过程中的离子方程式
(3)“过滤Ⅱ”所得滤液经
(4)氯化铵用量[
 ]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:
您最近一年使用:0次
解题方法
10 . 实验室以海绵铜(主要成分为Cu和CuO)为原料制取CuCl的主要流程如图:
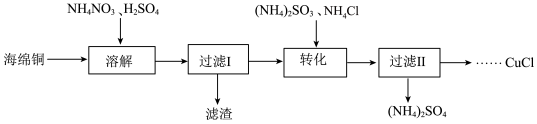
已知:①CuCl为白色固体,难溶于水和乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl有水存在时在空气中易被氧化,在酸性条件下较稳定。
(1)“溶解”时选用约为0.5mol•L-1的硫酸,过程中无气体产生。若硫酸浓度过大,反应会产生NO、NO2等有害气体,NH4NO3的用量会___ (填“增大”或“减小”或“不变”)。
(2)“转化”步骤中发生反应的离子方程式为___ 。加入的(NH4)2SO3需要适当过量的原因是__ 。
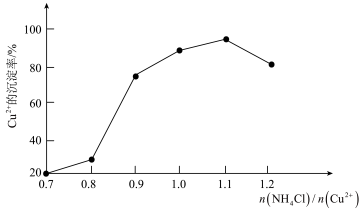
(3)氯化铵用量[ ]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,其原因是
]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,其原因是___ 。
(4)检验CuCl沉淀是否洗涤完全的方法是___ 。
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:__ 。(实验中可选试剂:0.1mol•L-1盐酸、10mol•L-1盐酸、蒸馏水、无水乙醇)

已知:①CuCl为白色固体,难溶于水和乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl有水存在时在空气中易被氧化,在酸性条件下较稳定。
(1)“溶解”时选用约为0.5mol•L-1的硫酸,过程中无气体产生。若硫酸浓度过大,反应会产生NO、NO2等有害气体,NH4NO3的用量会
(2)“转化”步骤中发生反应的离子方程式为
(3)氯化铵用量[
 ]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,其原因是
]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,其原因是
(4)检验CuCl沉淀是否洗涤完全的方法是
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:
您最近一年使用:0次
2020-02-27更新
|
147次组卷
|
2卷引用:江苏省苏州市2020届高三上学期期末学业质量阳光指标调研卷化学试题



