名校
1 . 乙研究小组为了利用稀硫酸制备 ,进行了如图所示的实验设计。
,进行了如图所示的实验设计。 能加快生成
能加快生成 的反应速率,发挥作用的原理可表述为:
的反应速率,发挥作用的原理可表述为:
①
②……
(1)反应②的离子方程式 为______________ 。
(2)某小组通过向铜和稀硫酸的混合物中加入过氧化氢的方法制备硫酸铜,但是在实际操作时,发现所消耗的 的量往往会大于理论值,原因是
的量往往会大于理论值,原因是__________ 。
取 晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。
晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。 时,固体的成分为
时,固体的成分为________ (写出计算步骤 )。
(4)当剩余固体为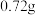 时,加热的温度不能低于
时,加热的温度不能低于_____ ℃,如果此时产生的气体中含有 ,请写出
,请写出 受热分解的化学方程式
受热分解的化学方程式________ 。
 ,进行了如图所示的实验设计。
,进行了如图所示的实验设计。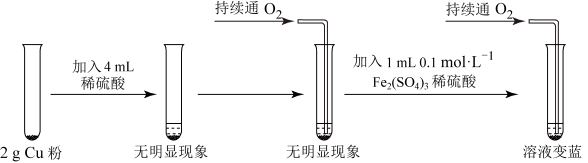
 能加快生成
能加快生成 的反应速率,发挥作用的原理可表述为:
的反应速率,发挥作用的原理可表述为:①

②……
(1)反应②的
(2)某小组通过向铜和稀硫酸的混合物中加入过氧化氢的方法制备硫酸铜,但是在实际操作时,发现所消耗的
 的量往往会大于理论值,原因是
的量往往会大于理论值,原因是取
 晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。
晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。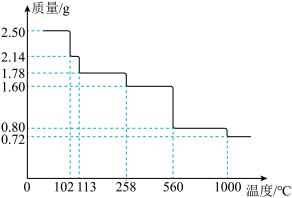
 时,固体的成分为
时,固体的成分为(4)当剩余固体为
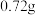 时,加热的温度不能低于
时,加热的温度不能低于 ,请写出
,请写出 受热分解的化学方程式
受热分解的化学方程式
您最近半年使用:0次
名校
2 . 氯化亚铜化学式为CuCl,白色立方结晶或白色粉末,难溶于水,在潮湿的空气中易氧化,不溶于乙醇,常用作催化剂、杀菌剂、媒染剂、脱色剂等。
I.CuCl的制备
取25g CuSO4∙5H2O和6.43gNaCl并加少量水溶解,将溶液倒入如图所示的三颈烧瓶中,加热至50℃,向三颈烧瓶中缓慢滴加Na2SO3和Na2CO3的混合溶液,使其持续反应30min。待反应结束后将混合物静置一段时间,抽滤,沉淀依次用36%的乙酸、无水乙醇、无水乙醚洗涤多次,得白色固体,真空或者充氮气保存。___________ 。
(2)反应时使用NaCl浓溶液,主要目的是___________ 。
(3)三颈烧瓶中CuSO4、NaCl、Na2SO3反应生成CuCl的离子方程式为___________ ;缓慢滴加Na2SO3和Na2CO3的混合溶液的主要原因是___________ 。
(4)沉淀用无水乙醇洗涤的目的是___________ 。
II.CuCl样品纯度的测定
准确称取CuCl样品0.25g,将其置于足量FeCl3溶液中,待固体完全溶解后,加水50mL和邻菲啰啉指示剂2滴,立即用amol∙L-1 Ce(SO4)2标准溶液滴定至绿色出现且30s不褪色,即为终点,重复2~3次,平均消耗Ce(SO4)2标准溶液bmL(已知: ,
, )
)
(5)滴定时应将Ce(SO4)2标准溶液加入___________ (填“酸式滴定管”或“碱式滴定管”)中;该样品中CuCl的质量分数为___________ ×100%。(用含a、b的代数式表示,列出计算式即可)
(6)下列操作可能会导致样品纯度测量结果偏低的是___________。(填标号)
I.CuCl的制备
取25g CuSO4∙5H2O和6.43gNaCl并加少量水溶解,将溶液倒入如图所示的三颈烧瓶中,加热至50℃,向三颈烧瓶中缓慢滴加Na2SO3和Na2CO3的混合溶液,使其持续反应30min。待反应结束后将混合物静置一段时间,抽滤,沉淀依次用36%的乙酸、无水乙醇、无水乙醚洗涤多次,得白色固体,真空或者充氮气保存。

(2)反应时使用NaCl浓溶液,主要目的是
(3)三颈烧瓶中CuSO4、NaCl、Na2SO3反应生成CuCl的离子方程式为
(4)沉淀用无水乙醇洗涤的目的是
II.CuCl样品纯度的测定
准确称取CuCl样品0.25g,将其置于足量FeCl3溶液中,待固体完全溶解后,加水50mL和邻菲啰啉指示剂2滴,立即用amol∙L-1 Ce(SO4)2标准溶液滴定至绿色出现且30s不褪色,即为终点,重复2~3次,平均消耗Ce(SO4)2标准溶液bmL(已知:
 ,
, )
)(5)滴定时应将Ce(SO4)2标准溶液加入
(6)下列操作可能会导致样品纯度测量结果偏低的是___________。(填标号)
| A.样品在空气中放置时间过长 |
| B.盛装Ce(SO4)2标准溶液的滴定管未用标准溶液润洗 |
| C.锥形瓶中装待测液前未干燥 |
| D.滴定管内部滴定前无气泡,滴定后有气泡 |
您最近半年使用:0次
7日内更新
|
256次组卷
|
3卷引用:山西省太原市2024届高三一模理综试卷-高中化学
山西省太原市2024届高三一模理综试卷-高中化学(已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)河南省郑州市宇华实验学校2024届高三下学期第三次模拟考试化学试题
3 . 氯化亚铜(CuCl)微溶于水,难溶于乙醇,易被氧化,广泛应用于医药、有机合成催化剂等工业。以废铜渣(主要含Cu、CuO,还有少量其他难溶物)为原料制备CuCl的工艺流程如图所示。 被还原为
被还原为 ,该过程中发生氧化还原反应的离子方程式为
,该过程中发生氧化还原反应的离子方程式为____________ 。
(2)若“浸出”过程中0.2 mol 参加反应时,转移1 mol电子,则还原产物为
参加反应时,转移1 mol电子,则还原产物为______ (填化学式)。
(3)“还原”过程中逐滴加入 、
、 溶液,初始时生成沉淀反应的离子方程式是
溶液,初始时生成沉淀反应的离子方程式是____________ 。“还原”过程中 溶液加入至过量的原因:一是让
溶液加入至过量的原因:一是让 全部被还原,二是
全部被还原,二是____________ 。
(4)“还原”过程中加入 溶液的体积(V)与溶液pH的关系如图所示。
溶液的体积(V)与溶液pH的关系如图所示。 溶液体积大于一定量时,溶液pH增大的原因是
溶液体积大于一定量时,溶液pH增大的原因是____________ 。
(5)用无水乙醇洗涤CuCl的优点是____________ (填一条)。
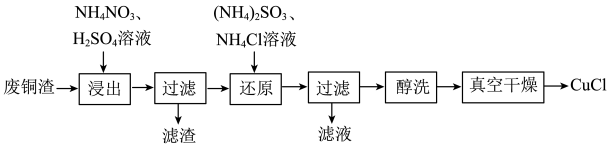
 被还原为
被还原为 ,该过程中发生氧化还原反应的离子方程式为
,该过程中发生氧化还原反应的离子方程式为(2)若“浸出”过程中0.2 mol
 参加反应时,转移1 mol电子,则还原产物为
参加反应时,转移1 mol电子,则还原产物为(3)“还原”过程中逐滴加入
 、
、 溶液,初始时生成沉淀反应的离子方程式是
溶液,初始时生成沉淀反应的离子方程式是 溶液加入至过量的原因:一是让
溶液加入至过量的原因:一是让 全部被还原,二是
全部被还原,二是(4)“还原”过程中加入
 溶液的体积(V)与溶液pH的关系如图所示。
溶液的体积(V)与溶液pH的关系如图所示。
 溶液体积大于一定量时,溶液pH增大的原因是
溶液体积大于一定量时,溶液pH增大的原因是(5)用无水乙醇洗涤CuCl的优点是
您最近半年使用:0次
4 . 氯化亚铜(CuCl)是一种易水解的白色固体。以低品位铜矿砂(主要成分CuS)为原料制备CuCl的工艺流程如图所示。
(1)“酸溶1”时,CuS作_______ (填“氧化剂”或“还原剂”)。
(2)“除锰”时,Cu2+转化为Cu(NH3)4CO3,Mn2+转化为MnCO3沉淀。沉锰的反应化学方程式为_______ 。将生成的MnCO3分离出来的实验操作为_______ 。
(3)“酸溶2”投料后,以一定的速率搅拌反应,可提高铜浸出率的措施有_______ (只答一种方法)。
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生_______ 气体。
(5)“洗涤”应先用稀盐酸洗涤,其目的是_______ 。

(1)“酸溶1”时,CuS作
(2)“除锰”时,Cu2+转化为Cu(NH3)4CO3,Mn2+转化为MnCO3沉淀。沉锰的反应化学方程式为
(3)“酸溶2”投料后,以一定的速率搅拌反应,可提高铜浸出率的措施有
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生
(5)“洗涤”应先用稀盐酸洗涤,其目的是
您最近半年使用:0次
5 . 一水硫酸四氨合铜[Cu(NH3)4SO4·H2O]是一种易溶于水,难溶于乙醇的绛蓝色晶体,可作高效安全的广谱杀菌剂。成外某兴趣小组查阅资料后设计实验方案制备出该晶体并对制备出的晶体进行成分检验和性质探究。
I.制备少量Cu(NH3)4SO4·H2O晶体:___________ (填仪器名称)。___________ 。
(3)步骤Ⅲ的离子方程式为___________ 。
(4)有同学查阅资料得知:(NH4)2SO4也难溶于乙醇。故对于制备出的晶体的成分,该同学提出如下假设:
假设一:只有(NH4)2SO4
假设二:只有Cu(NH3)4SO4·H2O
假设三:(NH4)2SO4和Cu(NH3)4SO4·H2O两种成分都有
已知产物晶体为蓝色,则无需实验即可排除___________ 。(填“假设一”、“假设二”、“假设三”)
Ⅱ.对制备出的晶体的成分进行检验和性质探究
(5)检验该晶体中阴离子的方法:___________ 。
(6)用所得晶体加水得到深蓝色溶液。取三份1L试样,分别加入一定量的水、稀硫酸、热的浓氢氧化钠溶液,实验现象记录如下:
结合化学用语,解释加入稀硫酸后出现的现象的原因___________ 。请补充完整加入热的浓氢氧化钠溶液后的现象:___________ 。
(7)晶体中N含量的测定
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL10%NaOH溶液,通入水蒸气,并用蒸馏水冲洗导管内壁,用V1mLc1mol/L的盐酸标准溶液完全吸收。取下接收瓶,用c2mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗V2mL溶液。___________ ,样品中N的质量分数的表达式为___________ ,最终通过N的质量分数确定了样品的成分。
I.制备少量Cu(NH3)4SO4·H2O晶体:
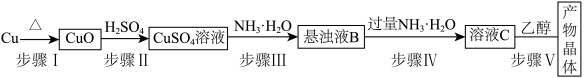
(3)步骤Ⅲ的离子方程式为
(4)有同学查阅资料得知:(NH4)2SO4也难溶于乙醇。故对于制备出的晶体的成分,该同学提出如下假设:
假设一:只有(NH4)2SO4
假设二:只有Cu(NH3)4SO4·H2O
假设三:(NH4)2SO4和Cu(NH3)4SO4·H2O两种成分都有
已知产物晶体为蓝色,则无需实验即可排除
Ⅱ.对制备出的晶体的成分进行检验和性质探究
(5)检验该晶体中阴离子的方法:
(6)用所得晶体加水得到深蓝色溶液。取三份1L试样,分别加入一定量的水、稀硫酸、热的浓氢氧化钠溶液,实验现象记录如下:
| 加入试剂 | 水 | 稀硫酸 | 热的氢氧化钠溶液 |
| 现象 | 深蓝色稍变浅 | 溶液颜色变成浅蓝色且与同浓度硫酸铜颜色相当 | 溶液最终变为无色 |
(7)晶体中N含量的测定
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL10%NaOH溶液,通入水蒸气,并用蒸馏水冲洗导管内壁,用V1mLc1mol/L的盐酸标准溶液完全吸收。取下接收瓶,用c2mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗V2mL溶液。
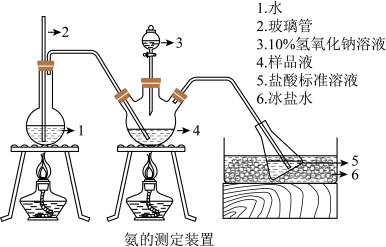
您最近半年使用:0次
6 . 碱式碳酸铜 俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
Ⅰ.配制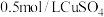 溶液和
溶液和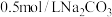 溶液各
溶液各 。
。
Ⅱ.取 所配
所配 溶液,按照
溶液,按照 和
和 的物质的量之比
的物质的量之比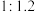 进行混合,在
进行混合,在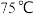 下搅拌反应产生蓝绿色沉淀。
下搅拌反应产生蓝绿色沉淀。
Ⅲ.待沉淀完全后减压过滤,用乙醇淋洗,干燥。
回答下列问题:
(1)步骤Ⅰ中,配制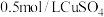 溶液时,不需要使用下列仪器中的
溶液时,不需要使用下列仪器中的___________ (填仪器名称)。___________ ,步骤Ⅲ中检验沉淀是否洗净的操作为___________ 。
(3)步骤Ⅲ中用乙醇淋洗的原因是___________ 。
Ⅳ.碱式碳酸铜纯度的测定:同学们设计了如图装置对制得的 蓝绿色固体进行实验。
蓝绿色固体进行实验。 装置加热前,需要首先打开活塞
装置加热前,需要首先打开活塞 ,用
,用 装置制取适量
装置制取适量 ,然后关闭
,然后关闭 ,点燃
,点燃 处酒精灯。装置A中发生反应的离子程式为
处酒精灯。装置A中发生反应的离子程式为___________ ,C中盛装的试剂应是___________ 。
(5)装置 的作用为
的作用为___________ 。
(6)待固体完全分解后,测得装置E增重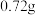 ,则该碱式碳酸铜的纯度为
,则该碱式碳酸铜的纯度为___________  (保留1位小数)。
(保留1位小数)。
 俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:Ⅰ.配制
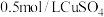 溶液和
溶液和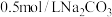 溶液各
溶液各 。
。Ⅱ.取
 所配
所配 溶液,按照
溶液,按照 和
和 的物质的量之比
的物质的量之比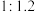 进行混合,在
进行混合,在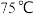 下搅拌反应产生蓝绿色沉淀。
下搅拌反应产生蓝绿色沉淀。Ⅲ.待沉淀完全后减压过滤,用乙醇淋洗,干燥。
回答下列问题:
(1)步骤Ⅰ中,配制
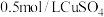 溶液时,不需要使用下列仪器中的
溶液时,不需要使用下列仪器中的
(3)步骤Ⅲ中用乙醇淋洗的原因是
Ⅳ.碱式碳酸铜纯度的测定:同学们设计了如图装置对制得的
 蓝绿色固体进行实验。
蓝绿色固体进行实验。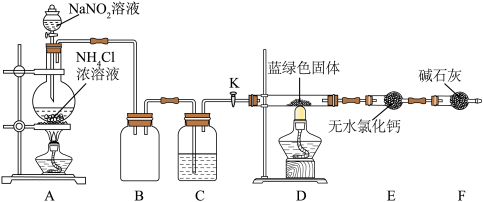
 装置加热前,需要首先打开活塞
装置加热前,需要首先打开活塞 ,用
,用 装置制取适量
装置制取适量 ,然后关闭
,然后关闭 ,点燃
,点燃 处酒精灯。装置A中发生反应的离子程式为
处酒精灯。装置A中发生反应的离子程式为(5)装置
 的作用为
的作用为(6)待固体完全分解后,测得装置E增重
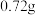 ,则该碱式碳酸铜的纯度为
,则该碱式碳酸铜的纯度为 (保留1位小数)。
(保留1位小数)。
您最近半年使用:0次
名校
7 . 在中华文明的历史长河中,江西人才辈出,文化璀璨,下列说法正确的是
| A.“落木千山天远大,澄江一道月分明”,月亮倒映在江水中的现象属于丁达尔效应 |
B.白鹿洞书院建筑群易受酸雨腐蚀, 的雨水为酸雨 的雨水为酸雨 |
C.“庐山山南刷铜绿”,“铜绿”的主要成分为 |
| D.“白如玉,明如镜,薄如纸,声如馨”的景德镇白瓷的主要成分为无机硅酸盐材料 |
您最近半年使用:0次
解题方法
8 . 广安代市镇火力发电厂需要燃烧大量的煤,产生大量CO2和SO2等,并留下大量煤渣,对环境有较大影响。其中一种不能继续燃烧的煤渣成分俗名叫“铁甲石”,主要成分为:Al2O3(15%~24%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)、FeO(0.9%~2.0%)、CuO(8.5%~11.0%)以及其他不溶性杂质,铁甲石中的氧化铝难溶于酸,可以通过煅烧改变铁甲石结构,使其溶于酸。铁甲石经过下列化工工艺,可以制取无水CuCl2。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
(1)第一次过滤的滤渣为___________ 。
(2)加H2O2后发生反应的离子方程式为___________ 。
(3)调节溶液pH需要控制的范围是___________ ,“调节溶液pH”的过程中除添加试剂,还需借助于___________ 测定溶液pH值。
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
(5)从滤液2中得到无水CuCl2的操作为___________ 。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀pH | 5.8 | 5.8 | 2.0 | 4.0 |
| 沉淀完成pH | 7.5 | 8.3 | 3.1 | 5.4 |
(1)第一次过滤的滤渣为
(2)加H2O2后发生反应的离子方程式为
(3)调节溶液pH需要控制的范围是
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
| A.氢氧化钠 | B.氨水 | C.CuO | D.AlCl3 |
(5)从滤液2中得到无水CuCl2的操作为
您最近半年使用:0次
9 . 第四周期过渡元素形成的化合物具有重要作用。黄铜( )用
)用 溶液浸泡后生成单质硫,所得
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米
溶液可用于制取纳米 ,
, 能与酸发生反应。
能与酸发生反应。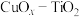 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: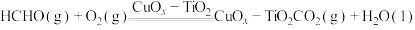 。
。 具有强氧化性,可与盐酸反应生成氯气。由
具有强氧化性,可与盐酸反应生成氯气。由 、
、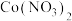 、
、 和
和 反应制备的配合物
反应制备的配合物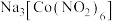 可应用于
可应用于 的鉴定。
的鉴定。
下列化学反应表示正确的是
 )用
)用 溶液浸泡后生成单质硫,所得
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米
溶液可用于制取纳米 ,
, 能与酸发生反应。
能与酸发生反应。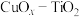 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: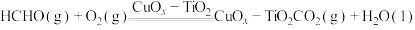 。
。 具有强氧化性,可与盐酸反应生成氯气。由
具有强氧化性,可与盐酸反应生成氯气。由 、
、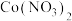 、
、 和
和 反应制备的配合物
反应制备的配合物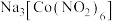 可应用于
可应用于 的鉴定。
的鉴定。下列化学反应表示正确的是
A. 与稀硫酸反应: 与稀硫酸反应: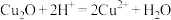 |
B. 溶液和 溶液和 反应: 反应: |
C. 与足量盐酸反应: 与足量盐酸反应: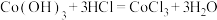 |
D.制备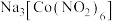 的反应: 的反应: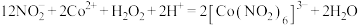 |
您最近半年使用:0次
名校
10 . 氯化亚铜(CuCl)是石油工业常用的脱硫剂和脱色剂,以低品位铜矿(主要成分为 和铁的氧化物)为原料制备CuCl流程如图。
和铁的氧化物)为原料制备CuCl流程如图。
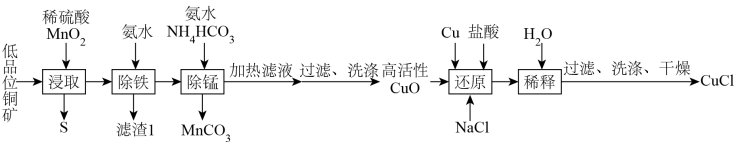
已知:CuCl难溶于醇和水,热水中能被氧化,CuCl易溶于浓度较大的 体系中(
体系中(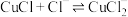 )。
)。
下列说法错误的是
 和铁的氧化物)为原料制备CuCl流程如图。
和铁的氧化物)为原料制备CuCl流程如图。
已知:CuCl难溶于醇和水,热水中能被氧化,CuCl易溶于浓度较大的
 体系中(
体系中(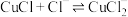 )。
)。下列说法错误的是
| A.“浸取”过程中可用浓硫酸代替稀硫酸 |
B.“除锰”过程中发生离子反应为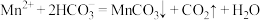 |
C.“还原”后所得产物主要为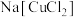 |
| D.产品CuCl可用冷的乙醇洗涤 |
您最近半年使用:0次



