名校
解题方法
1 . 我国正在推行垃圾分类,为研究废旧电池的再利用,实验室利用旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验流程如图所示。下列说法错误的是
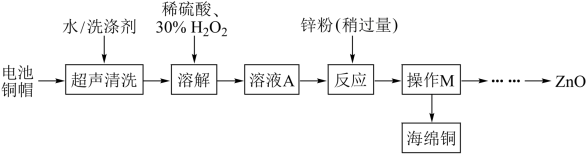

| A.“溶解”过程中,加入H2O2发生的反应方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O |
| B.溶液A中一定含有的溶质有ZnSO4和CuSO4 |
| C.操作M中用到的玻璃仪器有烧杯、漏斗和玻璃棒 |
| D.通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作,可得到ZnO |
您最近一年使用:0次
2021-05-12更新
|
655次组卷
|
10卷引用:考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)湖北省鄂东南省级示范高中教育教学改革联盟学校2021届高三5月联考化学试题(已下线)2021年高考化学押题预测卷(广东卷)(03)(已下线)课时19 金属元素为载体的化工流程选择题-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)基础卷05-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)湖北省襄阳市第一中学2021-2022学年高一下学期3月月考化学试题(已下线)必刷卷04-2022年高考化学考前信息必刷卷(山东专用)(已下线)选择题6-10
2 . 三星堆两次考古挖掘举世震惊,二号祭祀坑出土商代的铜人铜像填补了我国考古学、青铜文化、青铜艺术史上的诸多空白。下列有关说法错误的是


A.铜像表面的铜绿[ ]能在空气中稳定存在 ]能在空气中稳定存在 |
B.测定出土文物年代的 是碳的一种同素异形体 是碳的一种同素异形体 |
| C.X射线衍射法可对青铜器微观晶体结构进行分析 |
| D.青铜器的出土表明我国商代已经掌握冶炼铜技术 |
您最近一年使用:0次
2021-05-11更新
|
798次组卷
|
7卷引用:考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)山东省青岛市2021届高三二模化学试题(已下线)第10讲 金属材料及金属矿物的开发利用(精练)-2022年高考化学一轮复习讲练测(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)专题01 STSE 化学用语-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)考点16 铜及其金属材料-备战2023年高考化学一轮复习考点帮(全国通用)江苏省常州市十校2022-2023学年高三上学期12月联合调研化学试题
名校
3 . 根据物质的组成、结构等信息可以预测其性质或用途。下列预测中,明显不合理 的是
A.根据化合价预测,高铜酸钠(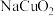 )与 )与 可生成硫酸盐 可生成硫酸盐 |
B.根据组成预测,铝酸三钙(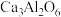 )溶于足量盐酸,生成白色沉淀 )溶于足量盐酸,生成白色沉淀 |
| C.根据在周期表中位置预测,单质砷(第ⅤA族)是重要的半导体材料 |
D.根据结构预测,葡萄糖[ ]溶液中加入新制氢氧化铜,溶液呈绛蓝色 ]溶液中加入新制氢氧化铜,溶液呈绛蓝色 |
您最近一年使用:0次
2021-05-10更新
|
524次组卷
|
3卷引用:浙江省金华十校2021届高三4月模拟考试化学试题
浙江省金华十校2021届高三4月模拟考试化学试题(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(精练)-2022年高考化学一轮复习讲练测浙江省杭州学军中学2021-2022学年高三上学期12月适应性考试化学试题
名校
解题方法
4 . 某含结晶水的盐A是制备负载型活性铁催化剂的主要原料,由五种常见元素组成,M(A)<500 g·mol−1。某兴趣小组对盐A进行了实验探究,流程如下:
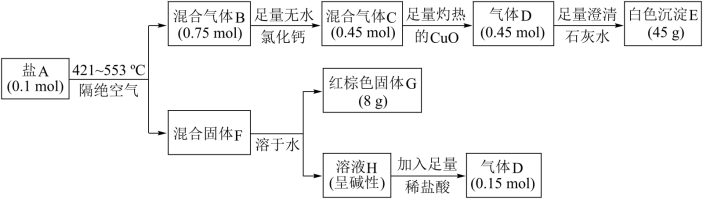
已知:①混合气体C转化为气体D时,质量增加了4.8 g;②溶液H为单一溶质,且不与氢氧化钾反应,焰色反应呈紫色。请回答:
(1)盐A除Fe、H、O以外的两种元素是_____ 。(填元素符号)
(2)混合气体C的组成成分_____ (填化学式)
(3)盐A在421~553℃下分解生成混合气体B和混合固体F的化学方程式:_____ 。
(4)盐A中加入足量稀硫酸,可得到一种二元弱酸,且该弱酸可以被酸性高锰酸钾溶液氧化生成气体D,试写出该弱酸被氧化的离子方程式:_______ 。
(5)某兴趣小组用混合气体C还原少量CuO粉末,使CuO完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:_______ 。(已知:Cu2O+2H+=Cu2++Cu+H2O)

已知:①混合气体C转化为气体D时,质量增加了4.8 g;②溶液H为单一溶质,且不与氢氧化钾反应,焰色反应呈紫色。请回答:
(1)盐A除Fe、H、O以外的两种元素是
(2)混合气体C的组成成分
(3)盐A在421~553℃下分解生成混合气体B和混合固体F的化学方程式:
(4)盐A中加入足量稀硫酸,可得到一种二元弱酸,且该弱酸可以被酸性高锰酸钾溶液氧化生成气体D,试写出该弱酸被氧化的离子方程式:
(5)某兴趣小组用混合气体C还原少量CuO粉末,使CuO完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
您最近一年使用:0次
2021-05-08更新
|
324次组卷
|
3卷引用:浙江省温州市2021届普通高中高考5月适应性测试(三模)化学试题
浙江省温州市2021届普通高中高考5月适应性测试(三模)化学试题(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)江西省景德镇市第一中学2021-2022学年高一上学期期中18班化学试题
名校
5 . 氯化亚铜(CuCl)可用作有机合成的催化剂,CuCl微溶于水,不溶于醇和稀酸,可溶于Cl-浓度较大的溶液(CuCl+Cl- CuCl
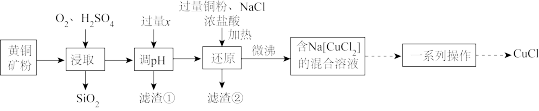
CuCl ),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2,还含有少量的SiO2)制备CuCl的工艺流程如图:
),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2,还含有少量的SiO2)制备CuCl的工艺流程如图:
25℃时,相关物质的Ksp见表。
回答下列问题:
(1)黄铜矿预先粉碎的目的是_______ 。
(2)调pH加入的过量x为_______ (填化学式),滤渣①的成分_______ (填化学式)。
(3)“还原”时,铜粉转化为Na[CuCl2]的离子反应方程式为_______ 。
(4)已知:温度、pH对CuCl产率的影响如图1、图2所示。则析出CuCl晶体的最佳条件为_______ 。
A.温度在60℃左右pH为2.0~2.5 B.温度在90℃左右pH为2.0~2.5
C.温度在60℃左右pH为5.0~6.0 D.温度在90℃左右pH为5.0~6.0
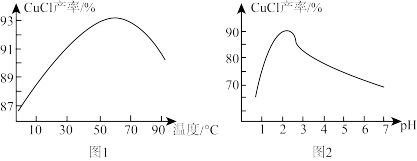
(5)析出的氯化亚铜晶体要立即用无水乙醇洗涤,“醇洗”可快速除去滤渣表面的水,防止滤渣被空气氧化为碱式氯化铜[Cu2(OH)3Cl]。写出氯化亚铜被氧化为碱式氯化铜的化学反应方程式_______ 。
(6)粗产品中氯化亚铜含量的测定:
①称取样品3.0 g于锥形瓶中,再加入过量的FeCl3溶液充分溶解,配制250 mL溶液。②从中取出25.00mL溶液,用0.1000 mol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+。
三次平行实验,到达滴定终点时,消耗硫酸铈标准溶液的体积分别为26.05 mL、24.05 mL、23.95 mL。则样品中CuCl的纯度为_______ (结果保留三位有效数字)。
 CuCl
CuCl ),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2,还含有少量的SiO2)制备CuCl的工艺流程如图:
),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2,还含有少量的SiO2)制备CuCl的工艺流程如图:
25℃时,相关物质的Ksp见表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | CuCl |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-19.7 | 1×10-5.9 |
(1)黄铜矿预先粉碎的目的是
(2)调pH加入的过量x为
(3)“还原”时,铜粉转化为Na[CuCl2]的离子反应方程式为
(4)已知:温度、pH对CuCl产率的影响如图1、图2所示。则析出CuCl晶体的最佳条件为
A.温度在60℃左右pH为2.0~2.5 B.温度在90℃左右pH为2.0~2.5
C.温度在60℃左右pH为5.0~6.0 D.温度在90℃左右pH为5.0~6.0
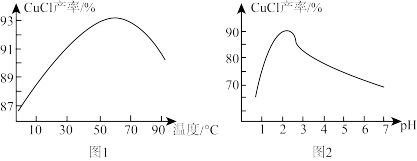
(5)析出的氯化亚铜晶体要立即用无水乙醇洗涤,“醇洗”可快速除去滤渣表面的水,防止滤渣被空气氧化为碱式氯化铜[Cu2(OH)3Cl]。写出氯化亚铜被氧化为碱式氯化铜的化学反应方程式
(6)粗产品中氯化亚铜含量的测定:
①称取样品3.0 g于锥形瓶中,再加入过量的FeCl3溶液充分溶解,配制250 mL溶液。②从中取出25.00mL溶液,用0.1000 mol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+。
三次平行实验,到达滴定终点时,消耗硫酸铈标准溶液的体积分别为26.05 mL、24.05 mL、23.95 mL。则样品中CuCl的纯度为
您最近一年使用:0次
2021-05-08更新
|
696次组卷
|
7卷引用:考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省大庆市2021届高三下学期(4月)第二次教学质量监测(二模)化学试题江西省南昌市八一中学2021届高三第三次模拟考试理科综合化学试题宁夏石嘴山市第三中学2021届高三第四次模拟考试化学试题(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点16 铜及其金属材料-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点16 铜及其金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
6 . 下列物质的名称与化学式不对应的是
| A.纯碱:Na2CO3 | B.钡餐:BaCO3 |
| C.铁红:Fe2O3 | D.胆矾:CuSO4·5H2O |
您最近一年使用:0次
7 . 下列说法正确的是
| A.硅胶具有吸水性,可用作食品的抗氧剂 |
| B.氯气有毒,不能用于药物的合成 |
| C.纯碱具有碱性,可用于治疗胃酸过多 |
| D.铜盐能杀死某些细菌,游泳池中常用硫酸铜作消毒剂 |
您最近一年使用:0次
解题方法
8 . (1)为探究黑色固体X(仅含两种元素)的组成和性质,设计并完成如下实验:
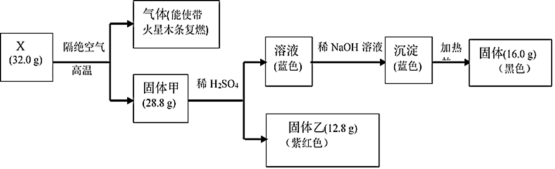
①X的化学式是___________ 。
②固体甲与稀硫酸反应的离子方程式是___________ 。
③热的氨气被固体X氧化成一种气体单质,该反应方程式___________ 。
(2)FeSO4受热分解的化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑。
Fe2O3+SO2↑+SO3↑。
①将FeSO4受热产生的气体按图示装置进行实验,证实含有SO2和SO3,能说明SO2存在的实验现象是:___________ ;

②为测定BaSO4沉淀的质量,后续的操作步骤依次为___________ 、洗涤、干燥、称量。
③试剂一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应):___________ 。

①X的化学式是
②固体甲与稀硫酸反应的离子方程式是
③热的氨气被固体X氧化成一种气体单质,该反应方程式
(2)FeSO4受热分解的化学方程式为:2FeSO4
 Fe2O3+SO2↑+SO3↑。
Fe2O3+SO2↑+SO3↑。①将FeSO4受热产生的气体按图示装置进行实验,证实含有SO2和SO3,能说明SO2存在的实验现象是:

②为测定BaSO4沉淀的质量,后续的操作步骤依次为
③试剂一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应):
您最近一年使用:0次
解题方法
9 . 下列矿物与其主要成分对应不当的是
A.铝土矿: | B.赤铁矿: | C.黄铜矿: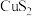 | D.水晶; |
您最近一年使用:0次
2021-04-10更新
|
376次组卷
|
2卷引用:浙江省杭州市2021届高三4月教学质量检测(二模)化学试题
20-21高一下·浙江·开学考试
解题方法
10 . 将CuO和Fe2O3的混合物ag分成两等份,向其中一份混合物中加入2mol/L的硫酸溶液50mL,恰好将固体完全溶解。将另一份混合物在过量的CO气流中加热并充分反应,冷却后得到剩余固体质量为bg。求;
(1)硫酸溶液中的 的物质的量为
的物质的量为_______ mol。
(2)b=_______ g(用a表示)。
(1)硫酸溶液中的
 的物质的量为
的物质的量为(2)b=
您最近一年使用:0次



