名校
解题方法
1 . 下列变化不能通过一步化学反应实现的是( )
| A.BaCl2→BaSO4 | B.CuO→Cu(OH)2 | C.NaOH→Na2SO3 | D.MgSO4→Mg(OH)2 |
您最近一年使用:0次
2020-09-10更新
|
2535次组卷
|
31卷引用:第2讲 物质的转化-【暑假自学课】2023年新高一暑假精品课(苏教版2019必修第一册)
(已下线)第2讲 物质的转化-【暑假自学课】2023年新高一暑假精品课(苏教版2019必修第一册)广东省梅州市大埔县虎山中学2023-2024学年高一上学期11月期中化学试题辽宁省阜新市海州高级中学2019-2020学年高一10月月考化学试题2020年春季苏教版高中化学必修1专题一《化学家眼中的物质世界》测试卷云南省昭通市巧家县第四中学2019-2020学年高一上学期期末考试化学试题江苏省启东中学2020-2021学年高一上学期期初考试化学试题人教版(2019)高一必修第一册第一章 物质及其变化 第一节 物质的分类及转化课时2 物质的转化(已下线)1.1.2 物质的转化(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)高一必修第一册(苏教2019版)专题1 第一单元 物质及其反应的分类(已下线)【浙江新东方】hzomo化学001云南省昆明师范专科学校附属中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高一上】【期中】【hd-lp414】【化学】新疆维吾尔族自治区哈密市第十五中学2020-2021学年高一上学期期末考试化学试题辽宁省庄河市高级中学2021-2022学年高一10月月考化学试题山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题福建省南安市侨光中学2021-2022学年高一上学期第一次阶段考化学试题甘肃省甘南舟曲县第一中学2021-2022学年高一上学期第一次月考化学试卷黑龙江省海林市朝鲜族中学2020-2021学年高一上学期第一次月考化学试题(已下线)衔接点05 物质间的相互转化-2022年初升高化学无忧衔接青海省西宁市湟中区多巴高级中学2021-2022学年高一下学期第一次月考化学试题江苏省淮安市涟水县第一中学2022-2023学年高一上学期第二次阶段检测化学试题河南省许昌市鄢陵县职业教育中心2021—2022学年高一上学期升学班第一次月考化学试题广西梧州市藤县第七中学2021-2022学年高一10月月考化学试题黑龙江省佳木斯市第八中学2021-2022学年高一上学期期中考试化学试题吉林省舒兰市第十八中学校2022-2023学年高一上学期期中考试化学试题贵州省桐梓县育才中学2019-2020学年高二上学期开学考试化学试题广西岑溪市2020-2021学年高二上学期期中考试化学(理)试题新疆维吾尔自治区疏勒县2022 届高三第一次调研测试化学试题(已下线)专题05元素及其化合物-2022年高考真题+模拟题汇编(全国卷)(已下线)专题05元素及其化合物-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题05元素及其化合物-五年(2018~2022)高考真题汇编(全国卷)
9-10高二下·广东湛江·期中
名校
解题方法
2 . 下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是
①金属钠在纯氧中燃烧
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用酒精中
①金属钠在纯氧中燃烧
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用酒精中
| A.②③①④ | B.③②①④ | C.③①②④ | D.①②③④ |
您最近一年使用:0次
2022-01-13更新
|
1300次组卷
|
83卷引用:2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(四)
2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(四)2023年广东省普通高中学业水平合格性考试化学科模拟仿真卷(一)天津市新华中学2022-2023学年高一上学期期末考试化学试题 云南省玉溪第一中学2022-2023学年高一下学期期中考试化学试题(已下线)专题九 铁及其化合物(已下线)合格考真题汇编8金属元素及其化合物二天津北京师范大学静海附属学校2023-2024学年高一上学期第三次月考化学试题(已下线)2010年湖南省浏阳一中高一上学期第三次阶段性测试化学卷(已下线)2010—2011学年湖北省沙市中学高一上学期期末考试化学试卷(已下线)2011-2012学年黑龙江省庆安三中高一上学期期末考试化学试卷(已下线)2012-2013学年山东省济宁市汶上一中高一3月质量检测化学试卷(已下线)2012-2013学年广东省佛山市佛山一中高一下学期期中考试化学试卷(已下线)2012-2013学年广东省佛山市佛山一中高一下学期期中考试化学试卷(已下线)2013-2014学年江苏省宿迁市高一上学期第二次月考化学试卷2014-2015黑龙江省哈尔滨六中高一12月月考化学试卷2014-2015湖南省浏阳一中等三校高一12月联考化学试卷2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷14-15内蒙古北方重工业集团三中高一上学期期末化学试卷2014-2015广东省深圳市南山区上学期高一化学期末试卷陕西省咸阳市西藏民族学院附属中学2015-2016学年高一上期末化学卷2015-2016学年广东省肇庆市高一上学期期末考试化学试卷2015-2016学年甘肃省甘谷一中高一上期末化学试卷2016-2017学年河南省南阳一中高一上月考二化学卷2016-2017学年河南省南阳一中高一月考二化学卷2016-2017学年江西省南昌市第二中学高一上学期期末考试化学试卷2016-2017学年黑龙江省鸡西市第十九中学高一上学期期末考试化学试卷青海省西宁市第四高级中学2017-2018学年高一上学期第二次月考化学试题1湖北省荆州中学2017-2018学年高一12月月考化学试题湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题湖北省宜昌市葛洲坝中学2017-2018学年高一12月月考化学试题湖北省宜昌市长阳县第一高级中学2017-2018学年高一12月月考化学试题安徽省淮南市第二中学2017-2018学年高一上学期第二次月考化学试题新疆昌吉市2017-2018学年高一上学期期末考试化学试题天津市红桥区2017-2018学年高一上学期期末考试化学试题宁夏银川一中2017-2018学年高一上学期期末考试化学试题湖北省宜昌市示范高中协作体2017-2018学年高一上学期期末化学试题湖南省师范大学附属中学2017-2018学年高一上学期期末考试化学试题黑龙江省伊春中学2017-2018学年高一化学上学期期末考试题【全国百强校】青海省平安县第一高级中学2017-2018学年高一下学期期中考试(A卷)化学试题人教版2017-2018学年高一化学必修1:3.2 几种重要的金属化合物 同步测试2河南省封丘县一中2018-2019学年高一上学期12月月考化学试题河南省信阳市第六高级中学2018-2019学年高一上学期第三次(1月)月考化学试题山西省晋中市平遥县第二中学2018-2019学年高一上学期12月月考化学试题陕西省黄陵中学2018-2019学年高一(普通班)上学期期末考试化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高一上学期期末考试化学试题新疆石河子第二中学2018-2019学年高一上学期期末考试化学试题江西省赣州市会昌中学2019-2020学年高一上学期第二次月考化学试题河北省安平中学2019-2020学年高一上学期第四次月考化学试题山西省晋中市平遥县第二中学2019-2020学年高一12月月考化学试题北京市昌平区新学道临川学校2019-2020学年高一上学期期末考试化学试题福建省泉州第五中学苏教版高中化学必修1专题3 单元综合练习云南省大理市下关第一中学2019-2020学年高一上学期期末考试化学试题安徽省六安市第一中学2019-2020学年高一下学期疫情防控延期开学期间辅导测试(二)化学试题江西省上饶市2019-2020学年高一上学期期末考试 化学(自招班)试题天津市西青区2019-2020学年高一上学期期末考试化学试题陕西省咸阳市实验中学2019-2020学年高一上学期第三次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第六次综合测试化学试题人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物黑龙江省鸡东县第二中学2020-2021学年高一上学期中考试化学试卷宁夏石嘴山市平罗中学2020-2021学年高一上学期第三次月考化学试题天津市东丽区2020-2021学年高一上学期期末考试化学试题吉林省长春市第二十中学2020-2021学年高一上学期第三次考试化学试题广西南宁市英华学校2020-2021学年高一上学期期末考试化学试题(已下线)专题3.1.3 铁盐与亚铁盐(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)吉林省长春市农安县2021-2022学年高一上学期期末考试化学试题新疆哈密市第八中学2021-2022学年高一上学期期末考试化学试题陕西省西安市阎良区关山中学2021-2022学年高一上学期第三次质量检测化学(理科)试题安徽省宿州市北方中学2021-2022学年高一上学期期末测试化学试题云南省大理白族自治州实验中学2020-2021学年高一上学期12月月考化学试题(已下线)2010年广东省湛江二中高二第二学期期中考试化学(文)试题(已下线)2012-2013学年山西省晋中市昔阳中学高二下学期期末考试化学试卷(已下线)2012-2013学年辽宁省铁岭市六校第一次联合考试化学试卷(已下线)2015届甘肃省天水市秦安县二中高三上学期期中考试化学试卷2015-2016学年黑龙江省绥棱一中高二6月月考化学试卷2017届辽宁省铁岭市高三上学期第一次联考化学试卷辽宁省大石桥市第二高级中学2016-2017学年高二学业水平模拟测试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(文)上学期10月月考化学试题内蒙古开来中学2018-2019学年高二下学期期末考试化学试题辽宁省实验中学东戴河分校2020届高三上学期期初摸底考试化学试题黑龙江省佳木斯市汤原高级中学2018-2019学年高二下学期期末考试化学试题四川省南充市阆中中学2020届高三化学选择题专项训练(15)(已下线)专题3.2 铁及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》河南省洛阳市第一高级中学2021届高三上学期10月月考化学试题
3 . 某无色混合气体,可能含有CO、H2、SO2、Cl2、HCl中的一种或几种,把此混合气体通过少量澄清石灰水,无沉淀生成;再通过少量品红溶液,完全褪色;随后将该气体通过足量的氢氧化钠溶液后,再通过足量红热的CuO粉末,粉末变成红色;最后通入CaCl2溶液中,无沉淀生成,则下列关于此混合气体的叙述正确的是
| A.澄清石灰水中无沉淀,说明一定不含有SO2 |
| B.品红褪色,可能是Cl2导致的 |
| C.氧化铜粉末变红,说明CO和H2中至少有一种 |
| D.CaCl2溶液中无沉淀,说明通过CuO后得到的气体中一定不含有CO2 |
您最近一年使用:0次
2017-05-05更新
|
5389次组卷
|
12卷引用:上海市复旦大学附属中学2022-2023学年高一下学期阶段测试化学试题
上海市复旦大学附属中学2022-2023学年高一下学期阶段测试化学试题上海市复旦大学附中浦东分校2016-2017学年高一下学期期中考试化学试题【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题安徽省合肥市第六中学2019-2020学年高一下学期开学考试化学试题高一必修第一册(苏教2019) 模块综合测评安徽省灵璧县第一中学2020-2021学年高一上学期12月月考试题广东省大联考2021-2022学年高一下学期期中检测化学试题黑龙江省哈尔滨市德强学校2021-2022学年高一下学期期中考试化学试题辽宁省沈阳市第一二〇中学2023-2024学年高三上学期第一次质量检测化学试题山西省实验中学2021届高三9月月考化学试题山东省济宁市嘉祥县第一中学2021-2022学年高三上学期期中考试化学试题山西省实验中学2020-2021学年高三上学期第一次月考化学试题
4 . 某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2。利用该固体废渣制取Cu(NO3)2溶液的工艺流程如图所示:
②SiO2是酸性氧化物,难于水和酸。
(1)写出Cu2O与稀硝酸反应的离子反应方程式为___________ ;
(2)酸溶时,反应温度不宜超过70℃,其主要原因是___________ ;
(3)将酸溶步骤排放的NO循环利用既环保又能提高产量,具体操作流程是___________ ;
(4)酸溶试剂改用绿色氧化剂(10%H2O2和20%稀硝酸的混合液),基本无氮氧化物排放,写出废渣中Cu与绿色氧化剂反应的离子反应方程式___________ ;
(5)中和试剂选择Cu(OH)2,若改为NaOH,缺点是___________ ;
(6)以某工业废水(主要含Cu2+、Na+、SO )为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入
)为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入___________ ,洗涤,干燥。(须使用的试剂有:蒸馏水、1mol/L NaOH溶液、1mol/LHNO3溶液;Cu(NO3)2的溶解度曲线如图所示。)
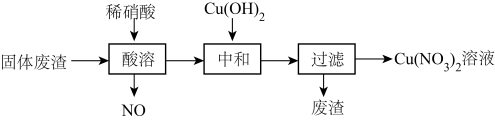
②SiO2是酸性氧化物,难于水和酸。
(1)写出Cu2O与稀硝酸反应的离子反应方程式为
(2)酸溶时,反应温度不宜超过70℃,其主要原因是
(3)将酸溶步骤排放的NO循环利用既环保又能提高产量,具体操作流程是
(4)酸溶试剂改用绿色氧化剂(10%H2O2和20%稀硝酸的混合液),基本无氮氧化物排放,写出废渣中Cu与绿色氧化剂反应的离子反应方程式
(5)中和试剂选择Cu(OH)2,若改为NaOH,缺点是
(6)以某工业废水(主要含Cu2+、Na+、SO
 )为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入
)为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入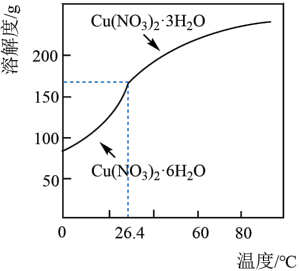
您最近一年使用:0次
2023-10-04更新
|
506次组卷
|
2卷引用:江苏省扬州中学2022-2023学年高一下学期3月月考化学试题
解题方法
5 . 写出下列物质之间转化的化学方程式。
(1)Cu→CuO→CuSO4→Cu(OH)2→CuSO4→Cu。___ 。
(2)C→CO2→CaCO3→CaO→Ca(OH)2→CaCl2。___ 。
(1)Cu→CuO→CuSO4→Cu(OH)2→CuSO4→Cu。
(2)C→CO2→CaCO3→CaO→Ca(OH)2→CaCl2。
您最近一年使用:0次
2021-12-01更新
|
1691次组卷
|
3卷引用:【定心卷】1.1.2 物质的转化随堂练习-人教版2023-2024学年必修第一册
【定心卷】1.1.2 物质的转化随堂练习-人教版2023-2024学年必修第一册人教2019版必修第一册第一章第一节 物质的分类及转化课后习题(已下线)1.1.3 物质性质与变化(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)
解题方法
6 . 实验室制取NO和 固体,下列装置能达到实验目的的是
固体,下列装置能达到实验目的的是
 固体,下列装置能达到实验目的的是
固体,下列装置能达到实验目的的是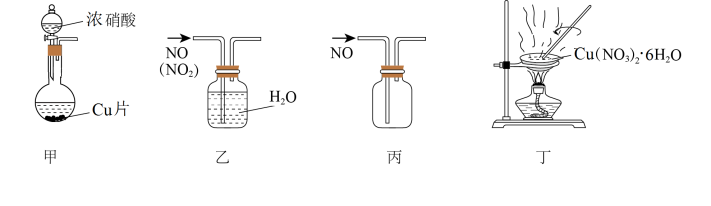
| A.用装置甲制取NO气体 | B.用装置乙除去NO中少量的 |
| C.用装置丙收集NO气体 | D.用装置丁灼烧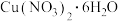 得到 得到 |
您最近一年使用:0次
7 . 草酸亚铁晶体(FeC2O4∙2H2O)是一种淡黄色粉末,某课外小组利用下列装置检验草酸亚铁晶体受热分解的部分产物。
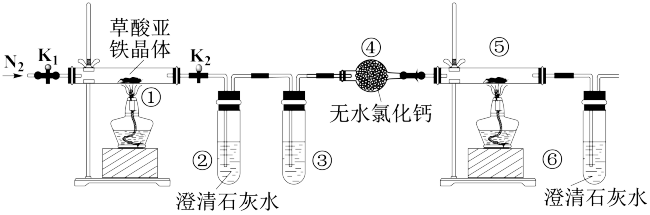
下列说法正确的是

下列说法正确的是
| A.③中盛放足量的饱和NaHCO3溶液用于除去生成的CO2 |
| B.加热前需要先向装置中通一段时间的N2 |
| C.若将④中的无水CaCl2换成无水硫酸铜可检验分解生成的水蒸气 |
| D.实验结束后,若①中淡黄色粉末完全变成黑色,则产物一定为铁 |
您最近一年使用:0次
2021-12-17更新
|
1672次组卷
|
5卷引用:云南省昆明市第八中学2023-2024学年高一上学期12月月考化学试题
云南省昆明市第八中学2023-2024学年高一上学期12月月考化学试题湖南省长沙市雅礼中学2021 -2022学年上学期高一12月月考化学试题(已下线)第三章 铁 金属材料(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)第一节 铁及其化合物 第1课时 铁的单质和氧化物、氢氧化物(已下线)高中化学-高一上-13
22-23高一上·全国·课后作业
解题方法
8 . 将少量Na分别投入下列物质的水溶液中,有气体放出且溶液质量减轻的是
| A.CuSO4 | B.NaOH | C.K2SO4 | D.HCl |
您最近一年使用:0次
名校
9 . 下列除杂方法正确的是
| 选项 | 物质(杂质) | 除杂方法 |
| A | 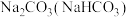 | 加热至恒重 |
| B |  | 加入足量稀盐酸,过滤 |
| C | 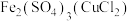 | 加入足量铁粉,过滤 |
| D | 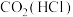 | 用饱和 溶液洗气 溶液洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-01更新
|
481次组卷
|
3卷引用:河北省邢台市质检联盟2023-2024学年高一上学期11月月考化学试题
名校
解题方法
10 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备ZnSO4·7H2O和CuSO4·5H2O的部分实验步骤如下:
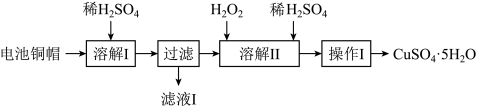
下列说法正确的是

下列说法正确的是
| A.滤液I中存在的主要阳离子有Zn2+、H+、Cu2+ |
| B.操作I为了尽可能多的得到CuSO4·5H2O晶体,应该将溶液蒸干 |
| C.溶解II过程发生反应的离子方程式为:Cu + H2O2 + 2H+ = Cu2+ + 2H2O |
| D.不可用操作I的方法从滤液I中提取ZnSO4·7H2O |
您最近一年使用:0次



