名校
解题方法
1 . 甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用 或
或 来生产燃料甲醇。
来生产燃料甲醇。
(1)已知:
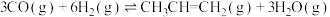
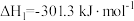

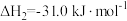
则 与
与 合成气态甲醇的热化学方程式为
合成气态甲醇的热化学方程式为___________ 。
(2)制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
①反应的平衡常数
___________ (用 、
、 表示),500℃时
表示),500℃时
___________ 。
②500℃时,测得反应III在某时刻 、
、 、
、 、
、 的浓度(
的浓度( )分别为0.8、0.1、0.3、0.15,则此时
)分别为0.8、0.1、0.3、0.15,则此时
___________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
③500℃时,2L密闭容器中投入amol 、bmol
、bmol 发生反应I,测得平街时
发生反应I,测得平街时 、
、 的浓度(
的浓度( )分别为0.2、0.1则:
)分别为0.2、0.1则:
___________ ,平衡时 的转化率为
的转化率为___________ 。若向平衡后的容器中再投入anol 、bmol
、bmol ,达平衡后,
,达平衡后, 的体积分数与原平衡相比
的体积分数与原平衡相比___________ (填“增大”、“减小”或“不变”)
(3)某科研小组在500℃、 作催化剂的条件下依据反应I合成甲醇,研究了
作催化剂的条件下依据反应I合成甲醇,研究了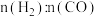 分别为
分别为 、
、 时
时 的转化率变化情况,如图所示:
的转化率变化情况,如图所示:
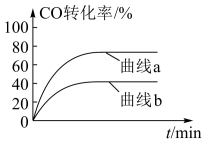
则图中表示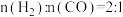 的变化曲线为
的变化曲线为___________ (填“曲线a”或“曲线b”),原因是___________ 。
 或
或 来生产燃料甲醇。
来生产燃料甲醇。(1)已知:
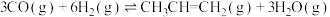
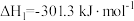

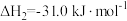
则
 与
与 合成气态甲醇的热化学方程式为
合成气态甲醇的热化学方程式为(2)制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
| 化学反应 | 平衡常数 | 温度/℃ | |
| 500 | 800 | ||
I. |  | 2.5 | 0.15 |
II. |  | 1.0 | 2.50 |
III.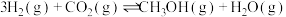 |  | ||

 、
、 表示),500℃时
表示),500℃时
②500℃时,测得反应III在某时刻
 、
、 、
、 、
、 的浓度(
的浓度( )分别为0.8、0.1、0.3、0.15,则此时
)分别为0.8、0.1、0.3、0.15,则此时
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。③500℃时,2L密闭容器中投入amol
 、bmol
、bmol 发生反应I,测得平街时
发生反应I,测得平街时 、
、 的浓度(
的浓度( )分别为0.2、0.1则:
)分别为0.2、0.1则:
 的转化率为
的转化率为 、bmol
、bmol ,达平衡后,
,达平衡后, 的体积分数与原平衡相比
的体积分数与原平衡相比(3)某科研小组在500℃、
 作催化剂的条件下依据反应I合成甲醇,研究了
作催化剂的条件下依据反应I合成甲醇,研究了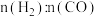 分别为
分别为 、
、 时
时 的转化率变化情况,如图所示:
的转化率变化情况,如图所示:
则图中表示
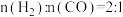 的变化曲线为
的变化曲线为
您最近一年使用:0次
名校
解题方法
2 . 用甲醇(CH3OH)制备一些高附加值产品,是目前研究的热点。
(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ. CH3OH(g)+H2O(g) 3H2(g)+CO2(g) △H1
3H2(g)+CO2(g) △H1
反应Ⅱ. H2(g)+CO2(g) H2O(g)+CO(g) △H2= a kJ·mol-1
H2O(g)+CO(g) △H2= a kJ·mol-1
反应Ⅲ. CH3OH(g) 2H2(g)+CO(g) △H3= b kJ·mol-1
2H2(g)+CO(g) △H3= b kJ·mol-1
反应Ⅳ. 2CH3OH(g) 2H2O(g)+C2H4(g) △H4= c kJ·mol-1
2H2O(g)+C2H4(g) △H4= c kJ·mol-1
①△H1=______ kJ·mol-1 。
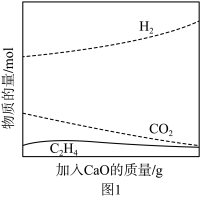
②工业上采用CaO吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图1,请分析加入CaO提高氢气产率的原因:______ 。
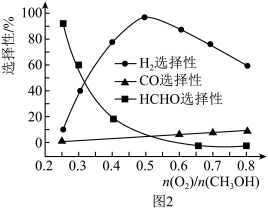
③在一定条件下用氧气催化氧化甲醇制氢气,原料气中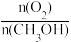 对反应的选择性影响如题图2所示(选择性越大表示生成的该物质越多)。制备H2时最好控制
对反应的选择性影响如题图2所示(选择性越大表示生成的该物质越多)。制备H2时最好控制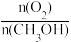 =
=______ ,当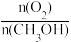 = 0.25时,CH3OH和O2发生的主要反应方程式为
= 0.25时,CH3OH和O2发生的主要反应方程式为______ 。
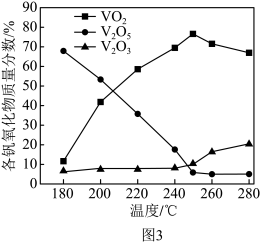
(2)以V2O5为原料,采用微波辅热-甲醇还原法可制备VO2,在微波功率1000kW下,取相同质量的反应物放入反应釜中,改变反应温度,保持反应时间为90min,反应温度对各钒氧化物质量分数的影响曲线如图3所示,温度高于250℃时,VO2的质量分数下降的原因是______ 。
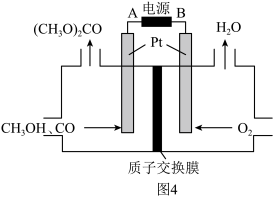
(3)以甲醇为原料,可以通过电化学方法合成碳酸二甲酯[(CH3O)2CO],工作原理如图4所示。
①电源的负极为______ (填“A”或“B”)。
②阳极的电极反应式为______ 。
(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ. CH3OH(g)+H2O(g)
 3H2(g)+CO2(g) △H1
3H2(g)+CO2(g) △H1反应Ⅱ. H2(g)+CO2(g)
 H2O(g)+CO(g) △H2= a kJ·mol-1
H2O(g)+CO(g) △H2= a kJ·mol-1反应Ⅲ. CH3OH(g)
 2H2(g)+CO(g) △H3= b kJ·mol-1
2H2(g)+CO(g) △H3= b kJ·mol-1 反应Ⅳ. 2CH3OH(g)
 2H2O(g)+C2H4(g) △H4= c kJ·mol-1
2H2O(g)+C2H4(g) △H4= c kJ·mol-1①△H1=
②工业上采用CaO吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图1,请分析加入CaO提高氢气产率的原因:

③在一定条件下用氧气催化氧化甲醇制氢气,原料气中
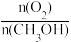 对反应的选择性影响如题图2所示(选择性越大表示生成的该物质越多)。制备H2时最好控制
对反应的选择性影响如题图2所示(选择性越大表示生成的该物质越多)。制备H2时最好控制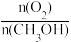 =
=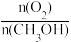 = 0.25时,CH3OH和O2发生的主要反应方程式为
= 0.25时,CH3OH和O2发生的主要反应方程式为
(2)以V2O5为原料,采用微波辅热-甲醇还原法可制备VO2,在微波功率1000kW下,取相同质量的反应物放入反应釜中,改变反应温度,保持反应时间为90min,反应温度对各钒氧化物质量分数的影响曲线如图3所示,温度高于250℃时,VO2的质量分数下降的原因是

(3)以甲醇为原料,可以通过电化学方法合成碳酸二甲酯[(CH3O)2CO],工作原理如图4所示。
①电源的负极为
②阳极的电极反应式为

您最近一年使用:0次
2020-01-19更新
|
314次组卷
|
3卷引用:江苏省无锡市普通高中2019-2020学年高三上学期期终调研试化学试题
12-13高三上·江苏无锡·期末
3 . 二甲醚(CH3OCH。)和甲醇(CH3OH)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
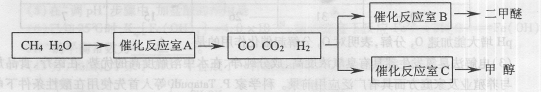
(1)催化反应室B中CO与H2合成二甲醚的化学方程式为____ 。
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)……(I)
CO(g)+H2O(g)⇌CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g)⇌CH3OH(g)……(Ⅲ)
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率=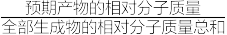 ×100%,试求反应(Ⅳ)的原子利用率为
×100%,试求反应(Ⅳ)的原子利用率为____ 。
②反应(Ⅳ)的△S____ 0(填“>”、“=”或“<”)。
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如图。则该反应的△H____ 0(填“>”、“=”或“<”)。300℃时该反应的平衡常数K=____ (用含字母的代数式表示)。

(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:CH3OCH3-12e-+16OH-=2CO +11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
①将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量____ 。
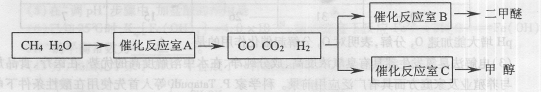
(1)催化反应室B中CO与H2合成二甲醚的化学方程式为
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)……(I)
CO(g)+H2O(g)⇌CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g)⇌CH3OH(g)……(Ⅲ)
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率=
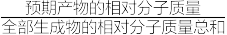 ×100%,试求反应(Ⅳ)的原子利用率为
×100%,试求反应(Ⅳ)的原子利用率为②反应(Ⅳ)的△S
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如图。则该反应的△H

(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:CH3OCH3-12e-+16OH-=2CO
 +11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:①将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量
您最近一年使用:0次



