1 . 甲醇是一种基本的有机化工原料,用途十分广泛。
已知:CH3OH(g) ⇌HCHO(g)+H2(g) ΔH=+84kJ·mol-1
2H2(g)+O2(g) ⇌2H2O(g) ΔH=-484kJ·mol-1
(1)①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:_______ 。
②若在恒温恒容的容器内进行反应CO(g)+2H2(g) ⇌CH3OH(g),下列表示该反应达到平衡状态的标志有_______ (填字母序号)。
A.容器中混合气体的密度不变化
B.有2个H—H键断裂的同时有3个C—H键生成
C.容器中混合气体的压强不变化
D.CH3OH(g)百分含量保持不变
(2)工业上以CO、CO2、H2为原料制备甲醇,其原理如下:
主反应:①CO+2H2⇌CH3OH ②CO2+3H2⇌CH3OH+H2O
副反应:2CO⇌CO2+C 2CO+2H2⇌CH4+CO2
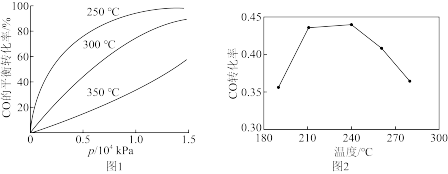
CO在不同温度下的平衡转化率与压强的关系如图1所示。该反应ΔH_____ (填“>”或“<”)0,实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是_____ 。由图2知,当温度高于240℃时,CO转化率下降的原因为_____ 。
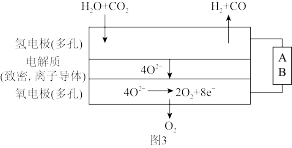
(3)电解水蒸气和CO2产生合成气(H2+CO)。较高温度下(700~1000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2,由图3可知A为直流电源的_____ (填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:_____ 。
已知:CH3OH(g) ⇌HCHO(g)+H2(g) ΔH=+84kJ·mol-1
2H2(g)+O2(g) ⇌2H2O(g) ΔH=-484kJ·mol-1
(1)①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:
②若在恒温恒容的容器内进行反应CO(g)+2H2(g) ⇌CH3OH(g),下列表示该反应达到平衡状态的标志有
A.容器中混合气体的密度不变化
B.有2个H—H键断裂的同时有3个C—H键生成
C.容器中混合气体的压强不变化
D.CH3OH(g)百分含量保持不变
(2)工业上以CO、CO2、H2为原料制备甲醇,其原理如下:
主反应:①CO+2H2⇌CH3OH ②CO2+3H2⇌CH3OH+H2O
副反应:2CO⇌CO2+C 2CO+2H2⇌CH4+CO2
CO在不同温度下的平衡转化率与压强的关系如图1所示。该反应ΔH

(3)电解水蒸气和CO2产生合成气(H2+CO)。较高温度下(700~1000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2,由图3可知A为直流电源的

您最近一年使用:0次
2 . 锌及其化合物用途广泛。火法炼锌以闪锌矿(主要成分是ZnS)为主要原料,涉及的主要反应有: 2ZnS(s) + 3O2(g) = 2ZnO(s) + 2SO2(g) 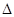 H1=-930 kJ·mol-1
H1=-930 kJ·mol-1
2C(s) + O2(g) = 2CO(g)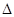 H2=-221 kJ·mol-1
H2=-221 kJ·mol-1
ZnO(s) + CO(g) = Zn(g) + CO2(g)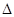 H3= +198 kJ·mol-1
H3= +198 kJ·mol-1
(1)反应ZnS(s) + C(s) + 2O2(g) =Zn(g) + CO2(g) + SO2(g)的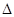 H4=
H4=________ kJ·mol-1。
反应中生成的CO2与NH3混合,在一定条件下反应合成尿素:
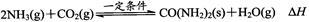
若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是________ 。
a.CO2与H2O(g)浓度相等 b.容器中气体的压强不再改变
c.2v(NH3)正 = v(H2O)逆 d.容器中混合气体的密度不再改变
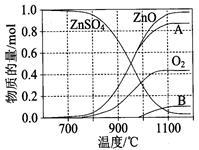
(2)硫酸锌可广泛用作印染媒染剂和木材防腐剂。ZnSO4受热分解过程中各物质物质的量随温度变化关系如图所示。
① 写出700℃~980℃时发生反应的化学方程式:_______ ,物质B的化学式是______ 。
② 硫酸锌分解生成的SO2经下图中的两个循环可分别得到S和H2SO4。写出循环I中反应2的化学方程式:______ ;循环II中电解过程阳极反应式是________ 。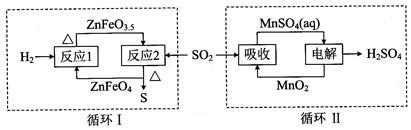
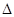 H1=-930 kJ·mol-1
H1=-930 kJ·mol-12C(s) + O2(g) = 2CO(g)
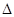 H2=-221 kJ·mol-1
H2=-221 kJ·mol-1ZnO(s) + CO(g) = Zn(g) + CO2(g)
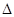 H3= +198 kJ·mol-1
H3= +198 kJ·mol-1(1)反应ZnS(s) + C(s) + 2O2(g) =Zn(g) + CO2(g) + SO2(g)的
 H4=
H4=反应中生成的CO2与NH3混合,在一定条件下反应合成尿素:
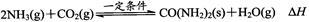
若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是
a.CO2与H2O(g)浓度相等 b.容器中气体的压强不再改变
c.2v(NH3)正 = v(H2O)逆 d.容器中混合气体的密度不再改变
(2)硫酸锌可广泛用作印染媒染剂和木材防腐剂。ZnSO4受热分解过程中各物质物质的量随温度变化关系如图所示。
① 写出700℃~980℃时发生反应的化学方程式:
② 硫酸锌分解生成的SO2经下图中的两个循环可分别得到S和H2SO4。写出循环I中反应2的化学方程式:


您最近一年使用:0次
2016-12-09更新
|
596次组卷
|
2卷引用:2015-2016学年江苏省江阴市青阳中学高二下期中化学试卷



