名校
解题方法
1 . 通过“价类二维图”研究物质性质是化学研究的重要方法,如图是氯元素的部分化合价与物质类别的对应关系。

(1)X化学式为___________ 。
(2)氯的某种氧化物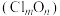 中氯、氧元素质量比为
中氯、氧元素质量比为 ,则
,则
___________ 。
(3) 与Z都可用于消毒,等物质的量的两种物质,消毒效率
与Z都可用于消毒,等物质的量的两种物质,消毒效率 是Z的
是Z的___________ 倍(消毒效率以单位物质的量得到的电子数表示)。我国最近成功研制出由 与Z制取
与Z制取 的新方法,请写出该反应的化学方程式
的新方法,请写出该反应的化学方程式___________ 。(并用双线桥法表示电子转移方向和数目)
(4)Y可用于实验室制取 ,其焰色试验为紫色,用Y和浓盐酸反应可制取Z气体,验证Z气体已经收集满的实验操作和现象是
,其焰色试验为紫色,用Y和浓盐酸反应可制取Z气体,验证Z气体已经收集满的实验操作和现象是___________ 。
(5)某反应使用催化剂后,其反应过程中能量变化如图所示(A+B→C+D为反应①,C+D→E+F为反应②,A+B→E+F为总反应)
___________ (用 和
和 表示)
表示)

(6)已知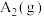 和
和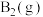 反应生成
反应生成 过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为
过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为___________  。
。

(7)甲同学用 盐酸与
盐酸与 溶液进行中和反应,通过计算得到
溶液进行中和反应,通过计算得到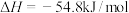 ,该结果与
,该结果与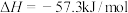 有偏差,产生此偏差的原因可能是
有偏差,产生此偏差的原因可能是___________ (填字母)。
A.用温度计测量盐酸起始温度后直接测是 溶液的温度
溶液的温度
B.一次性把 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中
C.实验装保温、隔热效果差

(1)X化学式为
(2)氯的某种氧化物
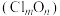 中氯、氧元素质量比为
中氯、氧元素质量比为 ,则
,则
(3)
 与Z都可用于消毒,等物质的量的两种物质,消毒效率
与Z都可用于消毒,等物质的量的两种物质,消毒效率 是Z的
是Z的 与Z制取
与Z制取 的新方法,请写出该反应的化学方程式
的新方法,请写出该反应的化学方程式(4)Y可用于实验室制取
 ,其焰色试验为紫色,用Y和浓盐酸反应可制取Z气体,验证Z气体已经收集满的实验操作和现象是
,其焰色试验为紫色,用Y和浓盐酸反应可制取Z气体,验证Z气体已经收集满的实验操作和现象是(5)某反应使用催化剂后,其反应过程中能量变化如图所示(A+B→C+D为反应①,C+D→E+F为反应②,A+B→E+F为总反应)

 和
和 表示)
表示)
(6)已知
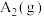 和
和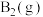 反应生成
反应生成 过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为
过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为 。
。
| 化学键 | A≡A | B—B |
键能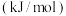 | 946 | 436 |
(7)甲同学用
 盐酸与
盐酸与 溶液进行中和反应,通过计算得到
溶液进行中和反应,通过计算得到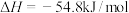 ,该结果与
,该结果与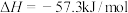 有偏差,产生此偏差的原因可能是
有偏差,产生此偏差的原因可能是A.用温度计测量盐酸起始温度后直接测是
 溶液的温度
溶液的温度B.一次性把
 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中C.实验装保温、隔热效果差
您最近一年使用:0次
名校
2 . 氮及其化合物在生产、环保研究等方面用途非常广泛,回答下列问题:
(1)用浓氨水除去Fe(OH)3样品中少量的Cu(OH)2,生成[Cu(NH3)4]2+,1mol[Cu(NH3)4]2+含______ molσ键。
(2)硝酸厂尾气可以回收制备硝酸。已知:
①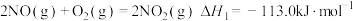
②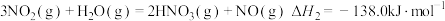
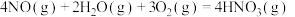 ,
,
______  。
。
(3)在隔绝空气的密闭容器中发生反应:FeSO4(aq)+NO(g) Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是______。(填标号)
Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是______。(填标号)
(4)向一恒容密闭容器中充入适量NH3和O2,在一定条件下发生反应,氧化产物是N2、NO、NO2、N2O中的一种,达到平衡时改变温度,反应物和生成物的浓度与温度关系如图所示:______ (填化学式),写出该反应的化学方程式:______ 。
②正反应
______ (填“>”“<”或“=”)0,判断依据是______
③T3℃时NH3的平衡转化率为______ 。
(1)用浓氨水除去Fe(OH)3样品中少量的Cu(OH)2,生成[Cu(NH3)4]2+,1mol[Cu(NH3)4]2+含
(2)硝酸厂尾气可以回收制备硝酸。已知:
①
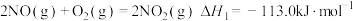
②
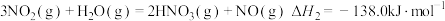
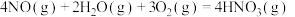 ,
,
 。
。(3)在隔绝空气的密闭容器中发生反应:FeSO4(aq)+NO(g)
 Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是______。(填标号)
Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是______。(填标号)| A.溶液颜色不变,反应达到平衡状态 | B.其他条件不变,充入少量O2,平衡不移动 |
| C.其他条件不变,加少量FeSO4,溶液颜色加深 | D.其他条件不变,微热,溶液颜色加深 |
(4)向一恒容密闭容器中充入适量NH3和O2,在一定条件下发生反应,氧化产物是N2、NO、NO2、N2O中的一种,达到平衡时改变温度,反应物和生成物的浓度与温度关系如图所示:

②正反应

③T3℃时NH3的平衡转化率为
您最近一年使用:0次
2024-03-19更新
|
377次组卷
|
3卷引用:2024届吉林省通化市梅河口市第五中学高三下学期一模化学试题
23-24高三下·江苏南通·开学考试
名校
3 .  是环境污染物。
是环境污染物。
(1)消除 转化为游离态的氮。氮元素的单质有
转化为游离态的氮。氮元素的单质有 。
。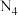 分子有多种结构,一种
分子有多种结构,一种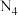 分子中4个氮原子在同一平面上,
分子中4个氮原子在同一平面上,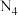 的结构式为
的结构式为_______ 。
(2)以氨气为原料脱硝除去 。
。
①合成氨是人类科学技术上的一项重大突破,氨的用途广泛。
已知: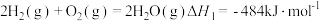
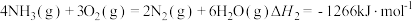
则 的
的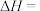
_______  。
。
②近期我国科学家为了解决合成氨反应速率和平衡产率的矛盾,选择使用 双催化剂,通过光辐射产生温差(如体系温度为
双催化剂,通过光辐射产生温差(如体系温度为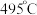 时,
时, 的温度为
的温度为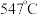 ,而
,而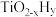 的温度为
的温度为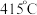 )。结合图1示解释该双催化剂的工作原理是
)。结合图1示解释该双催化剂的工作原理是_______ 。 。研究表明催化剂添加助剂后催化活性提高的原因是形成活性
。研究表明催化剂添加助剂后催化活性提高的原因是形成活性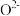 参与反应,图2为丙烯脱硝机理。
参与反应,图2为丙烯脱硝机理。_______ 。(用化学式表示)
②若参加反应的丙烯与 物质的量之比为
物质的量之比为 ,则反应的化学方程式为
,则反应的化学方程式为_______ 。
(4)以 为原料脱硝除去
为原料脱硝除去 。
。
烟气中的 与
与 反应缓慢。雾化后的
反应缓慢。雾化后的 在催化剂中
在催化剂中 元素作用下可以产生具有极强氧化活性的
元素作用下可以产生具有极强氧化活性的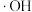 (羟基自由基),
(羟基自由基),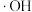 能将
能将 快速氧化为
快速氧化为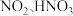 等物质。
等物质。  在一种固体催化剂表面转化的过程如图3所示:
在一种固体催化剂表面转化的过程如图3所示:_______ 。
②化学式为 的催化剂中,
的催化剂中, 和
和 的物质的量之比为
的物质的量之比为_______ 。
 是环境污染物。
是环境污染物。(1)消除
 转化为游离态的氮。氮元素的单质有
转化为游离态的氮。氮元素的单质有 。
。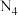 分子有多种结构,一种
分子有多种结构,一种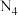 分子中4个氮原子在同一平面上,
分子中4个氮原子在同一平面上,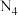 的结构式为
的结构式为(2)以氨气为原料脱硝除去
 。
。①合成氨是人类科学技术上的一项重大突破,氨的用途广泛。
已知:
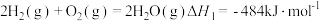
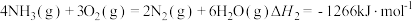
则
 的
的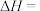
 。
。②近期我国科学家为了解决合成氨反应速率和平衡产率的矛盾,选择使用
 双催化剂,通过光辐射产生温差(如体系温度为
双催化剂,通过光辐射产生温差(如体系温度为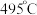 时,
时, 的温度为
的温度为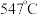 ,而
,而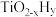 的温度为
的温度为 )。结合图1示解释该双催化剂的工作原理是
)。结合图1示解释该双催化剂的工作原理是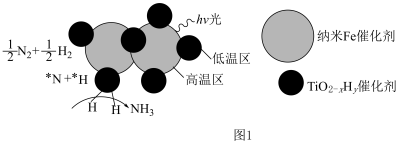
 。研究表明催化剂添加助剂后催化活性提高的原因是形成活性
。研究表明催化剂添加助剂后催化活性提高的原因是形成活性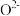 参与反应,图2为丙烯脱硝机理。
参与反应,图2为丙烯脱硝机理。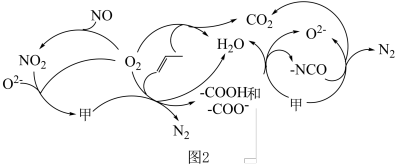
②若参加反应的丙烯与
 物质的量之比为
物质的量之比为 ,则反应的化学方程式为
,则反应的化学方程式为(4)以
 为原料脱硝除去
为原料脱硝除去 。
。烟气中的
 与
与 反应缓慢。雾化后的
反应缓慢。雾化后的 在催化剂中
在催化剂中 元素作用下可以产生具有极强氧化活性的
元素作用下可以产生具有极强氧化活性的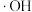 (羟基自由基),
(羟基自由基),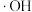 能将
能将 快速氧化为
快速氧化为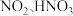 等物质。
等物质。  在一种固体催化剂表面转化的过程如图3所示:
在一种固体催化剂表面转化的过程如图3所示: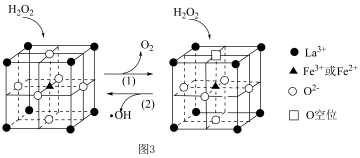
②化学式为
 的催化剂中,
的催化剂中, 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解题方法
4 . 运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
I.氨为重要的化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a. CH4(g)+H2O(g) CO(g)+3H2(g) ∆H1=+216.4kJ/mol
CO(g)+3H2(g) ∆H1=+216.4kJ/mol
b. CO(g)+H2O(g) CO2(g)+H2(g) ∆H2= –41.2kJ/mol
CO2(g)+H2(g) ∆H2= –41.2kJ/mol
则反应CH4(g)+2H2O(g) CO2(g)+4H2(g) ∆H=
CO2(g)+4H2(g) ∆H= _________ 。
(2)起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。
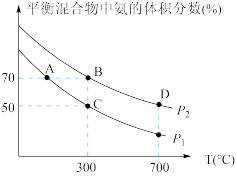
①恒压时,反应一定达到平衡状态的标志是_________ (填序号)
A. 和
和 的转化率相等 B.反应体系密度保持不变
的转化率相等 B.反应体系密度保持不变
C. 保持不变 D.
保持不变 D.
②P1_________ P2 (填“>” “<”“=”或“不确定”,下同);反应的平衡常数:B点_________ D点。
③C点 的转化率为
的转化率为_________ ;在A、B两点条件下,该反应从开始到平衡时生成氮气的平均速率:υ(A)_________ υ(B)。
Ⅱ.用间接电化学法去除烟气中NO的原理如下图所示。

(3)已知阴极室溶液呈酸性,则阴极的电极反应式为_________ 。
I.氨为重要的化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a. CH4(g)+H2O(g)
 CO(g)+3H2(g) ∆H1=+216.4kJ/mol
CO(g)+3H2(g) ∆H1=+216.4kJ/molb. CO(g)+H2O(g)
 CO2(g)+H2(g) ∆H2= –41.2kJ/mol
CO2(g)+H2(g) ∆H2= –41.2kJ/mol则反应CH4(g)+2H2O(g)
 CO2(g)+4H2(g) ∆H=
CO2(g)+4H2(g) ∆H= (2)起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。

①恒压时,反应一定达到平衡状态的标志是
A.
 和
和 的转化率相等 B.反应体系密度保持不变
的转化率相等 B.反应体系密度保持不变C.
 保持不变 D.
保持不变 D.
②P1
③C点
 的转化率为
的转化率为Ⅱ.用间接电化学法去除烟气中NO的原理如下图所示。

(3)已知阴极室溶液呈酸性,则阴极的电极反应式为
您最近一年使用:0次
5 . 合成氨是目前人工固氮最重要的途径,研究合成氨的反应和氨气的用途具有重要意义。工业上合成氨的反应为: 。请回答下列问题:
。请回答下列问题:
(1)①合成氨反应过程片段的作用机理,可以用如下模拟示意图表示。

写出符合在催化剂表面合成氨反应过程的正确排序_______ (用字母标号表示)。
②已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量或气态原子形成1mol化学键所放出的能量。结合下表中化学键的键能数值,计算合成氨反应中生成 时
时_______ (填“吸收”或“放出”)的热量是_______ kJ。
(2)某同学在实验室模拟工业合成氨的反应:恒温下,在2L定容密闭容器中通入 和
和 ,催化剂存在下发生反应。
,催化剂存在下发生反应。
①容器中压强( )随时间(
)随时间( )的变化图象如图所示,测得
)的变化图象如图所示,测得 ,反应开始至5min,用
,反应开始至5min,用 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为_______ 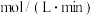 ,平衡时氢气的转化率为
,平衡时氢气的转化率为_______ 。

②下列情况能说明该反应一定达到化学平衡状态的是_______ (填标号)。
A.每消耗 的同时生成
的同时生成
B.
C. 的含量保持不变
的含量保持不变
D.混合气体的平均相对分子质量不变
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示。

①溶液中 向电极
向电极_______ (填“a”或“b”)移动。
②电极a的电极反应式为_______ 。
 。请回答下列问题:
。请回答下列问题:(1)①合成氨反应过程片段的作用机理,可以用如下模拟示意图表示。

写出符合在催化剂表面合成氨反应过程的正确排序
②已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量或气态原子形成1mol化学键所放出的能量。结合下表中化学键的键能数值,计算合成氨反应中生成
 时
时| 化学键 | H-H | N-H | N≡N |
键能/( ) ) | 436 | 391 | 946 |
 和
和 ,催化剂存在下发生反应。
,催化剂存在下发生反应。①容器中压强(
 )随时间(
)随时间( )的变化图象如图所示,测得
)的变化图象如图所示,测得 ,反应开始至5min,用
,反应开始至5min,用 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为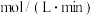 ,平衡时氢气的转化率为
,平衡时氢气的转化率为
②下列情况能说明该反应一定达到化学平衡状态的是
A.每消耗
 的同时生成
的同时生成
B.

C.
 的含量保持不变
的含量保持不变D.混合气体的平均相对分子质量不变
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示。

①溶液中
 向电极
向电极②电极a的电极反应式为
您最近一年使用:0次
名校
解题方法
6 . 生产生活中氨及铵盐有重要用途,而汽车尾气中含NO、NO2则应降低其排放。
(1)已知(活化能单位 ):
):
则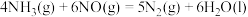 的
的
_______  。
。
(2)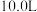 的密闭容器中,按物质的量比
的密闭容器中,按物质的量比 投入氮气和氢气,发生反应
投入氮气和氢气,发生反应 用传感器测得温度为
用传感器测得温度为 时容器中
时容器中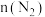 随时间变化如表:
随时间变化如表:
① 时,
时,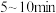 内
内 平均速率为
平均速率为
_______ ;
② 时,该反应平衡常数为
时,该反应平衡常数为_______ (列出计算式);
③x_______ 0.06(填“>”“<”或“=”),原因是_______ 。
④将 与
与 的混合气体置于绝热恒容密闭容器中发生反应,正反应速率随时间变化的趋势如图所示(催化剂活性始终保持不变),下列说法正确的是
的混合气体置于绝热恒容密闭容器中发生反应,正反应速率随时间变化的趋势如图所示(催化剂活性始终保持不变),下列说法正确的是_______ 。
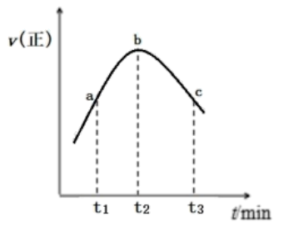
A.反应在b点达到平衡状态
B.从 到
到 逆反应的速率先增大后减小
逆反应的速率先增大后减小
C.a、b、c三点中,c点 的转化率最大
的转化率最大
D.如果将容器改为恒温恒容,其它条件不变,c点 的产率会变小
的产率会变小
(1)已知(活化能单位
 ):
):| 反应 | 正反应活化能 | 逆反应活化能 |
 | 282 | 102 |
 | a | b |
则
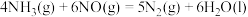 的
的
 。
。(2)
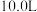 的密闭容器中,按物质的量比
的密闭容器中,按物质的量比 投入氮气和氢气,发生反应
投入氮气和氢气,发生反应 用传感器测得温度为
用传感器测得温度为 时容器中
时容器中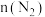 随时间变化如表:
随时间变化如表:物质的量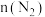 | 0 |  |  | 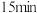 |  |
 |  | 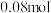 |  |  |  |
 |  | 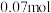 | _______ |  | 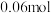 |
①
 时,
时,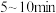 内
内 平均速率为
平均速率为
②
 时,该反应平衡常数为
时,该反应平衡常数为③x
④将
 与
与 的混合气体置于绝热恒容密闭容器中发生反应,正反应速率随时间变化的趋势如图所示(催化剂活性始终保持不变),下列说法正确的是
的混合气体置于绝热恒容密闭容器中发生反应,正反应速率随时间变化的趋势如图所示(催化剂活性始终保持不变),下列说法正确的是
A.反应在b点达到平衡状态
B.从
 到
到 逆反应的速率先增大后减小
逆反应的速率先增大后减小C.a、b、c三点中,c点
 的转化率最大
的转化率最大D.如果将容器改为恒温恒容,其它条件不变,c点
 的产率会变小
的产率会变小
您最近一年使用:0次
2021-04-16更新
|
209次组卷
|
2卷引用:吉林省松原市前郭尔罗斯蒙古族自治县第五中学2021届高三下学期第三次摸底测试化学试题
7 . 二氧化碳是用途非常广泛的基础化工原料,回答下列问题:
(1)工业上可以用 来生产燃料甲醇。
来生产燃料甲醇。
已知: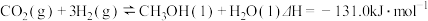 ;
;

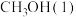 的燃烧热
的燃烧热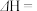
_________ 。
(2)在催化剂作用下, 和
和 可以直接转化为乙酸:
可以直接转化为乙酸: 。在不同温度下乙酸的生成速率变化如图所示。
。在不同温度下乙酸的生成速率变化如图所示。

①温度在 范围时,乙酸的生成速率减慢的主要原因是
范围时,乙酸的生成速率减慢的主要原因是___________ ,当温度在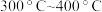 范围时,影响乙酸生成速率的主要因素是
范围时,影响乙酸生成速率的主要因素是__________ 。
②欲使乙酸的平衡产率提高,应采取的措施是__________ (填标号)。
A.升高温度 B.降低温度 C.增大压强 D.加入合适的催化剂
(3)高温下, 与足量的碳在密闭容器中实现反应:
与足量的碳在密闭容器中实现反应:
①向容积为1L的恒容器中加入0.2mol ,在不同温度下达到平衡时
,在不同温度下达到平衡时 的物质的量浓度
的物质的量浓度 随温度的变化如图所示。
随温度的变化如图所示。

某温度下,若向该平衡体系中再通入0.2mol ,达到新平衡后,体系中CO的百分含量
,达到新平衡后,体系中CO的百分含量________ (填“变大”“变小”或“不变”)。若升高温度,再次达到平衡,气体的平均摩尔质量_______ (填“变大”“变小”或“不变”或“无法确定”)
②向压强为p MPa、体积可变的恒压容器中充入一定量 ,
, 时反应达到平衡,CO的体积分数为40%,则
时反应达到平衡,CO的体积分数为40%,则 的转化率为
的转化率为_________ 。
(4)反应 的正、逆反应速率可表示为:
的正、逆反应速率可表示为: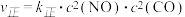 ,
,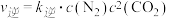 ;k正、k逆分别为正、逆反应速率常数,c为物质的量浓度,一定温度下,在体积为1L的容器加入2mol NO和2mol CO发生上述反应,测得CO和
;k正、k逆分别为正、逆反应速率常数,c为物质的量浓度,一定温度下,在体积为1L的容器加入2mol NO和2mol CO发生上述反应,测得CO和 物质的量浓度随时间的变化如下图所示,则a点时,v正:v逆=
物质的量浓度随时间的变化如下图所示,则a点时,v正:v逆=__________

(1)工业上可以用
 来生产燃料甲醇。
来生产燃料甲醇。已知:
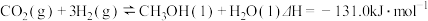 ;
;
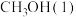 的燃烧热
的燃烧热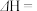
(2)在催化剂作用下,
 和
和 可以直接转化为乙酸:
可以直接转化为乙酸: 。在不同温度下乙酸的生成速率变化如图所示。
。在不同温度下乙酸的生成速率变化如图所示。
①温度在
 范围时,乙酸的生成速率减慢的主要原因是
范围时,乙酸的生成速率减慢的主要原因是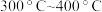 范围时,影响乙酸生成速率的主要因素是
范围时,影响乙酸生成速率的主要因素是②欲使乙酸的平衡产率提高,应采取的措施是
A.升高温度 B.降低温度 C.增大压强 D.加入合适的催化剂
(3)高温下,
 与足量的碳在密闭容器中实现反应:
与足量的碳在密闭容器中实现反应:
①向容积为1L的恒容器中加入0.2mol
 ,在不同温度下达到平衡时
,在不同温度下达到平衡时 的物质的量浓度
的物质的量浓度 随温度的变化如图所示。
随温度的变化如图所示。
某温度下,若向该平衡体系中再通入0.2mol
 ,达到新平衡后,体系中CO的百分含量
,达到新平衡后,体系中CO的百分含量②向压强为p MPa、体积可变的恒压容器中充入一定量
 ,
, 时反应达到平衡,CO的体积分数为40%,则
时反应达到平衡,CO的体积分数为40%,则 的转化率为
的转化率为(4)反应
 的正、逆反应速率可表示为:
的正、逆反应速率可表示为: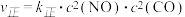 ,
,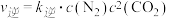 ;k正、k逆分别为正、逆反应速率常数,c为物质的量浓度,一定温度下,在体积为1L的容器加入2mol NO和2mol CO发生上述反应,测得CO和
;k正、k逆分别为正、逆反应速率常数,c为物质的量浓度,一定温度下,在体积为1L的容器加入2mol NO和2mol CO发生上述反应,测得CO和 物质的量浓度随时间的变化如下图所示,则a点时,v正:v逆=
物质的量浓度随时间的变化如下图所示,则a点时,v正:v逆=
您最近一年使用:0次
8 . 运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
I.氨为重要的化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:a. CH4(g)+H2O(g) CO(g)+3H2(g) ∆H1=+216.4kJ/mol,b.CO(g)+H2O(g)
CO(g)+3H2(g) ∆H1=+216.4kJ/mol,b.CO(g)+H2O(g) 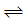 CO2(g)+H2(g) ∆H2=-41.2kJ/mol,则反应CH4(g)+2H2O(g)⇌CO2(g)+4H2(g)∆H=
CO2(g)+H2(g) ∆H2=-41.2kJ/mol,则反应CH4(g)+2H2O(g)⇌CO2(g)+4H2(g)∆H= ____ 。
(2)起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。
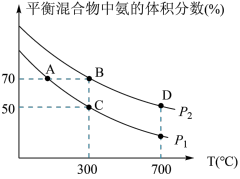
①恒压时,反应一定达到平衡状态的标志是_______ (填序号)。
A. 和
和 的转化率相等 B.反应体系密度保持不变
的转化率相等 B.反应体系密度保持不变
C. 保持不变 D.
保持不变 D.
②P1_____ P2 (填“>”“=”或“不确定”)。
③C点 的转化率为
的转化率为____ ;在A、B两点条件下,该反应从开始到平衡时生成氮气的平均速率:υ(A)__ υ(B) (填“>”“=”或“不确定”)。
Ⅱ.用间接电化学法去除烟气中NO的原理如下图所示。已知阴极室溶液呈酸性,则阴极的电极反应式为____ 。反应过程中通过质子交换膜(ab)的 为2mol时,吸收柱中生成的气体在标准状况下的体积为
为2mol时,吸收柱中生成的气体在标准状况下的体积为______ L。

I.氨为重要的化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:a. CH4(g)+H2O(g)
 CO(g)+3H2(g) ∆H1=+216.4kJ/mol,b.CO(g)+H2O(g)
CO(g)+3H2(g) ∆H1=+216.4kJ/mol,b.CO(g)+H2O(g) 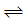 CO2(g)+H2(g) ∆H2=-41.2kJ/mol,则反应CH4(g)+2H2O(g)⇌CO2(g)+4H2(g)∆H=
CO2(g)+H2(g) ∆H2=-41.2kJ/mol,则反应CH4(g)+2H2O(g)⇌CO2(g)+4H2(g)∆H= (2)起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。

①恒压时,反应一定达到平衡状态的标志是
A.
 和
和 的转化率相等 B.反应体系密度保持不变
的转化率相等 B.反应体系密度保持不变C.
 保持不变 D.
保持不变 D.
②P1
③C点
 的转化率为
的转化率为Ⅱ.用间接电化学法去除烟气中NO的原理如下图所示。已知阴极室溶液呈酸性,则阴极的电极反应式为
 为2mol时,吸收柱中生成的气体在标准状况下的体积为
为2mol时,吸收柱中生成的气体在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
9 . 新华社报道:全国农村应当在“绿色生态·美丽多彩·低碳节能·循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。可见“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃、101kPa时:
①C(s)+ O2(g)=CO(g) ΔH=-126.4kJ/mol
O2(g)=CO(g) ΔH=-126.4kJ/mol
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol
③H2O(g)=H2O(l) ΔH=-44kJ/mol
则在25℃、101kPa时:
C(s)+H2O(g)=CO(g)+H2(g) ΔH=_____ 。
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0
Fe(s)+CO2(g) ΔH>0
已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值____ (填“增大”“减小”或“不变”)。
②1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?____ (填“是”或“否”),其判断依据是___ 。
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol。
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol。
现向体积为1L的恒容密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
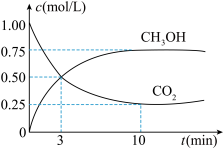
①从反应开始到平衡,氢气的平均反应速率v(H2)=____ 。
②下列措施能使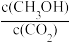 增大的是
增大的是____ (填字母)。
A.升高温度
B.再充入H2
C.再充入CO2
D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃、101kPa时:
①C(s)+
 O2(g)=CO(g) ΔH=-126.4kJ/mol
O2(g)=CO(g) ΔH=-126.4kJ/mol②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol
③H2O(g)=H2O(l) ΔH=-44kJ/mol
则在25℃、101kPa时:
C(s)+H2O(g)=CO(g)+H2(g) ΔH=
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)
 Fe(s)+CO2(g) ΔH>0
Fe(s)+CO2(g) ΔH>0已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值
②1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol。
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol。现向体积为1L的恒容密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)=
②下列措施能使
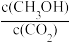 增大的是
增大的是A.升高温度
B.再充入H2
C.再充入CO2
D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
您最近一年使用:0次
2019-11-16更新
|
135次组卷
|
4卷引用:吉林省长春市吉林省实验中学2019-2020学年高二上学期期中考试化学试题
真题
名校
10 . 砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________ 。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________ 。该反应需要在加压下进行,原因是________________________ 。
(3)已知:As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
(4)298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应: (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
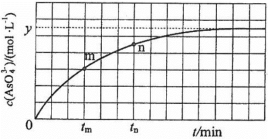
①下列可判断反应达到平衡的是__________ (填标号)。
a.溶液的pH不再变化
b.v(I−)=2v( )
)
c.c( )/c(
)/c( )不再变化
)不再变化
d.c(I−)=y mol·L−1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________ 。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________ 。
(1)画出砷的原子结构示意图
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式
(3)已知:As(s)+
 H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1H2(g)+ O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =
(4)298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应:
 (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是
a.溶液的pH不再变化
b.v(I−)=2v(
 )
)c.c(
 )/c(
)/c( )不再变化
)不再变化d.c(I−)=y mol·L−1
②tm时,v正
③tm时v逆
④若平衡时溶液的pH=14,则该反应的平衡常数K为
您最近一年使用:0次
2017-08-08更新
|
8534次组卷
|
16卷引用:吉林省长春市东北师大附中2020届高中毕业班三月份网络教学质量监测卷理科综合化学部分
吉林省长春市东北师大附中2020届高中毕业班三月份网络教学质量监测卷理科综合化学部分2017年全国普通高等学校招生统一考试理综化学(新课标Ⅲ卷精编版)内蒙古集宁一中2018届高三上学期第三次月考化学试题(已下线)黄金30题系列 高三化学 大题易丢分西藏拉萨北京实验中学2018届高三第五次月考理科综合化学试题(已下线)《考前20天终极攻略》-5月29日 化学反应原理综合(已下线)解密10 化学反应速率与化学平衡(教师版)——备战2018年高考化学之高频考点解密(已下线)解密20 原理综合题(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题2020届湖南省湘潭市高三教学质量监测卷化学试题广西北流市实验中学2019-2020学年高二下学期期中考试理科综合化学试题(已下线)专题14 化学反应原理综合-备战2021届高考化学二轮复习题型专练广东省湛江市第二十一中学2021-2022学年高二上学期期中考试化学试题云南省昌宁县第一中学2021-2022学年高三下学期3月月考化学试题云南省玉溪市民族中学2021-2022学年高三1月份考试理综化学试题



