1 . 硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO2的催化氧化:SO2(g)+ O2(g)
O2(g) SO3(g) ΔH=−98 kJ·mol−1。回答下列问题:
SO3(g) ΔH=−98 kJ·mol−1。回答下列问题:
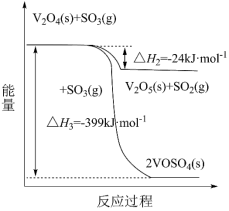
(1)钒催化剂参与反应的能量变化如图所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:_________ 。
(2)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α 随温度的变化如图所示。反应在5.0MPa、550℃时的α=__________ ,判断的依据是__________ 。影响α的因素有__________ 。

(3)将组成(物质的量分数)为2m% SO2(g)、m% O2(g)和q% N2(g)的气体通入反应器,在温度t、压强p条件下进行反应。平衡时,若SO2转化率为α,则SO3压强为___________ ,平衡常数Kp=___________ (以分压表示,分压=总压×物质的量分数)。
(4)研究表明,SO2催化氧化的反应速率方程为:v=k(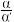 −1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图所示。
−1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图所示。
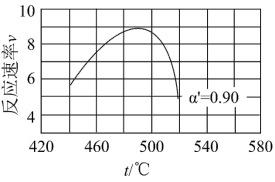
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。t<tm时,v逐渐提高;t>tm后,v逐渐下降。原因是__________________________ 。
 O2(g)
O2(g) SO3(g) ΔH=−98 kJ·mol−1。回答下列问题:
SO3(g) ΔH=−98 kJ·mol−1。回答下列问题:(1)钒催化剂参与反应的能量变化如图所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:

(2)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α 随温度的变化如图所示。反应在5.0MPa、550℃时的α=

(3)将组成(物质的量分数)为2m% SO2(g)、m% O2(g)和q% N2(g)的气体通入反应器,在温度t、压强p条件下进行反应。平衡时,若SO2转化率为α,则SO3压强为
(4)研究表明,SO2催化氧化的反应速率方程为:v=k(
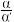 −1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图所示。
−1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图所示。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。t<tm时,v逐渐提高;t>tm后,v逐渐下降。原因是
您最近一年使用:0次
2020-07-08更新
|
19315次组卷
|
14卷引用:北京大学附属中学2021-2022学年高二下学期期末考试化学试卷
北京大学附属中学2021-2022学年高二下学期期末考试化学试卷2020年全国统一考试化学试题(新课标Ⅰ)(已下线)专题14 化学反应原理综合-2020年高考真题和模拟题化学分项汇编(已下线)专题15 化学反应原理大题不丢分-2021年高考化学必做热点专题(已下线)重点9 化学反应原理的综合应用-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)重点8 化学反应原理的综合应用-2021年高考化学专练【热点·重点·难点】(已下线)押全国卷理综第28题 化学反应原理-备战2021年高考化学临考题号押题2020年全国卷Ⅰ理综化学高考真题变式题(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点09 化学反应原理综合-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押全国卷理综第28题 化学反应原理-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题15化学反应原理综合-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题15化学反应原理综合-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题17 原理综合题
2 . 化学链燃烧( )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集
)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于
。基于 载氧体的甲烷化学链燃烧技术示意图如下。
载氧体的甲烷化学链燃烧技术示意图如下。
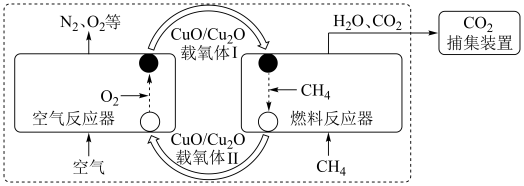
空气反应器与燃料反应器中发生的反应分别为:
①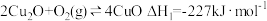
②
(1)反应

_______  。
。
(2)反应②的平衡常数表达式
_______ 。
(3)氧的质量分数:载氧体Ⅰ_______ (填“>”“=”或“<”)载氧体Ⅱ。
(4)往盛有 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数
载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生反应①。平衡时
为21%】,发生反应①。平衡时 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。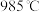 时
时 的平衡转化率
的平衡转化率
_______ (保留2位有效数字)。
(5)根据下图, 随温度升高而增大的原因是
随温度升高而增大的原因是_______ 。反应温度必须控制在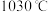 以下,原因是
以下,原因是_______ 。

(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的 载氧体,反应②活化能如下表所示。
载氧体,反应②活化能如下表所示。
由表中数据判断:使用_______ (填“氧化铝”或“膨润土”)掺杂的载氧体反应较快;使用氧化铝或者膨润土掺杂的载氧体,单位时间内燃料反应器释放的热量分别为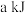 、
、 ,则a
,则a_______ b(填“>”“=”或“<”)。
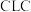 )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集
)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于
。基于 载氧体的甲烷化学链燃烧技术示意图如下。
载氧体的甲烷化学链燃烧技术示意图如下。
空气反应器与燃料反应器中发生的反应分别为:
①
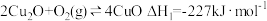
②

(1)反应


 。
。(2)反应②的平衡常数表达式

(3)氧的质量分数:载氧体Ⅰ
(4)往盛有
 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数
载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生反应①。平衡时
为21%】,发生反应①。平衡时 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。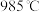 时
时 的平衡转化率
的平衡转化率
(5)根据下图,
 随温度升高而增大的原因是
随温度升高而增大的原因是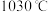 以下,原因是
以下,原因是
(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的
 载氧体,反应②活化能如下表所示。
载氧体,反应②活化能如下表所示。| 载氧体掺杂物质 | 氧化铝 | 膨润土 |
活化能/ |  | 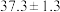 |
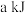 、
、 ,则a
,则a
您最近一年使用:0次
2021-11-09更新
|
5516次组卷
|
7卷引用:北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题
北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题2021年新高考福建化学高考真题(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编福建省龙岩第一中学2021-2022学年高二下学期开学考试(实验班)化学试题(已下线)专题17 原理综合题(已下线)专题17 原理综合题福建省福州市福建师范大学附属中学2022-2023学年高二下学期期末化学试题
3 . 丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+ O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为________ kJ·mol-1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x_____________ 0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是__________ (填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
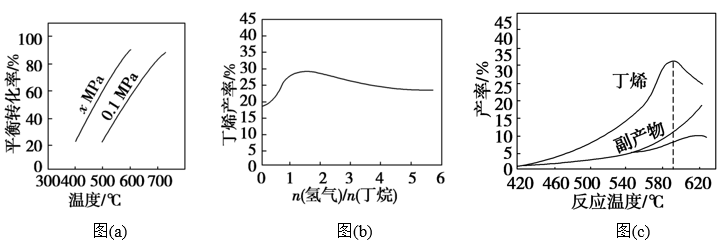
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是___________ 。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590 ℃之前随温度升高而增大的原因可能是___________ 、____________ ;590℃之后,丁烯产率快速降低的主要原因可能是_____________ 。
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+
 O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1③H2(g)+
 O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
O2(g)= H2O(g) ΔH3=-242 kJ·mol-1反应①的ΔH1为
A.升高温度 B.降低温度 C.增大压强 D.降低压强

(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590 ℃之前随温度升高而增大的原因可能是
您最近一年使用:0次
2017-08-08更新
|
11799次组卷
|
28卷引用:北京市中国人民大学附属中学2020届高三教学质量监测理科综合化学试题
北京市中国人民大学附属中学2020届高三教学质量监测理科综合化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅱ卷精编版)安徽省淮北市濉溪中学等三校2017-2018学年高二上学期期中联考化学试题(已下线)解密10 化学反应速率与化学平衡(教师版)——备战2018年高考化学之高频考点解密【全国百强校】四川省棠湖中学2019届高三上学期第三次月考理综-化学试题重庆市北碚区2019-2020学年高二11月联合性测试化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》(已下线)专题7.2 化学平衡状态 化学平衡移动(讲)-《2020年高考一轮复习讲练测》(已下线)专题十一 化学反应速率和化学平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训河北衡水中学2020届高三下学期三月份教学质量监测理科综合化学试题湖北省武汉市华中师范大学第一附属中学2020届高三2月份网络教学质量监测理综化学试题四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题河北省石家庄市第二中学2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分安徽省马鞍山市2020届高考第二次模拟理综化学试题湖南省株洲市2020年高中毕业班教学质量监测卷理科综合化学试题安徽省合肥市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题陕西省西安市西北工业大学附属中学2020届高三教学质量监测理科综合化学试题广东省广州市华南师范大学附属中学2020届高三教学质量监测卷理科综合化学试题山东省潍坊市临朐县实验中学2020-2021学年高二9月月考化学试题(已下线)第23讲 化学平衡状态 化学平衡的移动 (精讲)——2021年高考化学一轮复习讲练测陕西省子洲中学2019-2020学年高二下学期第一次月考化学试题福建省永安市第一中学2020-2021学年高二上学期第一次月考化学试题山东省东营市胜利第二中学2020-2021学年高二10月月考化学试题(已下线)第19讲 化学平衡(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题(已下线)第19讲 化学平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)贵州省贵阳市2022-2023学年高三上学期10月质量监测化学试题(已下线)第28讲化化学平衡的移动及反应进行的方向
2020·浙江·高考真题
4 . 研究 氧化
氧化 制
制 对资源综合利用有重要意义。相关的主要化学反应有:
对资源综合利用有重要意义。相关的主要化学反应有:
Ⅰ
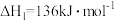
Ⅱ

Ⅲ

Ⅳ
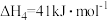
已知: 时,相关物质的相对能量(如图1)。
时,相关物质的相对能量(如图1)。
可根据相关物质的相对能量计算反应或变化的 (
( 随温度变化可忽略)。例如:
随温度变化可忽略)。例如: 
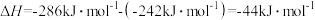 。
。
请回答:
(1)①根据相关物质的相对能量计算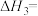
_____  。
。
②下列描述正确的是_____
A 升高温度反应Ⅰ的平衡常数增大
B 加压有利于反应Ⅰ、Ⅱ的平衡正向移动
C 反应Ⅲ有助于乙烷脱氢,有利于乙烯生成
D 恒温恒压下通水蒸气,反应Ⅳ的平衡逆向移动
③有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下: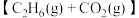

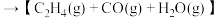 ,且第二步速率较慢(反应活化能为
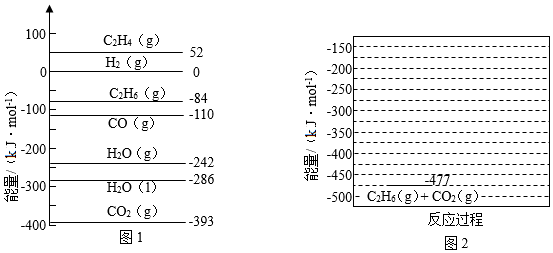
,且第二步速率较慢(反应活化能为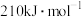 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量-反应过程图”,起点从
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量-反应过程图”,起点从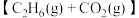 的能量
的能量 ,开始(如图2)
,开始(如图2)_____ 。
(2)① 和
和 按物质的量1:1投料,在
按物质的量1:1投料,在 和保持总压恒定的条件下,研究催化剂X对“
和保持总压恒定的条件下,研究催化剂X对“ 氧化
氧化 制
制 ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:
结合具体反应分析,在催化剂X作用下, 氧化
氧化 的主要产物是
的主要产物是______ ,判断依据是_______ 。
②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高 的选择性(生成
的选择性(生成 的物质的量与消耗
的物质的量与消耗 的物质的量之比)。在
的物质的量之比)。在 ,乙烷平衡转化率为
,乙烷平衡转化率为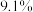 ,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到
,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到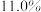 。结合具体反应说明乙烷转化率增大的原因是
。结合具体反应说明乙烷转化率增大的原因是_____ 。
 氧化
氧化 制
制 对资源综合利用有重要意义。相关的主要化学反应有:
对资源综合利用有重要意义。相关的主要化学反应有:Ⅰ

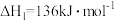
Ⅱ


Ⅲ


Ⅳ

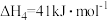
已知:
 时,相关物质的相对能量(如图1)。
时,相关物质的相对能量(如图1)。
可根据相关物质的相对能量计算反应或变化的
 (
( 随温度变化可忽略)。例如:
随温度变化可忽略)。例如: 
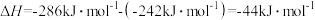 。
。请回答:
(1)①根据相关物质的相对能量计算
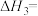
 。
。②下列描述正确的是
A 升高温度反应Ⅰ的平衡常数增大
B 加压有利于反应Ⅰ、Ⅱ的平衡正向移动
C 反应Ⅲ有助于乙烷脱氢,有利于乙烯生成
D 恒温恒压下通水蒸气,反应Ⅳ的平衡逆向移动
③有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:
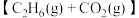

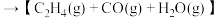 ,且第二步速率较慢(反应活化能为
,且第二步速率较慢(反应活化能为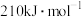 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量-反应过程图”,起点从
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量-反应过程图”,起点从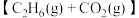 的能量
的能量 ,开始(如图2)
,开始(如图2)(2)①
 和
和 按物质的量1:1投料,在
按物质的量1:1投料,在 和保持总压恒定的条件下,研究催化剂X对“
和保持总压恒定的条件下,研究催化剂X对“ 氧化
氧化 制
制 ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:| 催化剂 | 转化率 | 转化率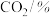 | 产率 |
| 催化剂X | 19.0 | 37.6 | 3.3 |
 氧化
氧化 的主要产物是
的主要产物是②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高
 的选择性(生成
的选择性(生成 的物质的量与消耗
的物质的量与消耗 的物质的量之比)。在
的物质的量之比)。在 ,乙烷平衡转化率为
,乙烷平衡转化率为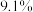 ,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到
,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到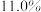 。结合具体反应说明乙烷转化率增大的原因是
。结合具体反应说明乙烷转化率增大的原因是
您最近一年使用:0次
2020-07-11更新
|
5287次组卷
|
8卷引用:2023-2024学年度第二学期高三化学零模试卷
(已下线)2023-2024学年度第二学期高三化学零模试卷北京市师范大学附属实验中学2024届高三零模化学试题2020年浙江省高考化学试卷(7月选考)(已下线)专题09 反应速率、化学平衡-2020年高考真题和模拟题化学分项汇编选择性必修1 专题2 素养检测(已下线)专题20.化学反应原理综合应用-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)专题17 原理综合题
名校
解题方法
5 . 以CO和 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为甲醇。
转化为甲醇。
已知:①
 kJ·mol
kJ·mol
②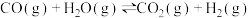
 kJ·mol
kJ·mol
③
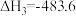 kJ·mol
kJ·mol
下列说法不正确 的是
 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为甲醇。
转化为甲醇。已知:①

 kJ·mol
kJ·mol
②
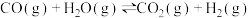
 kJ·mol
kJ·mol
③

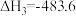 kJ·mol
kJ·mol
下列说法
A.若温度不变,反应①中生成1 mol  时,放出的热量大于90.5 kJ 时,放出的热量大于90.5 kJ |
B. 与 与 合成甲醇的热化学方程式为: 合成甲醇的热化学方程式为:  kJ·mol kJ·mol |
C.通过电解制 和选用高效催化剂,可降低 和选用高效催化剂,可降低 与 与 合成甲醇反应的焓变 合成甲醇反应的焓变 |
D.以 和 和 为原料合成甲醇,同时生成 为原料合成甲醇,同时生成 ,该反应需要吸收能量 ,该反应需要吸收能量 |
您最近一年使用:0次
2022-11-27更新
|
925次组卷
|
7卷引用:北京市海淀区2021-2022学年高三上学期期中考试化学试题
北京市海淀区2021-2022学年高三上学期期中考试化学试题北京市第二十二中学2021-2022学年高三上学期12月阶段性测试理科化学试题北京市东城区一六六中学2022-2023学年高三上学期期中考试化学试题(已下线)2023年北京卷高考真题变式题(选择题11-14)天津市静海区第一中学2021-2022学年高三上学期12月调研考试化学试题(已下线)考点17 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)化学反应的热效应
名校
解题方法
6 . 以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程如图所示。
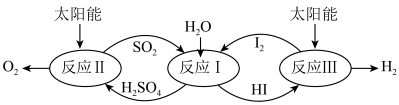
相关反应的热化学方程式为:
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) H1=-213kJ•mol-1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+ O2(g) H2=+327kJ•mol-1
O2(g) H2=+327kJ•mol-1
反应Ⅲ:2HI(aq)=H2(g)+I2(g) H3=+172kJ•mol-1
下列说法不正确的是

相关反应的热化学方程式为:
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) H1=-213kJ•mol-1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+
 O2(g) H2=+327kJ•mol-1
O2(g) H2=+327kJ•mol-1反应Ⅲ:2HI(aq)=H2(g)+I2(g) H3=+172kJ•mol-1
下列说法不正确的是
| A.该过程实现了太阳能到化学能的转化 |
| B.SO2和I2对总反应起到了催化作用 |
| C.总反应的热化学方程式为2H2O(l)=2H2(g)+O2(g) H=+286kJ•mol-1 |
| D.该过程降低了水分解制氢的活化能,但总反应的H不变 |
您最近一年使用:0次
2020-10-12更新
|
2798次组卷
|
28卷引用:【区级联考】北京市海淀区2019届高三第一学期上学期期末考试化学试题
【区级联考】北京市海淀区2019届高三第一学期上学期期末考试化学试题北京市2020届高三12月月考(新高考选考模式)化学试题北京市2020届高三质量监测化学试题北京市第三十一中学2021-2022学年高二上学期期中考试化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题(已下线)2023年北京卷高考真题变式题(选择题11-14)【全国百强校】浙江省学军中学2019届高三下学期4月选考模拟冲刺化学试题【全国百强校】内蒙古自治区赤峰二中2018-2019学年高一下学期第二次月考化学试题(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》2019年秋高三化学复习强化练习—— 盖斯定律及其应用河南省实验中学2020届高三12月月考化学试题(已下线)考点06 化学能与热能-2020年高考化学命题预测与模拟试题分类精编山东省济南市历城第二中学2021届高三10月份学情检测化学试题人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 过模拟 2年模拟精编精练湖北省部分省重点中学2020-2021学年高二上学期期中联考化学试题湖北省部分重点中学2020-2021学年高二上学期期中考试化学试题(已下线)押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)安徽省怀宁中学2020-2021学年高一下学期第一次月考化学试题(已下线)高中化学《新教材变化解读与考法剖析》第一章 化学反应的热效应(人教版2019选择性必修1)山东省聊城第三中学2021-2022学年高二上学期第三次质量检测化学试题山东省聊城市第二中学2022-2023学年高二上学期第一次月考化学试题山东省临沂市平邑县第一中学2022-2023学年高二上学期10月月考化学试题 湖北省仙桃中学2022-2023学年高一上学期10月月考化学试题湖南省衡阳市第八中学2022-2023学年高二下学期5月月考化学试题湖南省南雅中学2023-2024学年高二上学期第一次月考化学试题江西省宜春市上高二中2023-2024学年高二上学期第一次月考化学试题河北省唐山市丰润区2023-2024学年高二上学期期中考试化学试题福建省厦门市集美中学2023-2024学年高二上学期10月第一次月考化学试题
7 . 环己烯是有机合成的重要中间体,可由环已烷氧化脱氢制备。已知几种物质的燃烧热(25℃, ):
):
下列说法正确的是
 ):
):| 名称 | 氢气 | 环己烯 | 环已烷 |
| 化学式(状态) |  | 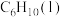 | 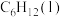 |
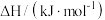 |  |  | 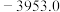 |
A.氢气燃烧的热化学方程式为 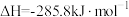 |
| B.由燃烧热可知,环己烯的能量小于环已烷的能量 |
C. 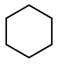 (l)= (l)= 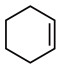 (l)+H2(g) (l)+H2(g)  |
| D.环已烷氧化脱氢制备环己烯时,氧气和高锰酸钾均可作氧化剂 |
您最近一年使用:0次
名校
解题方法
8 . 实现二氧化碳选择性、稳定性加氢合成甲醇是“甲醇经济”理念下的一个重要成果。由CO2和H2合成CH3OH的反应过程如下:
I.CO2(g)+H2(g) CO(g)+H2O(g) △H1=+40.9kJ·mol-1
CO(g)+H2O(g) △H1=+40.9kJ·mol-1
II.CO(g)+2H2(g) CH3OH(g) △H2=-90.4kJ·mol-1
CH3OH(g) △H2=-90.4kJ·mol-1
回答下列问题:
(1)如图是一种特定条件下反应I机理中的第一步变化,则碳原子的杂化类型从____ 变为___ 。
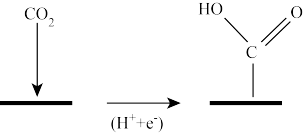
(2)写出由CO2和H2合成CH3OH的热化学方程式为____ 。
(3)恒压条件下,按n(CO2):n(H2)=1:3投料时,该反应在无分子筛膜和有分子筛膜时甲醇的平衡产率随温度的变化如图所示。(分子筛膜能选择性分离出H2O)
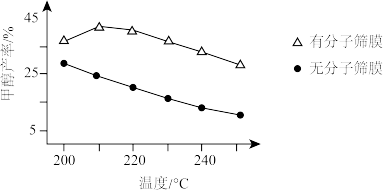
①根据图中数据,恒压条件下采用有分子筛膜时的最佳反应温度为____ ℃。
②有分子筛膜时甲醇产率高的原因是____ 。
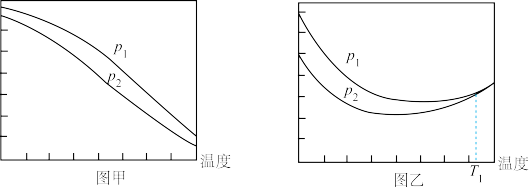
(4)不同压强下,依然按n(CO2):n(H2)=1:3投料,测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。
已知:CO2的平衡转化率=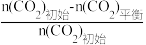 ×100%
×100%
CH3OH的平衡产率= ×100%
×100%
①压强:p1____ p2(填“>”“=”或“<”),判断依据是____ 。
②纵坐标表示CO2平衡转化率的是图____ (填“甲”或“乙”)。
③图乙中T1温度时,两条曲线几乎交于一点的原因是____ 。
I.CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+40.9kJ·mol-1
CO(g)+H2O(g) △H1=+40.9kJ·mol-1II.CO(g)+2H2(g)
 CH3OH(g) △H2=-90.4kJ·mol-1
CH3OH(g) △H2=-90.4kJ·mol-1回答下列问题:
(1)如图是一种特定条件下反应I机理中的第一步变化,则碳原子的杂化类型从

(2)写出由CO2和H2合成CH3OH的热化学方程式为
(3)恒压条件下,按n(CO2):n(H2)=1:3投料时,该反应在无分子筛膜和有分子筛膜时甲醇的平衡产率随温度的变化如图所示。(分子筛膜能选择性分离出H2O)

①根据图中数据,恒压条件下采用有分子筛膜时的最佳反应温度为
②有分子筛膜时甲醇产率高的原因是
(4)不同压强下,依然按n(CO2):n(H2)=1:3投料,测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

已知:CO2的平衡转化率=
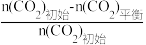 ×100%
×100%CH3OH的平衡产率=
 ×100%
×100%①压强:p1
②纵坐标表示CO2平衡转化率的是图
③图乙中T1温度时,两条曲线几乎交于一点的原因是
您最近一年使用:0次
9 . 实现二氧化碳选择性,稳定性加氢合成甲醇是“甲醇经济”理念下的一个重要成果。反应包括两步:
Ⅰ.
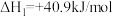
Ⅱ.
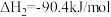
(1)由 合成
合成 的热化学方程式
的热化学方程式_______ 。
(2)恒压下,按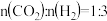 时,该反应在无分子筛膜和有分子筛膜时甲醇的平衡产率随温度的变化如图所示。(分子筛膜能选择性分离出水)。
时,该反应在无分子筛膜和有分子筛膜时甲醇的平衡产率随温度的变化如图所示。(分子筛膜能选择性分离出水)。

①根据图中数据,压强不变采用有分子筛膜时的最佳反应温度为_______  。
。
②有分子筛膜时甲醇产率高的原因是_______ 。
(3)如果在不同压强下, 和
和 的起始物质的量比仍为
的起始物质的量比仍为 ,测定
,测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度升高的变化关系,如图所示:
的平衡产率随温度升高的变化关系,如图所示:

已知: 的平衡转化率
的平衡转化率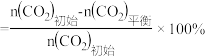 ,
, 的平衡产率
的平衡产率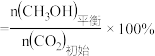 。
。
①压强p1______ p2(填“ ”或“
”或“ ”),原因
”),原因_______ 。
②其中图中纵坐标表示CO2平衡转化率的是图_______ (填“甲”或“乙”)。
③图乙中T1温度时,两条曲线几乎交于一点,分析原因_______ 。
Ⅰ.

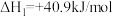
Ⅱ.

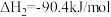
(1)由
 合成
合成 的热化学方程式
的热化学方程式(2)恒压下,按
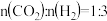 时,该反应在无分子筛膜和有分子筛膜时甲醇的平衡产率随温度的变化如图所示。(分子筛膜能选择性分离出水)。
时,该反应在无分子筛膜和有分子筛膜时甲醇的平衡产率随温度的变化如图所示。(分子筛膜能选择性分离出水)。
①根据图中数据,压强不变采用有分子筛膜时的最佳反应温度为
 。
。②有分子筛膜时甲醇产率高的原因是
(3)如果在不同压强下,
 和
和 的起始物质的量比仍为
的起始物质的量比仍为 ,测定
,测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度升高的变化关系,如图所示:
的平衡产率随温度升高的变化关系,如图所示:
已知:
 的平衡转化率
的平衡转化率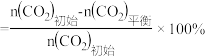 ,
, 的平衡产率
的平衡产率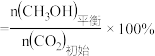 。
。①压强p1
 ”或“
”或“ ”),原因
”),原因②其中图中纵坐标表示CO2平衡转化率的是图
③图乙中T1温度时,两条曲线几乎交于一点,分析原因
您最近一年使用:0次
2021-03-26更新
|
1320次组卷
|
4卷引用:北京市平谷区2021届高三下学期质量监控(零模)化学试题
北京市平谷区2021届高三下学期质量监控(零模)化学试题北京市平谷区2021届高三一模化学试题北京市平谷区2022-2023学年高二上学期期末考试化学试题(已下线)2021年高考全国甲卷化学试题变式题
名校
10 . 我国提出 2060 年前实现碳中和,为有效降低大气 CO2中的含量,以 CO2为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。CO2在固体催化剂表面加氢合成甲烷过程中发生如下反应:
Ⅰ.主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
Ⅱ.副反应:CO2(g)+H2(g) CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-l
CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-l
(1)已知:Ⅲ.2H2(g)+O2(g)=2H2O(g) ∆H3=-395.6 kJ·mol-l
Ⅳ.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H4=__________ 。
(2)CO2加氢合成甲烷时,通常控制温度为 500 °C 左右,其可能的原因为_______。
(3)500 °C 时,向 1 L 恒容密闭容器中充入 4 mol CO2和 12 mol H2,初始压强为 p,20 min 时主、副反应都达到平衡状态,测得 c(H2O)=5 mol·L-1,体系压强为3/4 p, 则 0~ 20 min 内 v(CH4)=________ ,平衡时 CH4选择性= ___________ (CH4选择性= × 100%, 计算保留三位有效数字)。
× 100%, 计算保留三位有效数字)。
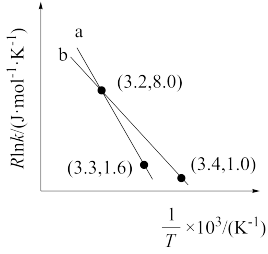
(4)以 CO2催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为 3CH3OH(g) C3H6(g)+3H2O(g)。该反应的 Arrhenius 经验公式的实验数据如图中曲线 a 所示,已知 Arhenius 经验公式
C3H6(g)+3H2O(g)。该反应的 Arrhenius 经验公式的实验数据如图中曲线 a 所示,已知 Arhenius 经验公式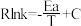 ,(Ea为活化能,k 为速率常数,R 和 C 为常数)。当改变外界条件时,实验数据如图中的曲线 b 所示,则实验可能改变的外界条件是
,(Ea为活化能,k 为速率常数,R 和 C 为常数)。当改变外界条件时,实验数据如图中的曲线 b 所示,则实验可能改变的外界条件是 __________ 。
Ⅰ.主反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-lⅡ.副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-l
CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-l(1)已知:Ⅲ.2H2(g)+O2(g)=2H2O(g) ∆H3=-395.6 kJ·mol-l
Ⅳ.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H4=
(2)CO2加氢合成甲烷时,通常控制温度为 500 °C 左右,其可能的原因为_______。
| A.反应速率快 | B.平衡转化率高 |
| C.催化剂活性高 | D.主反应催化剂选择性好 |
 × 100%, 计算保留三位有效数字)。
× 100%, 计算保留三位有效数字)。(4)以 CO2催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为 3CH3OH(g)
 C3H6(g)+3H2O(g)。该反应的 Arrhenius 经验公式的实验数据如图中曲线 a 所示,已知 Arhenius 经验公式
C3H6(g)+3H2O(g)。该反应的 Arrhenius 经验公式的实验数据如图中曲线 a 所示,已知 Arhenius 经验公式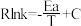 ,(Ea为活化能,k 为速率常数,R 和 C 为常数)。当改变外界条件时,实验数据如图中的曲线 b 所示,则实验可能改变的外界条件是
,(Ea为活化能,k 为速率常数,R 和 C 为常数)。当改变外界条件时,实验数据如图中的曲线 b 所示,则实验可能改变的外界条件是 
您最近一年使用:0次



