1 . 化学反应原理在生产、生活中用途广泛。氮是地球上含量丰富的一种元素,氮及其化合物对我们的生产、生活有重要的影响。请回答下列问题:
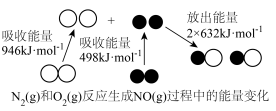
(1)机动车发动机工作时会引发 与
与 的反应(如图所示),请用热化学方程式表示以下反应
的反应(如图所示),请用热化学方程式表示以下反应___________ 。
(2)已知
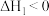 ,
,
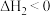 ,下列能量变化示意图中,正确的是___________。
,下列能量变化示意图中,正确的是___________。
(1)机动车发动机工作时会引发
 与
与 的反应(如图所示),请用热化学方程式表示以下反应
的反应(如图所示),请用热化学方程式表示以下反应
(2)已知

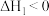 ,
,
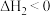 ,下列能量变化示意图中,正确的是___________。
,下列能量变化示意图中,正确的是___________。A.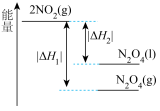 | B.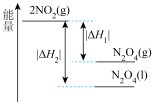 |
C.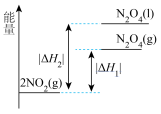 | D.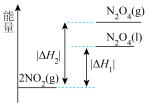 |
您最近一年使用:0次
2 . 下列说法中,正确的是
A. 表示放热反应, 表示放热反应, 表示吸热反应 表示吸热反应 |
| B.热化学方程式中的化学计量数只表示物质的量,可以是分数 |
C.含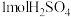 的溶液与含 的溶液与含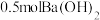 的溶液混合反应,放出的热量即为中和热 的溶液混合反应,放出的热量即为中和热 |
D. 与 与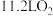 反应生成液态水放出的热量就是 反应生成液态水放出的热量就是 的燃烧热 的燃烧热 |
您最近一年使用:0次
3 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ•mol-1
(1)总反应的△H=________ kJ•mol-1。
(2)下列示意图中能体现上述反应能量变化的是________ 。判断的理由是________ 。
A.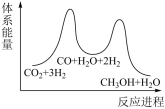 B.
B.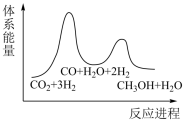 C.
C.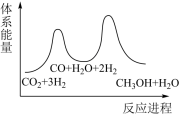
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ•mol-1
(1)总反应的△H=
(2)下列示意图中能体现上述反应能量变化的是
A.
 B.
B. C.
C.
您最近一年使用:0次
名校
解题方法
4 . 如图所示H2和Cl2反应生成HCl的能量变化示意图,由图可知
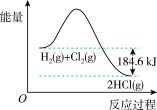

| A..反应物总能量低于生成物总能量 |
| B.H2+Cl2=2HCl+184.6kJ |
| C.H2(g)+Cl2(g)=2HCl(l) △H<-184.6kJ/mol |
| D.1molCl2(g)的能量高于2molHCl(g)的能量 |
您最近一年使用:0次
名校
5 . 已知存在这样的反应:2A(g) B(g)(△H<0);下列能量变化示意图正确的是
B(g)(△H<0);下列能量变化示意图正确的是
 B(g)(△H<0);下列能量变化示意图正确的是
B(g)(△H<0);下列能量变化示意图正确的是A.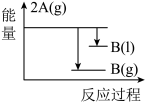 | B.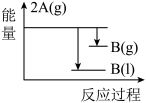 |
C.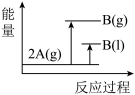 | D.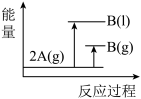 |
您最近一年使用:0次
6 . 我们通过更深入地研究化学反应的方向、限度和速率,利用这些规律来解决日常生活和工业生产中的实际问题,让生活更美好。
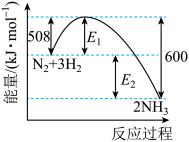
(1)一定条件下,在密闭容器中,氮气与氢气合成氨气,能量变化曲线如图所示。下列说法正确的是___________
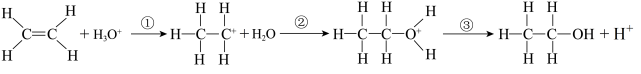
(2)乙烯与水通过加成反应可得乙醇。反应机理、能量变化与反应进程的关系如图所示:
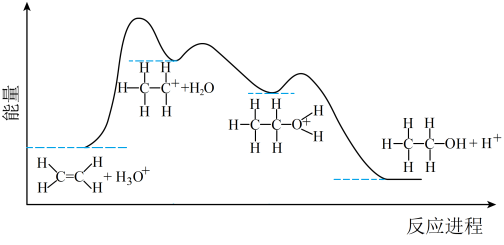
下列叙述正确的是________
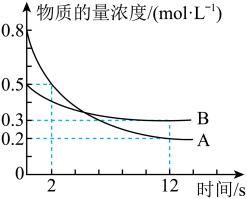
(3)某温度下,在2L恒容密闭容器中投入一定量的A、B,发生反应:3A(g)+bB(g) cC(g)+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是__________
cC(g)+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是__________
(4)一定条件下N2O发生如下反应:
Ⅰ. 2N2O(g) 2N2(g)+O2(g)
2N2(g)+O2(g)  =-164kJ·mol-1
=-164kJ·mol-1
Ⅱ. N2O(g)+CO(g) N2(g)+CO2(g)
N2(g)+CO2(g)  =-356kJ·mol-1
=-356kJ·mol-1
①反应Ⅰ平衡常数的表达式K=___________ 。
②恒温恒容条件下,下列可以作为判断反应Ⅰ达到平衡的依据是___________ 。
a. 气体的压强不变 b. 2v正(N2O)=v逆(O2) c. K不变 d. 容器内气体的密度不变
③某温度下,反应Ⅰ的K=0.16,该温度下,测得容器中N2O、N2、O2的浓度分别为0.5mol·L-1、0.5mol·L-1、0.25mol·L-1,此时,反应Ⅰ是否处于平衡状态? 若不是,预测反应的方向。___________
(5)甲为10L的恒温容器。盛有1mol N2O和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,n(N2):n(O2)=8:1,则n(N2O)=___________ mol;0~5min,O2的平均反应速率v(O2)=___________ mol·L-1·min-1。
(6)不同压强的密闭容器中分别充入1mol N2O和1mol CO,发生反应Ⅰ和反应Ⅱ,测得N2O的平衡转化率与温度的关系如图所示。

P1、P2、P3由小到大的顺序为___________ ;温度高于T0℃时,容器内发生的主要反应为___________ (填“Ⅰ”、“Ⅱ”或“Ⅰ和Ⅱ”)。
(1)一定条件下,在密闭容器中,氮气与氢气合成氨气,能量变化曲线如图所示。下列说法正确的是___________

| A.加入催化剂,E1、E2都变小 |
B.N2(g)+3H2(g)  2NH3(g) 2NH3(g)  =-600kJ·mol-1 =-600kJ·mol-1 |
| C.升温可以增大该反应的化学平衡常数 |
| D.通入1mol N2和3mol H2充分反应,放热小于92kJ |


下列叙述正确的是________
| A.①、②、③三步均属于加成反应 |
| B.H+为反应的催化剂 |
| C.①、②、③三步反应均为放热反应 |
| D.总反应是放热反应,不需要加热就能发生 |
 cC(g)+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是__________
cC(g)+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是__________
| A.0-2s,D的平均反应速率为0.1mol/(L·s) |
| B.12s时,B的转化率为40% |
| C.化学计量系数之比b:c=1:2 |
| D.图中两曲线相交时,A的消耗速率等于A的生成速率 |
Ⅰ. 2N2O(g)
 2N2(g)+O2(g)
2N2(g)+O2(g)  =-164kJ·mol-1
=-164kJ·mol-1Ⅱ. N2O(g)+CO(g)
 N2(g)+CO2(g)
N2(g)+CO2(g)  =-356kJ·mol-1
=-356kJ·mol-1①反应Ⅰ平衡常数的表达式K=
②恒温恒容条件下,下列可以作为判断反应Ⅰ达到平衡的依据是
a. 气体的压强不变 b. 2v正(N2O)=v逆(O2) c. K不变 d. 容器内气体的密度不变
③某温度下,反应Ⅰ的K=0.16,该温度下,测得容器中N2O、N2、O2的浓度分别为0.5mol·L-1、0.5mol·L-1、0.25mol·L-1,此时,反应Ⅰ是否处于平衡状态? 若不是,预测反应的方向。
(5)甲为10L的恒温容器。盛有1mol N2O和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,n(N2):n(O2)=8:1,则n(N2O)=
(6)不同压强的密闭容器中分别充入1mol N2O和1mol CO,发生反应Ⅰ和反应Ⅱ,测得N2O的平衡转化率与温度的关系如图所示。

P1、P2、P3由小到大的顺序为
您最近一年使用:0次
7 . 为了探究化学反应的热效应,某兴趣小组进行了如图所示实验:
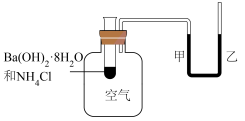
(1)室温下,观察到的现象是_______ 。
(2)理想新能源应具有资源丰富、可再生、无污染等特点,下列属于理想新能源的是_______。

(1)室温下,观察到的现象是
(2)理想新能源应具有资源丰富、可再生、无污染等特点,下列属于理想新能源的是_______。
| A.天然气 | B.煤 | C.太阳能 | D.氢能 |
您最近一年使用:0次
8 . 下列反应符合如图图示的是
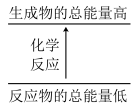

| A.铁在氧气中燃烧 | B.铁粉和硫粉反应 |
| C.煅烧石灰石 | D.铁片与稀硫酸反应 |
您最近一年使用:0次
2023-05-31更新
|
90次组卷
|
3卷引用:上海市行知中学2022-2023学年高一下学期5月月考化学试题
上海市行知中学2022-2023学年高一下学期5月月考化学试题上海市曹杨第二中学2022-2023学年高一下学期期末考试化学试题(已下线)专题01 化学反应与能量变化-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
9 . 化学反应中的能量变化常表现为热量变化,如有的反应为放热反应,有的为吸热反应,请从下列选项中选出对此解释合理的为
| A.旧化学键断裂时吸收的能量高于新化学键形成时所释放的总能量为吸热反应 |
| B.旧化学键断裂时吸收的能量低于新化学键形成时所释放的总能量为吸热反应 |
| C.在化学反应中需要加热的反应就是吸热反应 |
| D.在化学反应中需要使用催化剂的反应为放热反应 |
您最近一年使用:0次
2023-05-25更新
|
261次组卷
|
5卷引用:上海市吴淞中学2023-2024学年高二上学期第一学段考试化学试题
上海市吴淞中学2023-2024学年高二上学期第一学段考试化学试题5.3.1 化学变化中的能量变化(第1课时)-【帮课堂】高一化学同步精品讲义(沪科版2020必修第二册)山西省运城市景胜中学2022-2023学年高一5月月考化学(B卷)试题(已下线)6.1.1化学反应与热能-随堂练习(已下线)专题05 化学反应与能量变化(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
10 . 硫元素与铁可以形成多种硫化物,其中FeS和 最为常见,而FeS又是你最不陌生的,其样品如下图所示。
最为常见,而FeS又是你最不陌生的,其样品如下图所示。

将铁粉与硫粉混合均匀加热,即可生成FeS。但你所不知的是:细粉级的FeS在50℃以上便可自燃,纵然是极其小心地储存,也会被氧气缓慢完全氧化,其中 的Fe被氧化为+3价,同时有淡黄色晶体生成。
的Fe被氧化为+3价,同时有淡黄色晶体生成。
(1)由此信息推断的结论错误的是___________
A.上述铁粉与硫粉的反应是放热反应
B.细粉级的FeS被氧气缓慢时,可生成 和S
和S
C.等量的铁在Cl2中燃烧时,转移的电子数多
D.在50℃以上FeS自燃,有硫生成
E.FeS与硝酸反应,生成
(2)在低温冷冻下,向 溶液中滴加少量
溶液中滴加少量 溶液,得到黑色固体
溶液,得到黑色固体 ,则此反应的离子方程式为
,则此反应的离子方程式为___________ 。将 投入稀盐酸中溶解,有臭鸡蛋气味气体产生。此反应的产物除
投入稀盐酸中溶解,有臭鸡蛋气味气体产生。此反应的产物除 外,还有
外,还有___________ 和___________ (填写化学式)。
 最为常见,而FeS又是你最不陌生的,其样品如下图所示。
最为常见,而FeS又是你最不陌生的,其样品如下图所示。
将铁粉与硫粉混合均匀加热,即可生成FeS。但你所不知的是:细粉级的FeS在50℃以上便可自燃,纵然是极其小心地储存,也会被氧气缓慢完全氧化,其中
 的Fe被氧化为+3价,同时有淡黄色晶体生成。
的Fe被氧化为+3价,同时有淡黄色晶体生成。(1)由此信息推断的结论错误的是
A.上述铁粉与硫粉的反应是放热反应
B.细粉级的FeS被氧气缓慢时,可生成
 和S
和SC.等量的铁在Cl2中燃烧时,转移的电子数多
D.在50℃以上FeS自燃,有硫生成
E.FeS与硝酸反应,生成

(2)在低温冷冻下,向
 溶液中滴加少量
溶液中滴加少量 溶液,得到黑色固体
溶液,得到黑色固体 ,则此反应的离子方程式为
,则此反应的离子方程式为 投入稀盐酸中溶解,有臭鸡蛋气味气体产生。此反应的产物除
投入稀盐酸中溶解,有臭鸡蛋气味气体产生。此反应的产物除 外,还有
外,还有
您最近一年使用:0次



