1 . 已知:①C(s)+2H2(g)=CH4(g) ΔH1 ②C(s)+ H2(g)=
H2(g)= C2H2(g) ΔH2 ③C(s)+H2(g)=
C2H2(g) ΔH2 ③C(s)+H2(g)= C2H4(g) ΔH3;且ΔH2<ΔH3<ΔH1<0。则关于反应C2H2(g)+H2(g)=C2H4(g)和2CH4(g)=C2H4(g)+2H2(g)的说法正确的是
C2H4(g) ΔH3;且ΔH2<ΔH3<ΔH1<0。则关于反应C2H2(g)+H2(g)=C2H4(g)和2CH4(g)=C2H4(g)+2H2(g)的说法正确的是
 H2(g)=
H2(g)= C2H2(g) ΔH2 ③C(s)+H2(g)=
C2H2(g) ΔH2 ③C(s)+H2(g)= C2H4(g) ΔH3;且ΔH2<ΔH3<ΔH1<0。则关于反应C2H2(g)+H2(g)=C2H4(g)和2CH4(g)=C2H4(g)+2H2(g)的说法正确的是
C2H4(g) ΔH3;且ΔH2<ΔH3<ΔH1<0。则关于反应C2H2(g)+H2(g)=C2H4(g)和2CH4(g)=C2H4(g)+2H2(g)的说法正确的是| A.都是放热反应 | B.都是吸热反应 |
| C.前者放热后者吸热 | D.前者吸热后者放热 |
您最近一年使用:0次
2 . 联氨(N2H4)常温下为无色液体,可用作火箭燃料。
①2O2(g)+N2(g)=N2O4(l) ΔH1 ②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3 ④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=﹣1048.9 kJ·mol−1
下列说法不正确的是
①2O2(g)+N2(g)=N2O4(l) ΔH1 ②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3 ④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=﹣1048.9 kJ·mol−1
下列说法不正确的是
| A.O2(g)+2H2(g)=2H2O(l) ΔH5,ΔH5>ΔH3 |
| B.ΔH4=2ΔH3﹣2ΔH2﹣ΔH1 |
| C.1 mol O2(g)和2 mol H2(g)具有的总能量高于2 mol H2O(g) |
| D.联氨和N2O4作火箭推进剂的原因之一是反应放出大量的热 |
您最近一年使用:0次
2022-12-10更新
|
123次组卷
|
2卷引用:河北省唐山市迁西县职业技术教育中心2021-2022学年高二(普职融通部)上学期9月月考化学试题
解题方法
3 . 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用
(1)肼(N2H4)可作为火箭发动机的燃料。肼(N2H4)与氧化剂N2O4(l)反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH1=-195 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1
试计算1 mol肼(l)与N2O4(l)完全反应生成N2和水蒸气时放出的热量为______ kJ,写出肼(l)和N2O4(l)反应的热化学方程式:_____________________ 。
(2)肼一空气燃料电池是一种碱性电池(产物无污染),该电池放电时,负极的电极反应式为________ 。
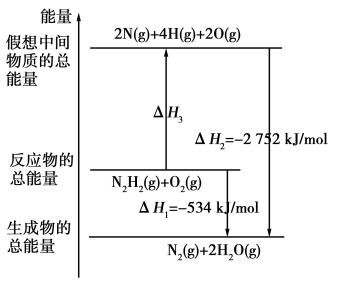
(3)有关肼化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则ΔH3=________ ,断裂1 mol N—H键所需的能量是________ kJ。
(1)肼(N2H4)可作为火箭发动机的燃料。肼(N2H4)与氧化剂N2O4(l)反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH1=-195 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1
试计算1 mol肼(l)与N2O4(l)完全反应生成N2和水蒸气时放出的热量为
(2)肼一空气燃料电池是一种碱性电池(产物无污染),该电池放电时,负极的电极反应式为
(3)有关肼化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则ΔH3=

您最近一年使用:0次
解题方法
4 . 反应C(石墨) → C(金刚石)是吸热反应,由此可知
| A.石墨比金刚石更稳定 | B.金刚石和石墨可以相互转化 |
| C.金刚石比石墨稳定 | D.金刚石和石墨不能相互转化 |
您最近一年使用:0次
解题方法
5 . 试从化学键的角度理解化学反应中的能量变化。(以2H2+O2=2H2O为例说明),已知:E反表示反应物(2H2+O2)所具有的总能量,E生表示生成物(2H2O)所具有的总能量。又知:拆开1moL H2中的化学键需要吸收436kJ能量,拆开1moL O2中的化学键需要吸收496kJ能量,形成水分子中的1moLH-O键能够释放463kJ能量。
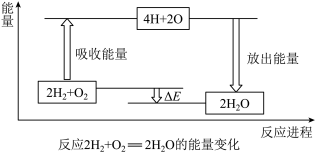
(1)宏观角度看:反应物所具有的总能量高于生成物所具有的总能量,所以该反应_______ (填“吸收”或“放出”)能量。
(2)微观角度看:断裂反应物中的化学键吸收的总能量为E吸 =_______ kJ; 形成生成物中的化学键放出的总能量为E放=_______ kJ。E吸_______ E放(填“>”或“<”),所以该反应要_______ (填“吸收”或“放出”)能量,能量变化值的大小△E=_______ kJ(填数值)

(1)宏观角度看:反应物所具有的总能量高于生成物所具有的总能量,所以该反应
(2)微观角度看:断裂反应物中的化学键吸收的总能量为E吸 =
您最近一年使用:0次
解题方法
6 . 回答下列问题:
(1)甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量关系如图所示。
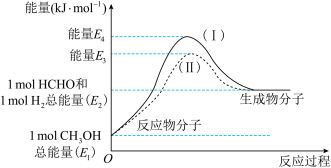
①甲醇催化脱氢转化为甲醛的反应是_______  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
②过程I与过程II的反应热是否相同?_______ ,原因是_______ 。
(2)在25℃、101kPa下,1g甲醇CH3OH燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:_______ 。
(3)CH4(g)+2O2(g)=CO2 (g) +2H2O(l) △H1
CH4(g)+2O2(g)=CO2 (g) +2H2O(g) △H2
则 △H1_______ △H2(填“>”、“﹤”或“=”)
(4)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知: ① N2(g)+2O2(g)=N2O4 (l) △H1= -195.0kJ/mol
② N2H4 (l)+ O2(g)= N2(g)+ 2H2O(g) △H2= -534.2kJ/mol
写出肼和N2O4反应的热化学方程式_______ 。
(1)甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量关系如图所示。

①甲醇催化脱氢转化为甲醛的反应是
 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。②过程I与过程II的反应热是否相同?
(2)在25℃、101kPa下,1g甲醇CH3OH燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:
(3)CH4(g)+2O2(g)=CO2 (g) +2H2O(l) △H1
CH4(g)+2O2(g)=CO2 (g) +2H2O(g) △H2
则 △H1
(4)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知: ① N2(g)+2O2(g)=N2O4 (l) △H1= -195.0kJ/mol
② N2H4 (l)+ O2(g)= N2(g)+ 2H2O(g) △H2= -534.2kJ/mol
写出肼和N2O4反应的热化学方程式
您最近一年使用:0次
解题方法
7 . 我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,在低温下获得高转化率与高反应速率。反应过程示意图如下:
CO2(g)+H2(g) ΔH<0,在低温下获得高转化率与高反应速率。反应过程示意图如下:
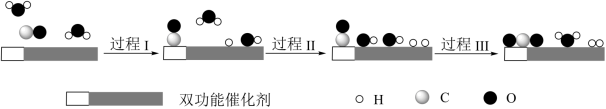
下列说法正确的是
 CO2(g)+H2(g) ΔH<0,在低温下获得高转化率与高反应速率。反应过程示意图如下:
CO2(g)+H2(g) ΔH<0,在低温下获得高转化率与高反应速率。反应过程示意图如下:
下列说法正确的是
| A.过程Ⅰ、过程Ⅱ均为放热过程 |
| B.使用催化剂降低了水煤气变换反应的ΔH |
| C.图示显示:起始时的2个H2O最终都参与了反应 |
| D.该催化过程中:只有极性键的断裂和形成 |
您最近一年使用:0次
名校
8 . 下列与化学反应能量变化相关的叙述中错误的是
| A.放热反应的反应速率总是大于吸热反应的反应速率 |
| B.物质发生化学变化一定伴随能量的变化 |
C.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 相同 相同 |
D.水凝结成冰的过程中, 、 、 |
您最近一年使用:0次
2022-12-09更新
|
468次组卷
|
4卷引用:山东省青岛第二中学2020-2021学年高二上学期期末化学试题
解题方法
9 . 反应 过程中的能量变化如下图所示,回答下列问题。
过程中的能量变化如下图所示,回答下列问题。_______ 热反应(填“吸”、“放”)。
②在反应体系中加入催化剂,反应速率增大,
_______ ,
_______ (填增大”、“减小”或“不变”)。
③当反应达到平衡时,升高温度,A的转化率_______ (填“增大”、“减小”或“不变”)。
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
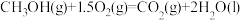
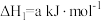
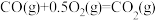
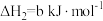
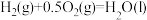
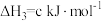
则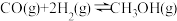

_______  (用a、b、c表示)。
(用a、b、c表示)。
(3)一定压强下,在容积为 的密闭容器中充入
的密闭容器中充入 与
与 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: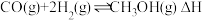 ,平衡转化率与温度、压强的关系如图所示。则
,平衡转化率与温度、压强的关系如图所示。则
_______  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
 过程中的能量变化如下图所示,回答下列问题。
过程中的能量变化如下图所示,回答下列问题。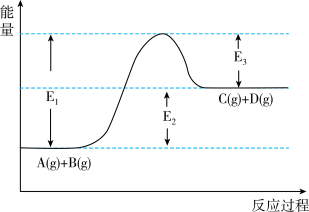
②在反应体系中加入催化剂,反应速率增大,


③当反应达到平衡时,升高温度,A的转化率
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
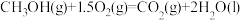
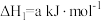
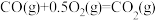
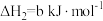
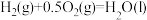
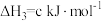
则
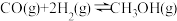

 (用a、b、c表示)。
(用a、b、c表示)。(3)一定压强下,在容积为
 的密闭容器中充入
的密闭容器中充入 与
与 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: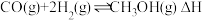 ,平衡转化率与温度、压强的关系如图所示。则
,平衡转化率与温度、压强的关系如图所示。则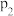
 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);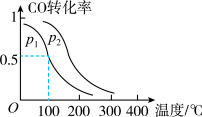
您最近一年使用:0次
名校
解题方法
10 . 生产生活中的化学反应都伴随能量的变化,请回答下列问题。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途,制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)天然气中含有的微量 会腐蚀管道和设备,在
会腐蚀管道和设备,在 下进行脱硫处理,
下进行脱硫处理, 会被氧气氧化为
会被氧气氧化为 ,并产生水蒸气。
,并产生水蒸气。
写出该反应的热化学方程式:___________
(3)汽车尾气中排放的 和
和 会污染环境,在汽车尾气系统中装置催化转化器,可有效降低
会污染环境,在汽车尾气系统中装置催化转化器,可有效降低 和
和 的排放。已知:
的排放。已知:
Ⅰ.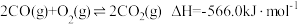
Ⅱ.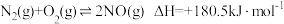
Ⅲ.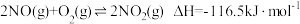
① 的燃烧热为
的燃烧热为___________  。
。
② 将
将 还原为单质的热化学方程式为
还原为单质的热化学方程式为___________ 。
③下图是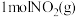 和
和 反应生成
反应生成 和
和 过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是___________ (填“增大”、“减小”或“不变”,下同), 的变化是
的变化是___________ 。


(4)实验室利用如上图装置进行中和热的测定。
①图中还缺少一个玻璃仪器,名称为___________ 。
②在操作正确的前提下,提高中和热测定准确性的关键是___________ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途,制作冷敷袋可以利用
(2)天然气中含有的微量
 会腐蚀管道和设备,在
会腐蚀管道和设备,在 下进行脱硫处理,
下进行脱硫处理, 会被氧气氧化为
会被氧气氧化为 ,并产生水蒸气。
,并产生水蒸气。| 化学键 | 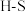 |  |  |  中共价键 中共价键 |
键能/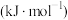 | 339 | 498 | 464 | 1083 |
写出该反应的热化学方程式:
(3)汽车尾气中排放的
 和
和 会污染环境,在汽车尾气系统中装置催化转化器,可有效降低
会污染环境,在汽车尾气系统中装置催化转化器,可有效降低 和
和 的排放。已知:
的排放。已知:Ⅰ.
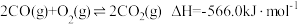
Ⅱ.
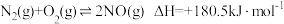
Ⅲ.
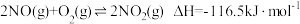
①
 的燃烧热为
的燃烧热为 。
。②
 将
将 还原为单质的热化学方程式为
还原为单质的热化学方程式为③下图是
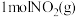 和
和 反应生成
反应生成 和
和 过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是 的变化是
的变化是

(4)实验室利用如上图装置进行中和热的测定。
①图中还缺少一个玻璃仪器,名称为
②在操作正确的前提下,提高中和热测定准确性的关键是
您最近一年使用:0次



