名校
解题方法
1 . 下列说法中正确的是
A.若 白磷的能量比 白磷的能量比 红磷多 红磷多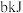 ,则白磷转化为红磷的热化学方程式为 ,则白磷转化为红磷的热化学方程式为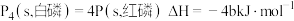 |
B.若 ,则 ,则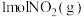 置于密闭容器中充分反应放出的热量为 置于密闭容器中充分反应放出的热量为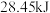 |
C.在稀溶液中,强酸与强碱反应的中和热为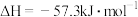 ,若将含有 ,若将含有 的浓硫酸和含有 的浓硫酸和含有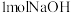 的溶液混合,放出的热量等于 的溶液混合,放出的热量等于 |
D. 的燃烧热是 的燃烧热是 ,则 ,则 |
您最近一年使用:0次
2 . 在下列各说法中,正确的是
A.1mol 与0.5mol 与0.5mol 反应放出的热就是 反应放出的热就是 的燃烧热 的燃烧热 |
| B.化学反应过程中放出的热量就叫反应热 |
C.1mol 与1mol 与1mol 反应生成 反应生成 沉淀时放出的热叫做中和热 沉淀时放出的热叫做中和热 |
D. 表示放热反应, 表示放热反应, 表示吸热反应 表示吸热反应 |
您最近一年使用:0次
3 . 一定条件下,石墨燃烧过程中的能量变化可用下图表示。下列说法不正确的是
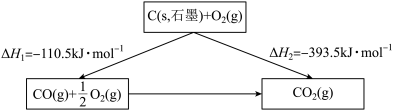

| A.石墨的燃烧热△H1=-110.5kJ/mol |
| B.石墨的燃烧热△H2=-393.5kJ/mol |
| C.由图可知1molCO(g)转化成1molCO2(g)的△H=△H2-△H1 |
| D.已知C(s,金刚石)=C(s,石墨)△H3<0,则1molC(s,金刚石)转化成1molCO2(g)的△H'>△H2 |
您最近一年使用:0次
2023-09-10更新
|
121次组卷
|
2卷引用:云南省文山州广南县第十中学校2023-2024学年高二上学期10月月考化学试题
名校
4 . 下列说法不正确的是
| A.CH4 的燃烧热是890.3kJ·mol-1,则表示 CH4 的燃烧热的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.由C(金刚石)=C(石墨) ΔH=-1.9 kJ·mol-1可知,石墨比金刚石稳定 |
| C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含 1mol HNO3 的稀溶液与含 1mol Ba(OH)2 的稀溶液混合,放出的热量为 57.3 kJ |
| D.1mol 钠蒸气与 2 mol 钠蒸气完全燃烧时,燃烧热相同 |
您最近一年使用:0次
2023-08-19更新
|
371次组卷
|
2卷引用:云南省大理白族自治州民族中学2023-2024学年高二上学期10月月考化学试题
解题方法
5 . 下列有关说法正确的是
A.已知C(s)+O2(g)=CO2(g) ΔH1,C(s)+ O2(g)=CO(g) ΔH2,则ΔH1<ΔH2 O2(g)=CO(g) ΔH2,则ΔH1<ΔH2 |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH=-571.6kJ•mol-1,则H2的燃烧热为285.8kJ•mol-1 |
C.已知HI(g)  H2(g)+ H2(g)+ I2(s) ΔH=-26.5kJ•mol-1,由此可知,在密闭容器中充入1molHI气体,充分分解后可以放出26.5kJ的热量 I2(s) ΔH=-26.5kJ•mol-1,由此可知,在密闭容器中充入1molHI气体,充分分解后可以放出26.5kJ的热量 |
| D.HCl和NaOH反应中和热ΔH=-57.3kJ•mol-1,则:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6kJ•mol-1 |
您最近一年使用:0次
6 . 火电厂利用燃煤发电,煤燃烧中的热化学方程式有:
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
CO(g)+ O2(g)=CO2(g) ΔH2=-283 kJ/mol
O2(g)=CO2(g) ΔH2=-283 kJ/mol
C(s)+ O2(g)=CO(g) ΔH3=?
O2(g)=CO(g) ΔH3=?
下列有关说法中不正确的是
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
CO(g)+
 O2(g)=CO2(g) ΔH2=-283 kJ/mol
O2(g)=CO2(g) ΔH2=-283 kJ/molC(s)+
 O2(g)=CO(g) ΔH3=?
O2(g)=CO(g) ΔH3=?下列有关说法中不正确的是
| A.CO的燃烧热为283 kJ/mol |
| B.二氧化碳分解为一氧化碳和氧气的反应是吸热反应 |
| C.ΔH3=ΔH2-ΔH1=110.5 kJ/mol |
| D.ΔH3=ΔH1-ΔH2=-110.5 kJ/mol |
您最近一年使用:0次
2021-03-17更新
|
163次组卷
|
2卷引用:云南省文山州砚山县第三高级中学2020-2021学年高二1月月考化学试题
解题方法
7 . 在101kPa和298K时,有关反应的热化学方程式有:
H2(g) + O2(g)=H2O(g) ΔH1= -241.8kJ·mol -1
O2(g)=H2O(g) ΔH1= -241.8kJ·mol -1
H2(g) + O2 (g) =H2O(1) ΔH2= -285.8kJ·mol-1
O2 (g) =H2O(1) ΔH2= -285.8kJ·mol-1
下列说法错误的是
H2(g) +
 O2(g)=H2O(g) ΔH1= -241.8kJ·mol -1
O2(g)=H2O(g) ΔH1= -241.8kJ·mol -1H2(g) +
 O2 (g) =H2O(1) ΔH2= -285.8kJ·mol-1
O2 (g) =H2O(1) ΔH2= -285.8kJ·mol-1下列说法错误的是
A.1molH2和 molO2所具有的总能量小于1molH2O( g)所具有的总能量 molO2所具有的总能量小于1molH2O( g)所具有的总能量 |
B.O2前面的系数 表示参加反应的O2的物质的量 表示参加反应的O2的物质的量 |
| C.燃烧热是以在101kPa时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量定义的,则H2的燃烧热ΔH为-285.8kJ·mol-1 |
| D.H2燃烧生成1molH2O(g)时,放出241. 8kJ的热量 |
您最近一年使用:0次
2020-09-18更新
|
96次组卷
|
2卷引用:云南省曲靖市第二中学学联体2019-2020学年高二下学期联合考试(第四次)化学试题
名校
解题方法
8 . 已知热化学方程式:①S(s) + O2(g) = SO2(g) ΔH = -296 kJ·mol-1;
②2SO2(g) + O2(g) 2SO3(g) ΔH = -196.6 kJ·mol-1;
2SO3(g) ΔH = -196.6 kJ·mol-1;
③H2S(g) + O2(g) = SO2(g)+ H2O(l) ΔH = -586 kJ·mol-1。
O2(g) = SO2(g)+ H2O(l) ΔH = -586 kJ·mol-1。
下列说法错误的是
②2SO2(g) + O2(g)
 2SO3(g) ΔH = -196.6 kJ·mol-1;
2SO3(g) ΔH = -196.6 kJ·mol-1; ③H2S(g) +
 O2(g) = SO2(g)+ H2O(l) ΔH = -586 kJ·mol-1。
O2(g) = SO2(g)+ H2O(l) ΔH = -586 kJ·mol-1。下列说法错误的是
| A.硫的燃烧热是394.3 kJ·mol-1 |
| B.由盖斯定律可得出热化学方程式:2H2S(g) + SO2(g) = 3S(s) + 2H2O(l) ΔH = -284 kJ·mol-1 |
| C.S(g)+O2(g)= SO2(g) ΔH < -296 kJ·mol -1 |
| D.在一定条件下,将1 mol SO2(g)与0.5 mol O2(g)放入一 密闭容器中充分反应,放出的热量小于98.3 kJ |
您最近一年使用:0次
2022-02-18更新
|
505次组卷
|
4卷引用:云南省昭通市永善、绥江县2021-2022学年高二3月月考化学试题
9 . 在下列各说法中,正确的是
| A.热化学方程式中的化学计量数可以是分数 | B. 表示放热反应, 表示放热反应, 表示吸热反应 表示吸热反应 |
C. 的大小与热化学方程式中的计量数无关 的大小与热化学方程式中的计量数无关 | D.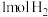 与 与 反应放出的热就是 反应放出的热就是 的燃烧热 的燃烧热 |
您最近一年使用:0次
2021-10-25更新
|
168次组卷
|
2卷引用:云南省昭通市镇雄县第四中学2021-2022学年高二上学期第一次月考化学试题
解题方法
10 . 下列说法或表示方法中正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.由C(金刚石)→C(石墨);ΔH=-119KJ/mol 可知,金刚石比石墨稳定 |
| C.在101Kpa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);ΔH=285.8KJ/mol |
| D.CH4(g)+2O2(g)=CO2(g)+2H2O(l),∆H= -890kJ·mol-1 说明破坏1mol CH4(g)和2 mol O2(g)的化学键所需要能量小于破坏1mol CO2(g)和2 mol H2O(l) 的化学键所需要能量 |
您最近一年使用:0次
2021-04-12更新
|
184次组卷
|
2卷引用:云南省砚山县第三高级中学2020-2021学年高二下学期期中考试化学试题



