2023高三·全国·专题练习
名校
解题方法
1 . 回答下列问题。
(1)用NH3可以消除氮氧化物的污染,已知:
反应Ⅰ:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH1=a kJ·mol-1
2N2(g)+6H2O(g) ΔH1=a kJ·mol-1
反应Ⅱ:N2(g)+O2(g) 2NO(g) ΔH2=b kJ·mol-1
2NO(g) ΔH2=b kJ·mol-1
反应Ⅲ:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH3=c kJ·mol-1
5N2(g)+6H2O(g) ΔH3=c kJ·mol-1
则反应Ⅱ中的b=___________ (用含a、c的代数式表示),反应Ⅲ中的ΔS___________ (填“>”“<”或“=”)0。
(2)已知:①2CO(g)+SO2(g) S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
②2H2(g)+SO2(g) S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
③CO的燃烧热ΔH3=-283 kJ·mol-1,
请回答:
表示液态硫(S)的燃烧热的热化学方程式为___________ ;反应②中,正反应活化能E1___________ (填“>”“<”或“=”)ΔH2。
(3)若某温度下,CH3COOH(aq)与NaOH(aq)反应的ΔH=-46.8 kJ·mol-1,H2SO4(aq)与NaOH(aq)的中和热为57.3 kJ·mol-1,则CH3COOH在水溶液中电离的反应热ΔH1=___________ 。
(4)已知:
则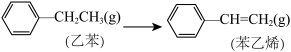 +H2(g) ΔH=
+H2(g) ΔH=___________ ;又知H2和苯乙烯的燃烧热ΔH分别为-290 kJ·mol-1和-4400 kJ·mol-1,则乙苯的燃烧热ΔH=___________ kJ·mol-1。
(1)用NH3可以消除氮氧化物的污染,已知:
反应Ⅰ:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔH1=a kJ·mol-1
2N2(g)+6H2O(g) ΔH1=a kJ·mol-1反应Ⅱ:N2(g)+O2(g)
 2NO(g) ΔH2=b kJ·mol-1
2NO(g) ΔH2=b kJ·mol-1反应Ⅲ:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) ΔH3=c kJ·mol-1
5N2(g)+6H2O(g) ΔH3=c kJ·mol-1则反应Ⅱ中的b=
(2)已知:①2CO(g)+SO2(g)
 S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1②2H2(g)+SO2(g)
 S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1③CO的燃烧热ΔH3=-283 kJ·mol-1,
请回答:
表示液态硫(S)的燃烧热的热化学方程式为
(3)若某温度下,CH3COOH(aq)与NaOH(aq)反应的ΔH=-46.8 kJ·mol-1,H2SO4(aq)与NaOH(aq)的中和热为57.3 kJ·mol-1,则CH3COOH在水溶液中电离的反应热ΔH1=
(4)已知:
| 化学键 | C—H | C—C | C=C | H—H |
| 键能/(kJ·mol-1) | 412 | 348 | 612 | 436 |
 +H2(g) ΔH=
+H2(g) ΔH=
您最近半年使用:0次
22-23高二上·河南周口·期末
2 . 化学反应中的热效应又称反应热,包括燃烧热、中和热等,其数据广泛应用于科学研究和工业生产方面。
(1)若 石墨完全燃烧放出的热量为
石墨完全燃烧放出的热量为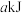 ,则石墨完全燃烧的热化学方程式为
,则石墨完全燃烧的热化学方程式为___________ 。
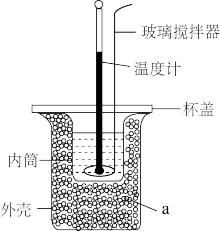
(2)利用如图所示装置测定中和反应的反应热的实验步骤如下:①用量筒量取 盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取
盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取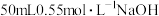 溶液,测出
溶液,测出 溶液温度;③将
溶液温度;③将 溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。装置中a的作用是
溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。装置中a的作用是___________ ,上述实验步骤中一处不合理的操作应改成___________ 。假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容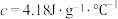 。测得溶液的温度依次为20.1℃、20.3℃、23.4℃,可计算出中和反应的反应热
。测得溶液的温度依次为20.1℃、20.3℃、23.4℃,可计算出中和反应的反应热
___________  (保留三位有效数字)。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热
(保留三位有效数字)。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热
___________ (“偏大”“偏小”或“相等”)。
(3)键能指 气态分子解离为气态原子所需的能量。已知
气态分子解离为气态原子所需的能量。已知 ,其中H—H、O=O、O—H的键能依次为
,其中H—H、O=O、O—H的键能依次为 、
、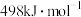 、
、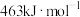 ,又知
,又知
 ,则氢气的燃烧热
,则氢气的燃烧热
___________ 。
(1)若
 石墨完全燃烧放出的热量为
石墨完全燃烧放出的热量为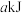 ,则石墨完全燃烧的热化学方程式为
,则石墨完全燃烧的热化学方程式为(2)利用如图所示装置测定中和反应的反应热的实验步骤如下:①用量筒量取
 盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取
盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取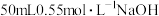 溶液,测出
溶液,测出 溶液温度;③将
溶液温度;③将 溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。装置中a的作用是
溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。装置中a的作用是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容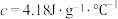 。测得溶液的温度依次为20.1℃、20.3℃、23.4℃,可计算出中和反应的反应热
。测得溶液的温度依次为20.1℃、20.3℃、23.4℃,可计算出中和反应的反应热
 (保留三位有效数字)。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热
(保留三位有效数字)。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热

(3)键能指
 气态分子解离为气态原子所需的能量。已知
气态分子解离为气态原子所需的能量。已知 ,其中H—H、O=O、O—H的键能依次为
,其中H—H、O=O、O—H的键能依次为 、
、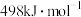 、
、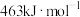 ,又知
,又知
 ,则氢气的燃烧热
,则氢气的燃烧热
您最近半年使用:0次
3 . 能源是国民经济发展的重要基础。请根据所学知识回答下列问题:
Ⅰ.在标准状况下,1.68L家用燃料(仅由C、H两种元素组成的某气体)质量为1.2g,在25℃和101kPa下完全燃烧生成 和
和 时,放出66.77kJ的热量。
时,放出66.77kJ的热量。
(1)该气体的分子式为___________ 。该气体的燃烧热
___________ 。(保留一位小数)
Ⅱ.火箭发射时可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。
和水蒸气。
已知:
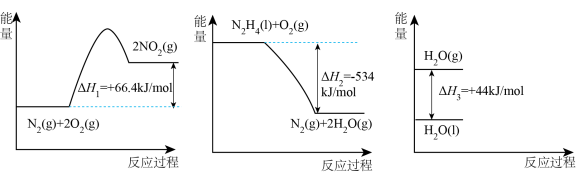
(2)请写出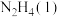 与
与 反应的热化学方程式
反应的热化学方程式___________ 。
(3)32g液态肼与足量 反应生成氮气和液态水时,放出的热量是
反应生成氮气和液态水时,放出的热量是___________ kJ。
(4)上述反应用于火箭推进器的原因:①能快速产生大量气体;②___________ 。
Ⅲ.氢能是一种极具发展潜力的清洁能源。 可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
已知:在25℃、101kPa下,
①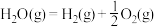
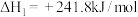
②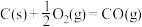
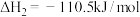
③

(5)25℃、101kPa下,CO与水蒸气反应转化为 和
和 的热化学方程式为
的热化学方程式为___________ 。
Ⅰ.在标准状况下,1.68L家用燃料(仅由C、H两种元素组成的某气体)质量为1.2g,在25℃和101kPa下完全燃烧生成
 和
和 时,放出66.77kJ的热量。
时,放出66.77kJ的热量。(1)该气体的分子式为

Ⅱ.火箭发射时可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。
和水蒸气。已知:

(2)请写出
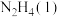 与
与 反应的热化学方程式
反应的热化学方程式(3)32g液态肼与足量
 反应生成氮气和液态水时,放出的热量是
反应生成氮气和液态水时,放出的热量是(4)上述反应用于火箭推进器的原因:①能快速产生大量气体;②
Ⅲ.氢能是一种极具发展潜力的清洁能源。
 可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一已知:在25℃、101kPa下,
①
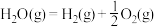
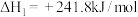
②
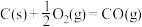
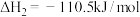
③


(5)25℃、101kPa下,CO与水蒸气反应转化为
 和
和 的热化学方程式为
的热化学方程式为
您最近半年使用:0次
22-23高三下·浙江·阶段练习
解题方法
4 .  ,有关物质的能量转化图如图,又已知
,有关物质的能量转化图如图,又已知 是
是 的稳定氧化物,试分析计算并回答下列说法不正确的是
的稳定氧化物,试分析计算并回答下列说法不正确的是

 ,有关物质的能量转化图如图,又已知
,有关物质的能量转化图如图,又已知 是
是 的稳定氧化物,试分析计算并回答下列说法不正确的是
的稳定氧化物,试分析计算并回答下列说法不正确的是
A. 时,单质 时,单质 的标准燃烧热: 的标准燃烧热: |
B.若 的摩尔质量为 的摩尔质量为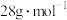 ,则 ,则 的热值为 的热值为 |
C.转化Ⅱ的热化学方程式为: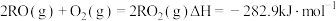 |
D.由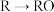 的热化学方程式为: 的热化学方程式为: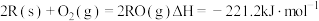 |
您最近半年使用:0次
2023高三·全国·专题练习
解题方法
5 . 已知水的比热容为4.18×10-3kJ•(g•℃)-1,10g硫磺在O2中完全燃烧生成气态SO2,放出的热量能量使500gH2O温度由18℃升至62.4℃,则硫磺的燃烧热为___________ ,热化学方程式为___________ 。
您最近半年使用:0次
2022高二·上海·专题练习
解题方法
6 . 在常温常压时,充分燃烧一定量的丁烷(C4H10)气体,放出热量QkJ(Q>0),将生成的二氧化碳全部通入足量NaOH溶液中,发生的反应为CO2+2NaOH=Na2CO3+H2O,共消耗了4mol·L-1的NaOH溶液200mL。则此条件下,下列热化学方程式正确的是
A.C4H10(g)+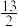 O2(g)=4CO2(g)+5H2O(l) ΔH=-QkJ·mol-1 O2(g)=4CO2(g)+5H2O(l) ΔH=-QkJ·mol-1 |
B.C4H10(g)+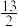 O2(g)=4CO2(g)+5H2O(l) ΔH=-10QkJ·mol-1 O2(g)=4CO2(g)+5H2O(l) ΔH=-10QkJ·mol-1 |
C.C4H10(g)+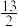 O2(g)=4CO2(g)+5H2O(l) ΔH=10QkJ·mol-1 O2(g)=4CO2(g)+5H2O(l) ΔH=10QkJ·mol-1 |
D.C4H10(g)+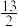 O2(g)=4CO2(g)+5H2O(l) ΔH=-10QkJ O2(g)=4CO2(g)+5H2O(l) ΔH=-10QkJ |
您最近半年使用:0次
20-21高二下·青海海东·阶段练习
名校
7 . 用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
(1)H2的燃烧热ΔH=_________ 。
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为_________ g。
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为__________ 。
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+
 O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1(1)H2的燃烧热ΔH=
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
您最近半年使用:0次
2021·河北秦皇岛·二模
8 . 已知25℃、101kPa下,1mol水蒸发为水蒸气需要吸热44.0kJ
①H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ•mol-1
②2CH3OH(l)+3O2(g)=4H2O(g)+2CO2(g)△H2=-1277.0kJ•mol-1
下列有关说法错误的是
①H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ•mol-1
②2CH3OH(l)+3O2(g)=4H2O(g)+2CO2(g)△H2=-1277.0kJ•mol-1
下列有关说法错误的是
| A.若反应②中CH3OH变为气态,则该反应的反应热△H>△H2 |
| B.CH3OH(l)的燃烧热△H=-726.5kJ•mol-1 |
| C.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)△H>﹣57.3kJ•mol-1 |
| D.液态水变为水蒸气过程中需要克服分子间作用力 |
您最近半年使用:0次
2021-04-13更新
|
630次组卷
|
6卷引用:押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)
(已下线)押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)(已下线)第17讲 化学能与热能(精讲)-2022年一轮复习讲练测(已下线)第03讲 盖斯定律(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)河北省秦皇岛市2021届普通高中学业水平选择性考试第二次模拟演练化学试题河南省商城县观庙高级中学2021-2022学年高二上学期12月月考化学试题江西省九校2022-2023学年高二下学期开学联考化学试题
20-21高二上·江西南昌·期末
名校
解题方法
9 . 下列化学用语的有关表达不正确的是
①甲烷的球棍模型
②苯乙烯(C8H8)的比例模型可以表示为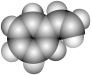
③-CH3与-OH、NH 具有相同质子数
具有相同质子数
④因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)=2H2(g)+O2(g) △H=+c kJ·mol-1
⑤因CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H= +b kJ·mol-1,故1 mol CuSO4(s)溶于水时,放出的热量为b kJ
①甲烷的球棍模型

②苯乙烯(C8H8)的比例模型可以表示为

③-CH3与-OH、NH
 具有相同质子数
具有相同质子数④因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)=2H2(g)+O2(g) △H=+c kJ·mol-1
⑤因CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H= +b kJ·mol-1,故1 mol CuSO4(s)溶于水时,放出的热量为b kJ
| A.②③④⑤ | B.①④⑤ | C.①③⑤ | D.②④⑤ |
您最近半年使用:0次
2021-02-05更新
|
394次组卷
|
3卷引用:专题08 化学反应与能量-备战2021届高考化学二轮复习题型专练
(已下线)专题08 化学反应与能量-备战2021届高考化学二轮复习题型专练江西师范大学附属中学2020-2021学年高二上学期期末考试化学试题江西省师范大学附属中学2021-2022学年高二上学期期末化学试题
20-21高二上·湖北咸宁·期末
名校
解题方法
10 . 已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.6kJ·mol-1。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的图示与过程如下:
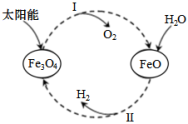
过程I:……
过程II:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol﹣1
下列说法错误的是

过程I:……
过程II:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol﹣1
下列说法错误的是
| A.该过程I能量转化形式是太阳能→化学能 |
B.过程I热化学方程式为:Fe3O4(s)=3FeO(s)+ O2(g) ΔH=﹣156.6kJ·mol﹣1 O2(g) ΔH=﹣156.6kJ·mol﹣1 |
| C.氢气的燃烧热为ΔH=﹣285.8 kJ·mol﹣1 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近半年使用:0次
2021-02-02更新
|
325次组卷
|
4卷引用:考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)湖北省咸宁市通城二中2020-2021学年高二上学期期末考试化学试题云南省下关第一中学2022-2023学年高二下学期5月期中考试化学试题



