1 . 已知25℃、101kPa下,1mol水蒸发为水蒸气需要吸热44.0kJ
①H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ•mol-1
②2CH3OH(l)+3O2(g)=4H2O(g)+2CO2(g)△H2=-1277.0kJ•mol-1
下列有关说法错误的是
①H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ•mol-1
②2CH3OH(l)+3O2(g)=4H2O(g)+2CO2(g)△H2=-1277.0kJ•mol-1
下列有关说法错误的是
| A.若反应②中CH3OH变为气态,则该反应的反应热△H>△H2 |
| B.CH3OH(l)的燃烧热△H=-726.5kJ•mol-1 |
| C.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)△H>﹣57.3kJ•mol-1 |
| D.液态水变为水蒸气过程中需要克服分子间作用力 |
您最近一年使用:0次
2021-04-13更新
|
637次组卷
|
6卷引用:押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)
(已下线)押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)(已下线)第17讲 化学能与热能(精讲)-2022年一轮复习讲练测河北省秦皇岛市2021届普通高中学业水平选择性考试第二次模拟演练化学试题河南省商城县观庙高级中学2021-2022学年高二上学期12月月考化学试题(已下线)第03讲 盖斯定律(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)江西省九校2022-2023学年高二下学期开学联考化学试题
名校
解题方法
2 . 下列化学用语的有关表达不正确的是
①甲烷的球棍模型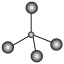
②苯乙烯(C8H8)的比例模型可以表示为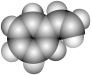
③-CH3与-OH、NH 具有相同质子数
具有相同质子数
④因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)=2H2(g)+O2(g) △H=+c kJ·mol-1
⑤因CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H= +b kJ·mol-1,故1 mol CuSO4(s)溶于水时,放出的热量为b kJ
①甲烷的球棍模型

②苯乙烯(C8H8)的比例模型可以表示为

③-CH3与-OH、NH
 具有相同质子数
具有相同质子数④因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)=2H2(g)+O2(g) △H=+c kJ·mol-1
⑤因CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H= +b kJ·mol-1,故1 mol CuSO4(s)溶于水时,放出的热量为b kJ
| A.②③④⑤ | B.①④⑤ | C.①③⑤ | D.②④⑤ |
您最近一年使用:0次
2021-02-05更新
|
394次组卷
|
3卷引用:专题08 化学反应与能量-备战2021届高考化学二轮复习题型专练
(已下线)专题08 化学反应与能量-备战2021届高考化学二轮复习题型专练江西师范大学附属中学2020-2021学年高二上学期期末考试化学试题江西省师范大学附属中学2021-2022学年高二上学期期末化学试题
名校
解题方法
3 . 已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.6kJ·mol-1。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的图示与过程如下:
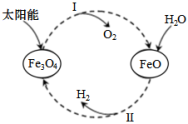
过程I:……
过程II:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol﹣1
下列说法错误的是

过程I:……
过程II:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol﹣1
下列说法错误的是
| A.该过程I能量转化形式是太阳能→化学能 |
B.过程I热化学方程式为:Fe3O4(s)=3FeO(s)+ O2(g) ΔH=﹣156.6kJ·mol﹣1 O2(g) ΔH=﹣156.6kJ·mol﹣1 |
| C.氢气的燃烧热为ΔH=﹣285.8 kJ·mol﹣1 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近一年使用:0次
2021-02-02更新
|
325次组卷
|
4卷引用:考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)湖北省咸宁市通城二中2020-2021学年高二上学期期末考试化学试题云南省下关第一中学2022-2023学年高二下学期5月期中考试化学试题
名校
解题方法
4 . 填空
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石___ (填“>”或“<”)石墨。
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1____ (填“>”或“<”)ΔH2。
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:________ 。
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=____ 。
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=______ 。
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是________ 。
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是
您最近一年使用:0次
2020-12-15更新
|
319次组卷
|
6卷引用:第六章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测
(已下线)第六章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)专题18 化学反应与能量(限时精练)-2022年高三毕业班化学常考点归纳与变式演练重庆市沙坪坝实验中学校2021-2022学年高二上学期12月月考化学试题2015届四川省成都郫县高三第二次阶诊断性考试理综化学试卷河北省安平中学2017-2018学年高一下学期期末考试化学试题1贵州省毕节市七星关区毕节市实验高级中学2020-2021学年高二上学期期中考试化学试题
13-14高二上·河南漯河·期中
名校
5 . 已知下列两个热化学方程式:
2H2(g)+O2(g)==2H2O(l) △H =-571.6kJ•mol-1
C3H8(g) +5O2(g)==3CO2(g) +4H2O(l) △H=-2220.0kJ•mol-1
实验测得氢气和丙烷的混和气体共5mol完全燃烧时放热3847kJ,则混和气体中氢气与丙烷的体积比是( )
2H2(g)+O2(g)==2H2O(l) △H =-571.6kJ•mol-1
C3H8(g) +5O2(g)==3CO2(g) +4H2O(l) △H=-2220.0kJ•mol-1
实验测得氢气和丙烷的混和气体共5mol完全燃烧时放热3847kJ,则混和气体中氢气与丙烷的体积比是( )
| A.1:3 | B.3:1 | C.1:4 | D.1:1 |
您最近一年使用:0次
2019-10-05更新
|
428次组卷
|
17卷引用:专题讲座(一) 化学计算的常用方法(精讲)-2022年一轮复习讲练测
(已下线)专题讲座(一) 化学计算的常用方法(精讲)-2022年一轮复习讲练测河北省藁城新冀明中学2021-2022学年高二上学期10月月考化学试题(已下线)专题讲座(一) 化学计算的常用方法(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)2013-2014学年河南省漯河市高二上学期期中考试化学试卷(已下线)2014秋季湖南省浏阳一中高二上学期第一次阶段测试化学(B)试题2014-2015学年云南省富民县一中高二上学期期中化学试卷2015-2016学年内蒙古巴彦淖尔高二上10月月考化学试卷2015-2016学年山东省桓台二中高二下期末化学试卷2016-2017学年天津市河东区高二上学期期中质检化学试卷陕西省西安市电子科技中学2017-2018学年高二上学期第一次月考化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题A内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题B湖南辰溪博雅实验学校2018-2019学年高二8月月考化学试题广东省深圳市耀华实验学校2018-2019学年高二上学期第一次月考化学试题甘肃省武威第一中学2019-2020学年高二10月月考化学试题江西省南城县第二中学2018-2019学年高二上学期第二次月考化学试题新疆乌鲁木齐市第四中学2019-2020学年高二上学期期中考试化学试题
6 . 油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)。已知燃烧1kg该化合物释放出热量3.8×104kJ。油酸甘油酯的燃烧热△H为
| A.3.8×104kJ·mol-1 | B.-3.8×104kJ·mol-1 |
| C.3.4×104kJ·mol-1 | D.-3.4×104kJ·mol-1 |
您最近一年使用:0次
2016-07-11更新
|
2811次组卷
|
34卷引用:课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)(已下线)《考前20天终极攻略》-5月24日 盖斯定律及反应热的有关计算(已下线)解密08 化学反应与热能(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点(已下线)2019年高考总复习巅峰冲刺-专题05 化学反应中的能量变化应试策略2020届高三化学二轮冲刺新题专练——燃烧热的定义与应用(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训(已下线)1.2 反应热的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)黑龙江省哈尔滨市第一六二中学2021-2022学年高三上学期第三次月考化学试题(已下线)第六章 化学反应与能量 第34讲 反应热的计算2016年全国普通高等学校招生统一考试化学(海南卷精编版)2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷2016-2017学年河北冀州市中学高二上开学调研化学卷2017届河北省沧州市第一中学高三上周测化学试卷2016-2017学年广东省仲元中学高二上学期期末考试化学(理)试卷湖北省新洲一中、黄陂一中、麻城一中2017-2018学年高二上学期期中联考化学试题安徽省合肥八中、马鞍山二中、阜阳一中2017-2018学年第一学期联考高二化学试卷福建省泉州市泉港区第一中学2017-2018学年高二年上学期期末考化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期10月模块诊断化学试题2016年全国普通高等学校招生统一考试化学(海南卷参考版)海南省文昌中学2019-2020学年高二上学期第二次月考化学试题湖南省师范大学附属中学2020届高三上学期第二次月考化学试题山西省大同市天镇县第一中学校2019-2020学年高二上学期第二次月考化学试题安徽省定远县育才学校2019-2020学年高二4月月考化学试题河南省郑州市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分天津市南开中学2020届高三教学质量监测理科综合化学部分人教版(2019)高二选择性必修第一册 第一章 化学反应的热效应 第一节 反应热 高考帮广东省揭阳市第三中学2020-2021学年高二上学期期中考化学试题海南省八所中学2020届高三上学期期末考试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题第一章 化学反应的热效应 第一节 反应热 第2课时 热化学方程式 燃烧热湖北省武汉市第三中学2023-2024学年高一下学期3月月考化学试卷



