名校
1 . 过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气、器材的消毒,可由乙酸与H2O2在硫酸催化下反应制得,热化学方程式为:CH3COOH(aq)+H2O2(aq) CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
(1)利用上述反应制备760g CHCOH,放出的热量为_______ kJ。
(2)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
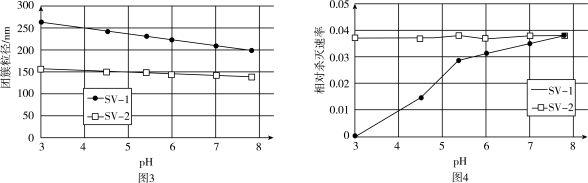
实验2:在不同温度下反应(反应均未达到平衡),测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
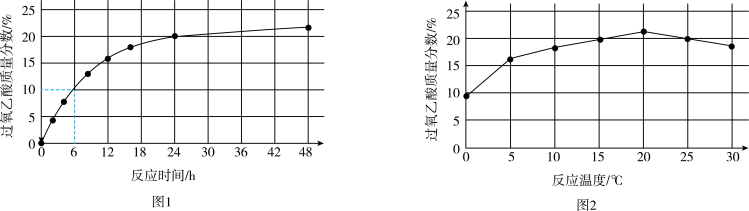 ①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=
①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=_____ g/h。(用含m的代数式表示)
②综合图1、图2分析,与20℃相比,25℃时过氧乙酸产率降低的可能原因是_______ (写出2条)。
(3)SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40nm和70nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是___________ 。
 CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol(1)利用上述反应制备760g CHCOH,放出的热量为
(2)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应(反应均未达到平衡),测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
 ①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=
①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=②综合图1、图2分析,与20℃相比,25℃时过氧乙酸产率降低的可能原因是
(3)SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40nm和70nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。

依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是
您最近一年使用:0次
2 . 已知碳酸钙分解的热化学方程式为:
 ,欲使1t
,欲使1t 完全分解,需要提供多少热
完全分解,需要提供多少热_______ ?若通过煤炭燃烧来提供热,则至少需要燃烧____ 千克煤炭?(已知煤炭的热值为 )
)

 ,欲使1t
,欲使1t 完全分解,需要提供多少热
完全分解,需要提供多少热 )
)
您最近一年使用:0次
3 . 乙炔( )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
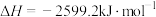 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热__________ ?

 )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
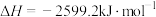 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热
您最近一年使用:0次
名校
4 . 1g正丁烷(C4H10)燃烧生成CO2和液态的水,放出49.6KJ热量,则其热化学方程式为
| A.2C4H10+13O2=8CO2+10H2O;△H=-5753.6KJ/mol |
| B.2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l);△H=-49.6KJ/mol |
| C.2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l);△H=-2876.8KJ/mol |
| D.C4H10(g)+13/2O2(g)=4CO2(g)+5H2O(l);△H=-2876.8KJ/mol |
您最近一年使用:0次
2022-10-31更新
|
73次组卷
|
2卷引用:广东省揭阳市惠来县第一中学2021-2022学年高二上学期第一次阶段考试化学试题
5 . 下列关于热化学反应的描述中正确的是
A. 和NaOH反应生成1mol水时,反应放出热量为57.3kJ 和NaOH反应生成1mol水时,反应放出热量为57.3kJ |
| B.需要加热才能发生的反应一定是吸热反应 |
C.由 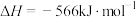 ,知CO的燃烧热为 ,知CO的燃烧热为 |
D.已知 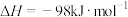 ,则 ,则 的燃烧热为 的燃烧热为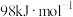 |
您最近一年使用:0次
名校
6 . 家用液化气中主要成分之一是丁烷。在101kPa时,10kg丁烷完全燃烧生成CO2和H2O,放出热量5×105kJ,丁烷的燃烧热为___________ 。
您最近一年使用:0次
名校
7 . Ⅰ.当今社会,能源的发展已成为全世界共同关注的话题,乙烷、二甲醚的燃烧热较大,可用作燃料。如图1表示乙烷、二甲醚燃烧过程中的能量变化。

请回答下列问题:
(1)a=__ 。
(2)乙烷的燃烧热为__ 。
(3)根据题图写出二甲醚完全燃烧时的热化学方程式:__ 。
Ⅱ.利用如图2装置测定中和热的实验步骤如下:

①用量筒量取50mL0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL0.55mol/LNaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(4)大小烧杯中填充泡沫塑料的作用是__ 。
(5)倒入NaOH溶液的正确操作是__ (从下列选出)。
A.一次迅速倒入 B.分三次少量倒入 C.沿玻璃棒缓慢倒入
(6)使硫酸与NaOH溶液混合均匀的正确操作是__ 。

请回答下列问题:
(1)a=
(2)乙烷的燃烧热为
(3)根据题图写出二甲醚完全燃烧时的热化学方程式:
Ⅱ.利用如图2装置测定中和热的实验步骤如下:

①用量筒量取50mL0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL0.55mol/LNaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(4)大小烧杯中填充泡沫塑料的作用是
(5)倒入NaOH溶液的正确操作是
A.一次迅速倒入 B.分三次少量倒入 C.沿玻璃棒缓慢倒入
(6)使硫酸与NaOH溶液混合均匀的正确操作是
您最近一年使用:0次
解题方法
8 . 按要求填空
(1)Cr2O 的颜色是
的颜色是___________ 。
(2)已知:16.0g甲烷气体完全燃烧生成液态水放出的热量为890.3kJ(298K、1.01×105Pa时测定)。写出该条件下,甲烷燃烧的热化学方程式___________ 。
(1)Cr2O
 的颜色是
的颜色是(2)已知:16.0g甲烷气体完全燃烧生成液态水放出的热量为890.3kJ(298K、1.01×105Pa时测定)。写出该条件下,甲烷燃烧的热化学方程式
您最近一年使用:0次
9 . 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①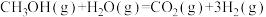

②
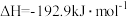
下列说法正确的是
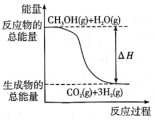
①
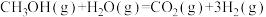

②

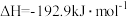
下列说法正确的是

| A.反应①中的能量变化如上图所示 |
B. 的燃烧热为 的燃烧热为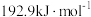 |
C.根据②推知反应 的 的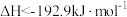 |
D. 转变成 转变成 的过程不一定要吸收能量 的过程不一定要吸收能量 |
您最近一年使用:0次
10 . 下列热化学方程式正确的是
| A.已知H2(g)的燃烧热是285.8kJ•mol-1,则2H2O(g)=2H2(g)+O2(g) △H=+571.6kJ•mol-1 |
| B.已知中和热为57.3kJ•mol-1,则HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) △H=+57.3kJ•mol-1 |
| C.已知ag乙烯气体充分燃烧时生成1molCO2和液态水,放出bkJ的热量,则表示乙烯燃烧热的热化学方程式为:2C2H4(g)+6O2(g)=4CO2(g)+4H2O(l) △H=-4bkJ•mol-1 |
| D.已知4g硫粉在氧气中完全燃烧生成SO2气体,放出37kJ的热量,则硫燃烧的热化学方程式为:S(s)+O2(g)=SO2(g) △H=-296kJ•mol-1 |
您最近一年使用:0次



