名校
解题方法
1 . 以N2O5为新型硝化剂的硝化反应具有反应条件温和、选择性高、无副反应发生、过程无污染等优点。N2O5可通过N2O4臭氧化法制备。
已知:①N2O4(g) 2NO2(g) ΔH1
2NO2(g) ΔH1
②2O3(g)=3O2(g) ΔH2
③2N2O5(s)=4NO2(g)+O2(g) ΔH3
则N2O4(g)+O3(g) N2O5(s)+O2(g)的ΔH为
N2O5(s)+O2(g)的ΔH为
已知:①N2O4(g)
 2NO2(g) ΔH1
2NO2(g) ΔH1②2O3(g)=3O2(g) ΔH2
③2N2O5(s)=4NO2(g)+O2(g) ΔH3
则N2O4(g)+O3(g)
 N2O5(s)+O2(g)的ΔH为
N2O5(s)+O2(g)的ΔH为A.ΔH1+ΔH2- ΔH3 ΔH3 | B.2ΔH1-ΔH2+ΔH3 |
C.ΔH1+ ΔH2- ΔH2- ΔH3 ΔH3 | D.2ΔH1+ ΔH2+ ΔH2+ ΔH3 ΔH3 |
您最近一年使用:0次
2023-10-12更新
|
445次组卷
|
3卷引用:辽宁省辽东教学共同体2023-2024学年高二上学期10月月考化学试题
2 . 盖斯定律是化学热力学发展的基础,下列不能应用盖斯定律解决的问题是
| A.比较Al与Fe燃烧热的大小 |
| B.比较CH3OH与CH4燃烧热大小 |
| C.比较S(s)与S(g)在空气中燃烧的热效应大小 |
| D.比较氢氧化钠分别与盐酸和氢氟酸中和反应的热效应大小 |
您最近一年使用:0次
2023-10-12更新
|
332次组卷
|
4卷引用:辽宁省辽东教学共同体2023-2024学年高二上学期10月月考化学试题
3 . 下列说法正确的是
已知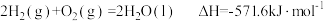
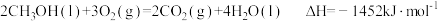
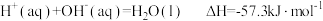
已知
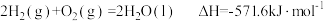
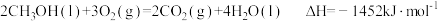
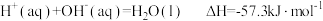
| A.H2(g)的燃烧热ΔH=-571.6kJ•mol-1 |
B.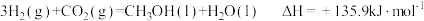 |
C.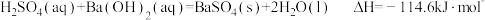 |
| D.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
您最近一年使用:0次
2023-10-05更新
|
63次组卷
|
2卷引用:江苏省常州市前黄高级中学2022-2023学年高二上学期第二次阶段考试化学试题
名校
解题方法
4 . 已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0 kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
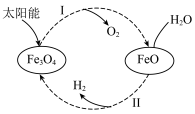
| A.过程Ⅰ中每消耗232 g Fe3O4转移2 mol电子 |
| B.过程Ⅱ的热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+128.9 kJ/mol |
| C.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近一年使用:0次
2023-09-19更新
|
355次组卷
|
25卷引用:【区级联考】北京市石景山区2019届高三第一学期期末考试化学试题
【区级联考】北京市石景山区2019届高三第一学期期末考试化学试题辽宁省锦州市滨海实验中学2019-2020学年高三上学期期末考试化学试题海南省海南中学2019-2020学年高二上学期期末考试化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题10-2020年北京新高考化学模拟试题(已下线)专题九 化学能与热能(提分特训)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训甘肃省天水市甘谷第一中学2019-2020学年高二下学期开学考试化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1节综合训练高中必刷题高二选择性必修1第一章 化学反应的热效应 第二节 反应热的计算 第二节综合训练河北省沧州市泊头市第一中学2020-2021学年高二上学期第一次月考化学试题山东省德州市夏津第一中学2020-2021学年高二上学期9月月考化学试题辽源市第五中学2019-2020学年高一下学期第二次月考化学试题湖南省中方一中2020-2021学年高二上学期期中考试化学试题河北省沧州市黄骅中学2020-2021学年高二上学期第三次月考化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研二化学试题河北省安平中学2020-2021学年高一下学期第四次月考(期末)化学试题(已下线)模块七 化学反应与能量(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)贵州省黔西南州赛文高级中学 2021-2022学年高二上学期期中考试化学试题河北省沧州市泊头市第一中学2021-2022学年高二上学期第一次月考化学试题天津市第二中学2022-2023学年高二上学期期中检测化学试题(已下线)第七章 化学反应速率与化学平衡 热点强化12 化学反应历程、机理的分析应用(已下线)题型98 结合反应能量图示或物质循环图示书写热化学方程式山东省烟台市招远第一中学2022-2023学年高一下学期期中考试化学(等级考)试题(已下线)章末综合评价(六)河南省洛阳市宜阳县第一高级中学清北园2023-2024学年高一上学期第七次能力达标测试化学试卷
5 . 由金属镁和氧气生成氧化镁的相关反应及其热效应(kJ·mol⁻¹)如下图所示。由此可判断ΔH 等于


| A.725 kJ∙mol−1 | B.−725 kJ∙mol−1 | C.1929 kJ∙mol−1 | D.−1929 kJ∙mol−1 |
您最近一年使用:0次
6 . 根据能量变化示意图得出的结论正确的是


| A.1 mol C完全燃烧生成CO2时放出的热量为393.5 kJ |
| B.2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol |
| C.2CO2(g)=2CO(g)+O2(g) ΔH=+283.0 kJ/mol |
| D.C(s)+O2(g)=CO2(g) ΔH=+393.5 kJ/mol |
您最近一年使用:0次
7 . 假定反应体系的始态为s,终态为l,它们之间变化如图所示:s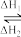 l,则下列说法不正确的是
l,则下列说法不正确的是
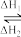 l,则下列说法不正确的是
l,则下列说法不正确的是| A.若ΔH1<0,则ΔH2>0 | B.若ΔH1<0,则ΔH2<0 |
| C.ΔH1和ΔH2的绝对值相等 | D.ΔH1+ΔH2=0 |
您最近一年使用:0次
名校
8 . 已知①H2(g)+ O2(g)=H2O(g) ΔH1=a kJ·mol-1
O2(g)=H2O(g) ΔH1=a kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH2=b kJ·mol-1
③H2(g)+ O2(g)=H2O(l) ΔH3=c kJ·mol-1
O2(g)=H2O(l) ΔH3=c kJ·mol-1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol-1
下列关系式正确的是
 O2(g)=H2O(g) ΔH1=a kJ·mol-1
O2(g)=H2O(g) ΔH1=a kJ·mol-1②2H2(g)+O2(g)=2H2O(g) ΔH2=b kJ·mol-1
③H2(g)+
 O2(g)=H2O(l) ΔH3=c kJ·mol-1
O2(g)=H2O(l) ΔH3=c kJ·mol-1④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol-1
下列关系式正确的是
| A.a<c<0 | B.b>d>0 |
| C.2a=b<0 | D.2c=d>0 |
您最近一年使用:0次
2023-08-26更新
|
722次组卷
|
3卷引用:第3课时 反应焓变的计算
9 . 回答下列问题
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1___________ ΔH2(填“>”“<”或“=”,下同)。
(2)相同条件下,2 mol氢原子所具有的能量___________ 1 mol 氢分子所具有的能量。
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1___________ ΔH2。
①P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1,
②4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2。
(4)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量___________ 57.3 kJ。
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1
(2)相同条件下,2 mol氢原子所具有的能量
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1
①P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1,
②4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2。
(4)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量
您最近一年使用:0次
10 . 下列各组热化学方程式中,化学反应的ΔH前者大于后者的是
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH1;2H2S(g)+O2(g)=2S(s)+2H2O(l) ΔH2
②S(s)+O2(g)=SO2(g) ΔH3;S(g)+O2(g)=SO2(g) ΔH4
③NH3·H2O(aq)+H+(aq)=NH (aq)+H2O(l) ΔH5;H+(aq)+OH-(aq)=H2O(l) ΔH6
(aq)+H2O(l) ΔH5;H+(aq)+OH-(aq)=H2O(l) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7;CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH1;2H2S(g)+O2(g)=2S(s)+2H2O(l) ΔH2
②S(s)+O2(g)=SO2(g) ΔH3;S(g)+O2(g)=SO2(g) ΔH4
③NH3·H2O(aq)+H+(aq)=NH
 (aq)+H2O(l) ΔH5;H+(aq)+OH-(aq)=H2O(l) ΔH6
(aq)+H2O(l) ΔH5;H+(aq)+OH-(aq)=H2O(l) ΔH6④CaCO3(s)=CaO(s)+CO2(g) ΔH7;CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
| A.②③④ | B.④ | C.① | D.①②③ |
您最近一年使用:0次



