1 . 已知胆矾晶体相关的焓变如图所示,则 为
为
 为
为
A.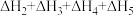 | B.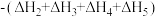 |
C.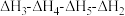 | D.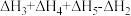 |
您最近半年使用:0次
2 . 某团队报道了高温富水环境下,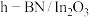 催化丙烷氧化脱氢原理,涉及反应如下:
催化丙烷氧化脱氢原理,涉及反应如下:
i.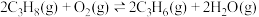

ii.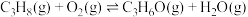

回答下列问题:
(1)上述反应过程中涉及的C、N、O元素可以组成多种配体,如CO、 、
、 等,CO、
等,CO、 的配位原子是C,而
的配位原子是C,而 的配位原子是N,简述其原因
的配位原子是N,简述其原因___________ 。
(2)已知:丙烷、丙烯的燃烧热分别为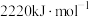 、
、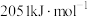 。18g液态水变为
。18g液态水变为 吸收热量44kJ。则
吸收热量44kJ。则
___________  。下列关于反应i自发性判断正确的是
。下列关于反应i自发性判断正确的是___________ (填标号)。
A.任何温度都能自发进行 B.任何温度都不能自发进行
C.在较高温度下能自发进行 D.在较低温度下能自发进行
(3)已知反应i速率方程为 (k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
(k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
①一定温度下,反应速率与浓度( )关系如下表所示:
)关系如下表所示:
根据数据计算,α+β+γ+δ=___________ 。
②速率常数与温度、活化能关系式为 (R、C为常数,T为温度,
(R、C为常数,T为温度, 为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与
为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与 关系如图:
关系如图:___________ (填“Cat1”或“Cat2”)。
(4)在密闭容器中充入 和
和 ,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:
,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:___________ 。
② 下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)在熔融碳酸钠中,丙烷-空气燃料电池的放电效率高。该燃料电池放电时,负极的电极反应式为___________ 。
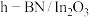 催化丙烷氧化脱氢原理,涉及反应如下:
催化丙烷氧化脱氢原理,涉及反应如下:i.
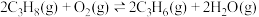

ii.
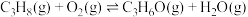

回答下列问题:
(1)上述反应过程中涉及的C、N、O元素可以组成多种配体,如CO、
 、
、 等,CO、
等,CO、 的配位原子是C,而
的配位原子是C,而 的配位原子是N,简述其原因
的配位原子是N,简述其原因(2)已知:丙烷、丙烯的燃烧热分别为
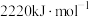 、
、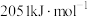 。18g液态水变为
。18g液态水变为 吸收热量44kJ。则
吸收热量44kJ。则
 。下列关于反应i自发性判断正确的是
。下列关于反应i自发性判断正确的是A.任何温度都能自发进行 B.任何温度都不能自发进行
C.在较高温度下能自发进行 D.在较低温度下能自发进行
(3)已知反应i速率方程为
 (k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
(k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。①一定温度下,反应速率与浓度(
 )关系如下表所示:
)关系如下表所示:| 序号 |  | 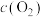 | 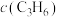 | 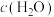 | v |
| Ⅰ | 0.1 | 0.1 | 0.1 | 0.1 | k |
| Ⅱ | 0.2 | 0.1 | 0.1 | 0.1 | 4k |
| Ⅲ | 0.2 | 0.4 | 0.1 | 0.1 | 8k |
| Ⅳ | 0.4 | 0.1 | 0.2 | 0.1 | 8k |
| Ⅴ | 0.4 | 0.4 | 0.1 | 0.2 | 16k |
②速率常数与温度、活化能关系式为
 (R、C为常数,T为温度,
(R、C为常数,T为温度, 为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与
为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与 关系如图:
关系如图: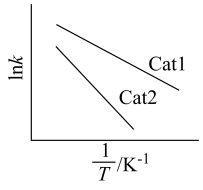
(4)在密闭容器中充入
 和
和 ,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:
,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示: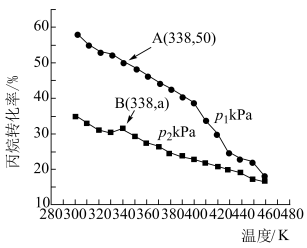
②
 下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
(5)在熔融碳酸钠中,丙烷-空气燃料电池的放电效率高。该燃料电池放电时,负极的电极反应式为
您最近半年使用:0次
名校
解题方法
3 . 向恒容密闭容器中充入1molCO2和1molH2,发生反应: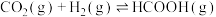 。测定不同温度下CO2的平衡转化率数据如下表所示:
。测定不同温度下CO2的平衡转化率数据如下表所示:
(1)该反应的
_____ 0(填“>”或“<”):
(2)已知:
 ,则反应
,则反应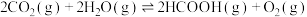 的
的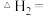
_____ (用△H和 表示):
表示):
(3)下列有利于提高CO2的平衡转化率的措施有_____。
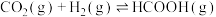 。测定不同温度下CO2的平衡转化率数据如下表所示:
。测定不同温度下CO2的平衡转化率数据如下表所示:| T/K | 373 | 473 | 573 | 673 |
| 平衡转化率 | α | 8.4α | 24.3α | 37.5α |

(2)已知:

 ,则反应
,则反应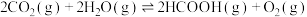 的
的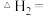
 表示):
表示):(3)下列有利于提高CO2的平衡转化率的措施有_____。
| A.增大反应体系的压强 | B.增大 |
| C.降低反应温度 | D.移出HCOOH |
您最近半年使用:0次
名校
解题方法
4 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)
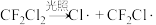 反应①
反应①
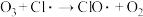 反应②
反应②
 反应③
反应③
(1)活性氯( )的作用是
)的作用是_____ 。
反应②和反应③的能量变化图如下所示
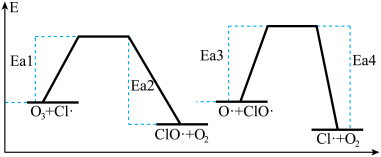
(2)利用上图数据计算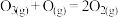 的
的
_____ 。
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)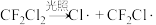 反应①
反应①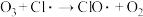 反应②
反应② 反应③
反应③(1)活性氯(
 )的作用是
)的作用是反应②和反应③的能量变化图如下所示

(2)利用上图数据计算
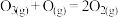 的
的
您最近半年使用:0次
名校
解题方法
5 . CO2可作为弱氧化剂用于乙烷脱氢制备乙烯。
(1)查阅下面资料,可实现计算CO2氧化C2H6脱氢反应的反应热:
i.需要查阅______ 的燃烧热数据(填化学式)。
ii.再查阅水的汽化热:H2O(l)=H2O(g) △H1=+44.0kJ•mol-1。
利用上述数据,可得如下热化学方程式:C2H6(g)+CO2(g)=C2H4(g)+CO(g)+H2O(g) △H2=+178.2kJ•mol-1
(2)判断该反应能够自发进行的条件______ 。
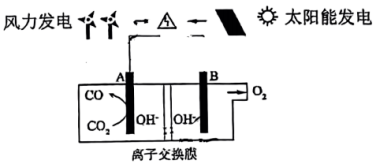
(3)如图是科学家利用温室气体CO2转化为CO的装置(A、B均采用石墨烯材料),下列说法正确的是______ 。
(1)查阅下面资料,可实现计算CO2氧化C2H6脱氢反应的反应热:
i.需要查阅
ii.再查阅水的汽化热:H2O(l)=H2O(g) △H1=+44.0kJ•mol-1。
利用上述数据,可得如下热化学方程式:C2H6(g)+CO2(g)=C2H4(g)+CO(g)+H2O(g) △H2=+178.2kJ•mol-1
(2)判断该反应能够自发进行的条件
| A.低温自发 | B.高温自发 | C.任何条件下均自发 | D.任何条件下均不自发 |

| A.A极的电极反应式为CO2+H2O+2e-=CO+2OH- |
| B.电路中通过2mol电子,将得到28gCO和11.2LO2 |
| C.该装置工作一段时间后,电解质溶液的pH减小 |
| D.A电极为阴极,离子交换膜为阴离子交换膜,OH-移向B极 |
您最近半年使用:0次
6 . 已知热化学方程式:

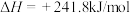
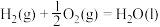
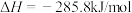
当1g液态水变为水蒸气时,其热量变化是

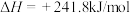
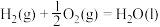
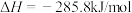
当1g液态水变为水蒸气时,其热量变化是
| A.吸热88kJ | B.吸热2.44kJ | C.放热44kJ | D.吸热44kJ |
您最近半年使用:0次
名校
解题方法
7 . 不同的化学反应具有不同的反应热,人们可以通过多种方法获得反应热的数据,通常用实验进行测定,也可以进行理论推算。
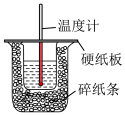
(1)在科学研究中,科学家常用量热计来测量反应热。我校某化学兴趣小组的同学欲测定中和热。用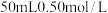 盐酸与
盐酸与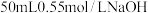 溶液在如图所示的简化装置中进行中和反应。则:
溶液在如图所示的简化装置中进行中和反应。则:
①从实验装置上看,图中尚缺少的一种仪器是______ 。
②大烧杯上如不盖硬纸板,求得的中和热数值_________ (填“偏大”“偏小”或“无影响”)。
③如果用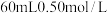 盐酸与
盐酸与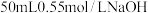 溶液进行反应,与上述实验相比,所求中和热
溶液进行反应,与上述实验相比,所求中和热_____ (填“相等”或“不相等”)。
(2) 与
与 在
在 催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用
催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用 作催化剂时该反应的过程示意图如图所示:
作催化剂时该反应的过程示意图如图所示:
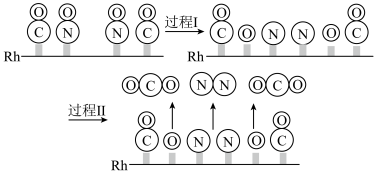
①过程Ⅰ为________ (填“吸热”或“放热”)过程。
②已知过程Ⅰ的焓变为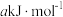 ,过程Ⅱ的焓变为
,过程Ⅱ的焓变为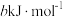 ,则该反应的热化学方程式为
,则该反应的热化学方程式为_______ 。
(3)已知: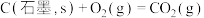
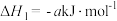
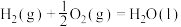
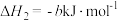
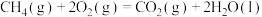
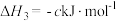
计算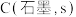 与
与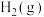 反应生成
反应生成 的
的 为
为______  (用含
(用含 的式子表示)。
的式子表示)。
(4)标准状况下, 在
在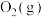 中完全燃烧生成
中完全燃烧生成 和
和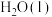 ,放出
,放出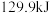 热量,请写出表示
热量,请写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:_______ 。

(1)在科学研究中,科学家常用量热计来测量反应热。我校某化学兴趣小组的同学欲测定中和热。用
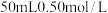 盐酸与
盐酸与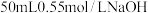 溶液在如图所示的简化装置中进行中和反应。则:
溶液在如图所示的简化装置中进行中和反应。则:①从实验装置上看,图中尚缺少的一种仪器是
②大烧杯上如不盖硬纸板,求得的中和热数值
③如果用
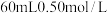 盐酸与
盐酸与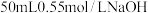 溶液进行反应,与上述实验相比,所求中和热
溶液进行反应,与上述实验相比,所求中和热(2)
 与
与 在
在 催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用
催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用 作催化剂时该反应的过程示意图如图所示:
作催化剂时该反应的过程示意图如图所示:
①过程Ⅰ为
②已知过程Ⅰ的焓变为
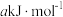 ,过程Ⅱ的焓变为
,过程Ⅱ的焓变为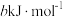 ,则该反应的热化学方程式为
,则该反应的热化学方程式为(3)已知:
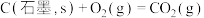
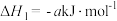
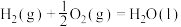
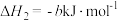
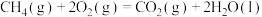
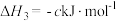
计算
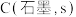 与
与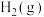 反应生成
反应生成 的
的 为
为 (用含
(用含 的式子表示)。
的式子表示)。(4)标准状况下,
 在
在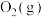 中完全燃烧生成
中完全燃烧生成 和
和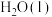 ,放出
,放出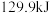 热量,请写出表示
热量,请写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:
您最近半年使用:0次
名校
解题方法
8 . 在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如下
反应I:2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g)
反应II:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
(1)已知:C2H4(g)+3O2(g)=2CO2(g)+2H2Og) 1=﹣1323.2kJ/mol
1=﹣1323.2kJ/mol
H2(g) O2(g)=H2O(g)
O2(g)=H2O(g)  2=﹣241.8kJ/mol
2=﹣241.8kJ/mol
请计算反应I的 =
=___________ 。
(2)在体积为1L的恒容密闭容器中,起始n(CO2)=1mol,发生反应II制取甲醇,如图表示反应II在起始投料比【投料比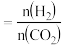 】分别为a、b时,CO2的平衡转化率随温度变化的关系
】分别为a、b时,CO2的平衡转化率随温度变化的关系
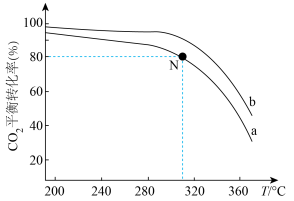
①投料比:a___________ b。(填“>”、“<”或“=”)
②310℃时,已知投料比a=4,求N点平衡常数K=___________ 。(保留两位有效数字)
③当投料比等于3时,关于反应II的说法正确的___________ 。
A.达到平衡后CO2和H2的平衡转化率相等
B.当v正(CO2)=3v逆(H2),该反应达到平衡状态
C.若反应改在恒压条件下进行,则放出的热量比恒容条件下少
D.当达到平衡后,再次充入1molCO2、3molH2,CO2的平衡转化率减小
反应I:2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g)
反应II:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
(1)已知:C2H4(g)+3O2(g)=2CO2(g)+2H2Og)
 1=﹣1323.2kJ/mol
1=﹣1323.2kJ/molH2(g)
 O2(g)=H2O(g)
O2(g)=H2O(g)  2=﹣241.8kJ/mol
2=﹣241.8kJ/mol请计算反应I的
 =
=(2)在体积为1L的恒容密闭容器中,起始n(CO2)=1mol,发生反应II制取甲醇,如图表示反应II在起始投料比【投料比
 】分别为a、b时,CO2的平衡转化率随温度变化的关系
】分别为a、b时,CO2的平衡转化率随温度变化的关系
①投料比:a
②310℃时,已知投料比a=4,求N点平衡常数K=
③当投料比等于3时,关于反应II的说法正确的
A.达到平衡后CO2和H2的平衡转化率相等
B.当v正(CO2)=3v逆(H2),该反应达到平衡状态
C.若反应改在恒压条件下进行,则放出的热量比恒容条件下少
D.当达到平衡后,再次充入1molCO2、3molH2,CO2的平衡转化率减小
您最近半年使用:0次
9 . 捕集并转化CO2可以有效实现碳达峰、碳中和。
Ⅰ.工业上利用两种温室气体CH4和CO2催化重整制取H2和CO,主要反应为:
反应①:
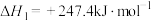
过程中还发生三个副反应:
反应②:

反应③: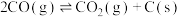
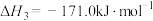
反应④: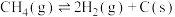 △H4
△H4
将CH4与CO2(体积比为1∶1)的混合气体以一定流速通过催化剂,产物中H2与CO的物质的量之比、CO2的转化率与温度的关系如图所示:
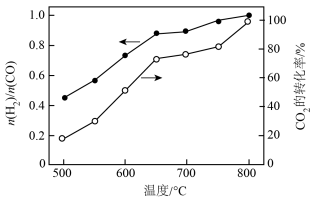
(1)△H4=___________ kJ·mol-1。
(2)500℃时, 比较小,此时发生的副反应以
比较小,此时发生的副反应以___________ (选填②、③、④中一种)为主。升高温度,产物中H2与CO的物质的量之比增大的原因是___________ 。
Ⅱ.光催化CH4和CO2生成CO和H2催化反应机理如图所示:
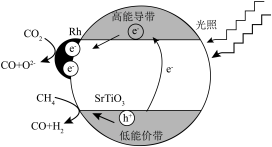
(3)上述反应机理中表现出氧化性的粒子有___________ 。
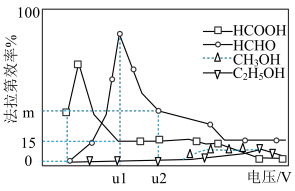
Ⅲ.用光电化学法将CO2还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:
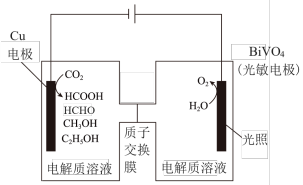
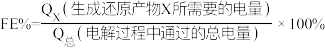 ,其中,Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,其中,Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
(4)当电解电压为u1V时,阴极生成HCHO的电极反应式为___________ 。
(5)当电解电压为u2V时,电解生成的HCOOH和HCHO的物质的量之比为5:6,生成HCHO的法拉第效率m为___________ 。
Ⅰ.工业上利用两种温室气体CH4和CO2催化重整制取H2和CO,主要反应为:
反应①:

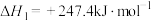
过程中还发生三个副反应:
反应②:


反应③:
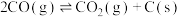
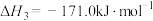
反应④:
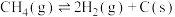 △H4
△H4将CH4与CO2(体积比为1∶1)的混合气体以一定流速通过催化剂,产物中H2与CO的物质的量之比、CO2的转化率与温度的关系如图所示:

(1)△H4=
(2)500℃时,
 比较小,此时发生的副反应以
比较小,此时发生的副反应以Ⅱ.光催化CH4和CO2生成CO和H2催化反应机理如图所示:

(3)上述反应机理中表现出氧化性的粒子有
Ⅲ.用光电化学法将CO2还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:


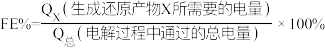 ,其中,Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,其中,Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。(4)当电解电压为u1V时,阴极生成HCHO的电极反应式为
(5)当电解电压为u2V时,电解生成的HCOOH和HCHO的物质的量之比为5:6,生成HCHO的法拉第效率m为
您最近半年使用:0次
解题方法
10 .  与ICl的反应机理如下:
与ICl的反应机理如下:
反应①: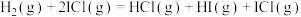 ;
;
反应②: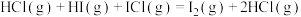 ,
,
其能量曲线如下图所示。不正确 的是
 与ICl的反应机理如下:
与ICl的反应机理如下:反应①:
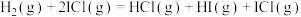 ;
;反应②:
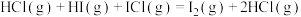 ,
,其能量曲线如下图所示。

A.反应①的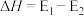 |
| B.反应①②均是放热反应 |
C. 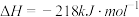 |
| D.该反应的反应速率主要取决于②的快慢 |
您最近半年使用:0次
2024-01-20更新
|
165次组卷
|
2卷引用:北京市顺义区2023-2024学年高二上学期期末质量监测化学试题



