解题方法
1 . 科学家在寻求将太阳能转化成化学能的办法,其中办法之一就是利用太阳能将 分解成
分解成 ,再将化学能转化为其他能源。右图是有关的能量循环示意图(已知:H-H键的键能为a
,再将化学能转化为其他能源。右图是有关的能量循环示意图(已知:H-H键的键能为a  ,O—O键的键能为b
,O—O键的键能为b  )。下列有关说法正确的是
)。下列有关说法正确的是
 分解成
分解成 ,再将化学能转化为其他能源。右图是有关的能量循环示意图(已知:H-H键的键能为a
,再将化学能转化为其他能源。右图是有关的能量循环示意图(已知:H-H键的键能为a  ,O—O键的键能为b
,O—O键的键能为b  )。下列有关说法正确的是
)。下列有关说法正确的是
A.图中 |
B.断开1mol H—O键所需要的太阳能为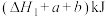 |
C.1mol  燃烧生成液态水的能量变化为 燃烧生成液态水的能量变化为 |
D.水蒸气所具有的能量比液态水多 kJ kJ |
您最近一年使用:0次
解题方法
2 . 研究大气中含硫化合物(主要是SO2和H2S)的转化具有重要意义。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离H2,发生的反应为2H2S(g) 2H2(g)+S2(g) △H。
2H2(g)+S2(g) △H。
已知:①H2S(g) H2(g)+S(g) △H1;
H2(g)+S(g) △H1;
②2S(g) S2(g) △H2。
S2(g) △H2。
则△H=______ (用含△H1、△H2的式子表示)。
(2)土壤中的微生物可将大气中的H2S经两步反应氧化成SO ,两步反应的能量变化示意图如图:
,两步反应的能量变化示意图如图: (aq)的热化学方程式为
(aq)的热化学方程式为_______ 。
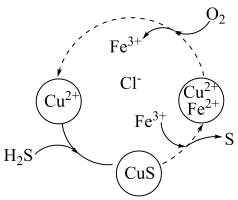
(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。______ 。
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有_______ 。
(4)二氧化硫—空气质子交换膜燃料电池可以利用大气中所含SO2快速启动,其装置示意图如图所示:______ (填“从A到B”或“从B到A”)。
②负极的电极反应为________ 。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离H2,发生的反应为2H2S(g)
 2H2(g)+S2(g) △H。
2H2(g)+S2(g) △H。已知:①H2S(g)
 H2(g)+S(g) △H1;
H2(g)+S(g) △H1;②2S(g)
 S2(g) △H2。
S2(g) △H2。则△H=
(2)土壤中的微生物可将大气中的H2S经两步反应氧化成SO
 ,两步反应的能量变化示意图如图:
,两步反应的能量变化示意图如图: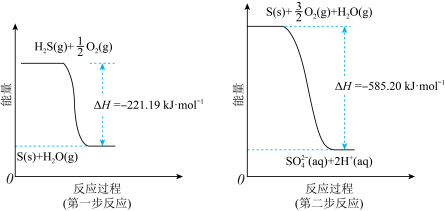
 (aq)的热化学方程式为
(aq)的热化学方程式为(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有
(4)二氧化硫—空气质子交换膜燃料电池可以利用大气中所含SO2快速启动,其装置示意图如图所示:
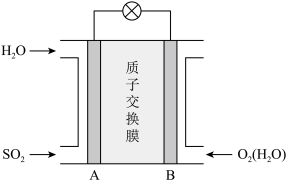
②负极的电极反应为
您最近一年使用:0次
3 . 已知:①
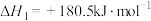
②
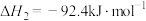
③
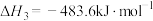
下列说法正确的是

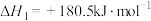
②

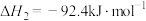
③

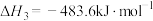
下列说法正确的是
A. 的燃烧热为 的燃烧热为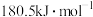 |
B. 的总能量一定大于 的总能量一定大于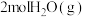 的总能量 的总能量 |
C.一定温度下在恒容密闭容器中充入 和足量 和足量 充分反应后可放热92.4kJ 充分反应后可放热92.4kJ |
D.氨的催化氧化反应的热方程式为 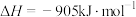 |
您最近一年使用:0次
名校
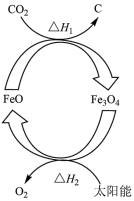
4 . 太阳能的开发与利用是能源领域的一个重要研究方向,由 制取C的太阳能工艺如图所示,下列有关说法
制取C的太阳能工艺如图所示,下列有关说法错误 的是( 代表阿伏加德罗常数的值)
代表阿伏加德罗常数的值)
 制取C的太阳能工艺如图所示,下列有关说法
制取C的太阳能工艺如图所示,下列有关说法 代表阿伏加德罗常数的值)
代表阿伏加德罗常数的值)
A.分解 转移的电子数为 转移的电子数为 |
B.根据盖斯定律, |
C. 在该工艺过程中起催化作用 在该工艺过程中起催化作用 |
| D.该工艺将太阳能转化为化学能 |
您最近一年使用:0次
5 . 当今世界多国相继规划了碳达峰、碳中和的时间节点,降低空气中二氧化碳含量成为研究热点。因此,研发二氧化碳的利用技术,将二氧化碳转化为能源是缓解环境和能源问题的方案之一、请回答下列问题:
Ⅰ. 耦合乙苯(
耦合乙苯( )脱氢制备苯乙烯(
)脱氢制备苯乙烯( )是综合利用
)是综合利用 的热点研究领域。制备苯乙烯涉及的主要反应如下:
的热点研究领域。制备苯乙烯涉及的主要反应如下:
i、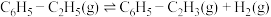

ii、

iii、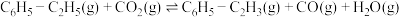
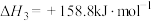
(1)
_____  。当反应达到平衡时,要提高
。当反应达到平衡时,要提高 的平衡产率,可采取的措施为
的平衡产率,可采取的措施为_____ (任写一种)。
(2)在某恒温恒容容器中发生 耦合乙苯(
耦合乙苯( )脱氢制备苯乙烯(
)脱氢制备苯乙烯( )的反应,下列能说明反应达到平衡的是_____(填标号)。
)的反应,下列能说明反应达到平衡的是_____(填标号)。
(3)恒压0.1MPa下,将原料气配比改为下列三种情况:只有 、
、 :
: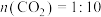 (对应曲线3)、
(对应曲线3)、 仅发生反应下i、ii,测得
仅发生反应下i、ii,测得 的平衡转化率与温度的变化关系如图1所示。
的平衡转化率与温度的变化关系如图1所示。
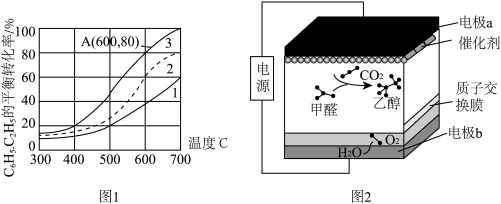
①图中表示原料气配比仅 的曲线是曲线
的曲线是曲线_____ (填“1”或“2”)。
②A点时, 的物质的量分数为0.01,该条件下反应i的
的物质的量分数为0.01,该条件下反应i的
_____ (分压=总压×物质的量分数)MPa.
Ⅱ.中科院化学所研究出了一种常温常压下通过电化学共还原 和甲醛进行偶联的方法,该方法能够同时实现甲醛的处理与
和甲醛进行偶联的方法,该方法能够同时实现甲醛的处理与 的高附加值转化,其工作原理如图2所示,总反应为
的高附加值转化,其工作原理如图2所示,总反应为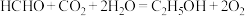 。
。
(4)电极b的电极反应式为_____ ,每生成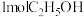 ,电路中转移的电子数为
,电路中转移的电子数为_____  。
。
Ⅰ.
 耦合乙苯(
耦合乙苯( )脱氢制备苯乙烯(
)脱氢制备苯乙烯( )是综合利用
)是综合利用 的热点研究领域。制备苯乙烯涉及的主要反应如下:
的热点研究领域。制备苯乙烯涉及的主要反应如下:i、
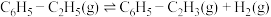

ii、


iii、
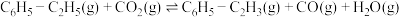
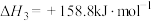
(1)

 。当反应达到平衡时,要提高
。当反应达到平衡时,要提高 的平衡产率,可采取的措施为
的平衡产率,可采取的措施为(2)在某恒温恒容容器中发生
 耦合乙苯(
耦合乙苯( )脱氢制备苯乙烯(
)脱氢制备苯乙烯( )的反应,下列能说明反应达到平衡的是_____(填标号)。
)的反应,下列能说明反应达到平衡的是_____(填标号)。| A.容器内压强不再发生变化 |
| B.CO的百分含量不再发生变化 |
| C.容器内混合气体的密度不再发生变化 |
D.每消耗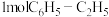 的同时生成 的同时生成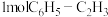 |
 、
、 :
: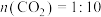 (对应曲线3)、
(对应曲线3)、 仅发生反应下i、ii,测得
仅发生反应下i、ii,测得 的平衡转化率与温度的变化关系如图1所示。
的平衡转化率与温度的变化关系如图1所示。
①图中表示原料气配比仅
 的曲线是曲线
的曲线是曲线②A点时,
 的物质的量分数为0.01,该条件下反应i的
的物质的量分数为0.01,该条件下反应i的
Ⅱ.中科院化学所研究出了一种常温常压下通过电化学共还原
 和甲醛进行偶联的方法,该方法能够同时实现甲醛的处理与
和甲醛进行偶联的方法,该方法能够同时实现甲醛的处理与 的高附加值转化,其工作原理如图2所示,总反应为
的高附加值转化,其工作原理如图2所示,总反应为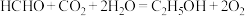 。
。(4)电极b的电极反应式为
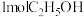 ,电路中转移的电子数为
,电路中转移的电子数为 。
。
您最近一年使用:0次
2023-06-29更新
|
301次组卷
|
3卷引用:甘肃省靖远县第一中学2022-2023学年高二下学期期末练习化学试题
名校
6 . 回答下列问题
(1)在一定条件下,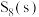 和
和 (g)发生反应依次转化为
(g)发生反应依次转化为 (g)和
(g)和 (g)。反应过程和能量关系可用如图简单表示(图中的
(g)。反应过程和能量关系可用如图简单表示(图中的 表示生成1mol产物的数据)
表示生成1mol产物的数据)

①写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:_______ 。
②写出 分解生成
分解生成 和
和 的热化学方程式:
的热化学方程式:_______ 。
(2)恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示。
已知:
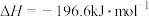
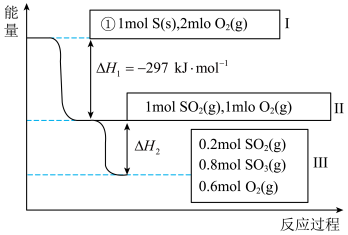
①写出能表示硫的燃烧热的热化学方程式:_______ 。
②
_______  。
。
(3) 焙烧产生的
焙烧产生的 可用于制硫酸。
可用于制硫酸。
已知25℃、101kPa时,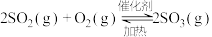
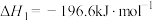
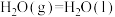
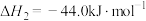 ;
;
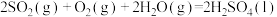
 ;
;
则 (g)与
(g)与 反应生成
反应生成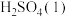 的热化学方程式是
的热化学方程式是_______ 。
(1)在一定条件下,
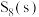 和
和 (g)发生反应依次转化为
(g)发生反应依次转化为 (g)和
(g)和 (g)。反应过程和能量关系可用如图简单表示(图中的
(g)。反应过程和能量关系可用如图简单表示(图中的 表示生成1mol产物的数据)
表示生成1mol产物的数据)
①写出表示
 燃烧热的热化学方程式:
燃烧热的热化学方程式:②写出
 分解生成
分解生成 和
和 的热化学方程式:
的热化学方程式:(2)恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示。
已知:

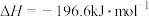

①写出能表示硫的燃烧热的热化学方程式:
②

 。
。(3)
 焙烧产生的
焙烧产生的 可用于制硫酸。
可用于制硫酸。已知25℃、101kPa时,
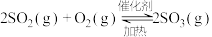
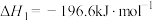
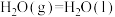
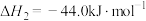 ;
;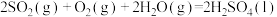
 ;
;则
 (g)与
(g)与 反应生成
反应生成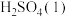 的热化学方程式是
的热化学方程式是
您最近一年使用:0次
7 . 工业上常利用 和
和 合成尿素
合成尿素 ,该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是
,该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是
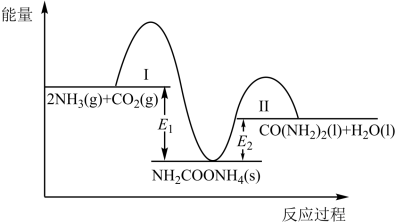
 和
和 合成尿素
合成尿素 ,该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是
,该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是
A. 为合成尿素反应的中间产物 为合成尿素反应的中间产物 |
B.利用 和 和 合成尿素是放热反应 合成尿素是放热反应 |
| C.反应II在热力学上进行趋势很大 |
D.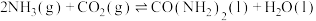 的焓变 的焓变 |
您最近一年使用:0次
2023-01-12更新
|
241次组卷
|
2卷引用:甘肃天祝藏族自治县第一中学2022-2023学年高二上学期1月期末考试化学试题
名校
8 . HCl气体被氧气氧化的能量关系如图,下列叙述正确的是


A.该反应 、 、 |
B.该反应的浓度平衡常数 |
C.用E表示键能,则该反应 |
D.反应 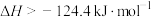 |
您最近一年使用:0次
2023-01-11更新
|
329次组卷
|
3卷引用:甘肃省庆阳市2022-2023学年高二上学期期末考试化学试题
名校
9 . 二氧化碳是常见的温室气体, 的回收利用是环保领域研究的热点课题。请回答下列问题:
的回收利用是环保领域研究的热点课题。请回答下列问题:
(1)利用 和
和 合成甲醇,下列为合成甲醇的有关化学方程式:
合成甲醇,下列为合成甲醇的有关化学方程式:
①
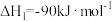
②

③

上述反应中
___________  。
。
(2)以 与
与 为原料可以合成尿素[
为原料可以合成尿素[ ],合成尿素的反应为
],合成尿素的反应为 。
。
①在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示,该反应的
___________ (填“>”“<”或“=”,下同)0,其他条件相同时,若y表示压强,则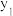
___________ 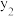 ,若y表示反应开始时的氨碳比[
,若y表示反应开始时的氨碳比[ ],则
],则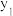
___________ 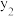 。
。

②T℃时,若向某压强为 的恒压密闭容器中充入
的恒压密闭容器中充入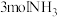 和
和 ,发生反应
,发生反应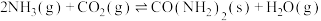 ,达到平衡时,容器的体积变为开始时的
,达到平衡时,容器的体积变为开始时的 ,该条件下
,该条件下 的平衡转化率为
的平衡转化率为___________ ,T℃时,该反应的平衡常数
___________ (用含 的代数式表示,利用各物质的平衡分压计算)。再向该容器中充入
的代数式表示,利用各物质的平衡分压计算)。再向该容器中充入 和
和 ,
, 的反应速率:
的反应速率:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)某甲醇燃料电池的工作原理如图所示,质子交换膜(只有质子能够通过)左右两侧的溶液均为1L2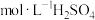 溶液,电极a的电极反应式为
溶液,电极a的电极反应式为___________ ,当导线中有1mol 转移时,左右两侧溶液的质量差为
转移时,左右两侧溶液的质量差为___________ g(假设反应物耗尽,忽略气质子交换膜体的溶解)。

 的回收利用是环保领域研究的热点课题。请回答下列问题:
的回收利用是环保领域研究的热点课题。请回答下列问题:(1)利用
 和
和 合成甲醇,下列为合成甲醇的有关化学方程式:
合成甲醇,下列为合成甲醇的有关化学方程式:①

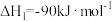
②


③


上述反应中

 。
。(2)以
 与
与 为原料可以合成尿素[
为原料可以合成尿素[ ],合成尿素的反应为
],合成尿素的反应为 。
。①在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示,该反应的

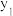
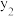 ,若y表示反应开始时的氨碳比[
,若y表示反应开始时的氨碳比[ ],则
],则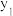
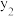 。
。
②T℃时,若向某压强为
 的恒压密闭容器中充入
的恒压密闭容器中充入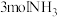 和
和 ,发生反应
,发生反应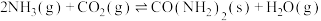 ,达到平衡时,容器的体积变为开始时的
,达到平衡时,容器的体积变为开始时的 ,该条件下
,该条件下 的平衡转化率为
的平衡转化率为
 的代数式表示,利用各物质的平衡分压计算)。再向该容器中充入
的代数式表示,利用各物质的平衡分压计算)。再向该容器中充入 和
和 ,
, 的反应速率:
的反应速率:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)某甲醇燃料电池的工作原理如图所示,质子交换膜(只有质子能够通过)左右两侧的溶液均为1L2
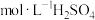 溶液,电极a的电极反应式为
溶液,电极a的电极反应式为 转移时,左右两侧溶液的质量差为
转移时,左右两侧溶液的质量差为
您最近一年使用:0次
2022-01-26更新
|
252次组卷
|
3卷引用:甘肃省酒泉市2022-2023学年高二上学期1月期末考试化学试题
10 . 研究碳、氮、硫等元素化合物的性质或转化对建设生态文明、美丽中国具有重要意义,请按要求回答下列问题。
I.H2S是石油化工行业广泛存在的污染性气体,但同时也是重要的氢源和硫源,工业上可以采取多种方式处理。
(1)已知:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l);ΔH1=akJ·mol-1
S(s)+O2(g)=SO2(g);ΔH2=bkJ·mol-1
则空气氧化脱除H2S反应2H2S(g)+O2(g)=2S(s)+2H2O(l)的ΔH=___________ kJ·mol-1.
(2)H2S与CO2在高温下发生反应: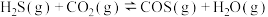 。在340℃时,将1molCO2与1molH2S充入2L的空钢瓶中。该反应平衡后
。在340℃时,将1molCO2与1molH2S充入2L的空钢瓶中。该反应平衡后 的物质的量分数为
的物质的量分数为 ,反应平衡常数K=
,反应平衡常数K=___________ 。
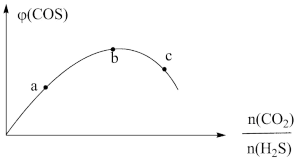
(3)若将H2S和CO2按不同比例投入一密闭容器中发生上述反应,反应达到平衡时,COS的体积分数随H2S和CO2的投料比的变化曲线如图所示,则b点时,平衡体系中S、C原子个数比接近___________ ;a、b、c三点CO2的转化率最大的是___________ 。
II.下图是一个电化学过程的示意图。请回答下列问题:

(4)写出通入CH3OH的电极的电极反应式:___________ 。
(5)乙池中反应的化学方程式___________ 。
(6)当乙池中B(Ag)极质量增加10.8g,甲池中理论上消耗标准状况O2的体积为___________,此时丙池中某电极析出某金属,则丙池中的某盐溶液可能是___________
I.H2S是石油化工行业广泛存在的污染性气体,但同时也是重要的氢源和硫源,工业上可以采取多种方式处理。
(1)已知:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l);ΔH1=akJ·mol-1
S(s)+O2(g)=SO2(g);ΔH2=bkJ·mol-1
则空气氧化脱除H2S反应2H2S(g)+O2(g)=2S(s)+2H2O(l)的ΔH=
(2)H2S与CO2在高温下发生反应:
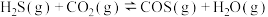 。在340℃时,将1molCO2与1molH2S充入2L的空钢瓶中。该反应平衡后
。在340℃时,将1molCO2与1molH2S充入2L的空钢瓶中。该反应平衡后 的物质的量分数为
的物质的量分数为 ,反应平衡常数K=
,反应平衡常数K=(3)若将H2S和CO2按不同比例投入一密闭容器中发生上述反应,反应达到平衡时,COS的体积分数随H2S和CO2的投料比的变化曲线如图所示,则b点时,平衡体系中S、C原子个数比接近

II.下图是一个电化学过程的示意图。请回答下列问题:

(4)写出通入CH3OH的电极的电极反应式:
(5)乙池中反应的化学方程式
(6)当乙池中B(Ag)极质量增加10.8g,甲池中理论上消耗标准状况O2的体积为___________,此时丙池中某电极析出某金属,则丙池中的某盐溶液可能是___________
| A.MgSO4 | B.CuSO4 | C.NaCl | D.AgNO3 |
您最近一年使用:0次



