解题方法
1 . 工业上利用反应 制取氢气。向两个容积为
制取氢气。向两个容积为 的密闭容器中加入
的密闭容器中加入 和
和 各
各 ,分别在不同温度和催化剂下进行反应,保持其他初始实验条件不变,经
,分别在不同温度和催化剂下进行反应,保持其他初始实验条件不变,经 测得两容器中
测得两容器中 转化率如图所示。下列说法正确的是
转化率如图所示。下列说法正确的是

 制取氢气。向两个容积为
制取氢气。向两个容积为 的密闭容器中加入
的密闭容器中加入 和
和 各
各 ,分别在不同温度和催化剂下进行反应,保持其他初始实验条件不变,经
,分别在不同温度和催化剂下进行反应,保持其他初始实验条件不变,经 测得两容器中
测得两容器中 转化率如图所示。下列说法正确的是
转化率如图所示。下列说法正确的是
| A.A点和B点均为反应的平衡状态 |
| B.催化剂2比催化剂1的催化效率高 |
C.C点时,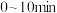 反应的平均速率 反应的平均速率 |
D.温度为 时,该反应平衡常数 时,该反应平衡常数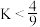 |
您最近一年使用:0次
名校
解题方法
2 . 金( )表面发生分解反应:
)表面发生分解反应: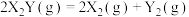 ,其速率方程为
,其速率方程为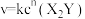 ,已知部分信息如下:
,已知部分信息如下:
①k为速率常数,只与催化剂、温度、固体接触面积有关,与浓度、压强无关;
②化学上,将物质消耗一半所用时间称为半衰期。
在某温度下,实验测得 与时间变化的关系如下表所示:
与时间变化的关系如下表所示:
下列叙述正确的是
 )表面发生分解反应:
)表面发生分解反应: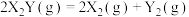 ,其速率方程为
,其速率方程为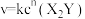 ,已知部分信息如下:
,已知部分信息如下:①k为速率常数,只与催化剂、温度、固体接触面积有关,与浓度、压强无关;
②化学上,将物质消耗一半所用时间称为半衰期。
在某温度下,实验测得
 与时间变化的关系如下表所示:
与时间变化的关系如下表所示: | 0 | 20 | 40 | 60 | 80 | 100 |
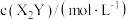 | 0.100 | 0.080 | 0.060 | 0.040 | 0.020 | 0 |
| A.升高温度,反应速率不变 |
B. |
C.其他条件不变,若 起始浓度为c 起始浓度为c ,则半衰期为250c min ,则半衰期为250c min |
D.当使用催化剂时,升高温度,反应10min时 可能大于0.09 可能大于0.09 |
您最近一年使用:0次
3 . 某温度下,在1L恒温密闭容器中投入20molX,发生反应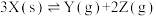 ,有关说法正确的是
,有关说法正确的是
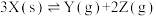 ,有关说法正确的是
,有关说法正确的是| 时间段/s | 产物Z的平均生成速率/(mol·L-1·s-1) |
| 1~10 | 0.4 |
| 0~20 | 0.3 |
| 0~30 | 0.2 |
| A.5s时,Y的浓度为1mol·L-1 |
| B.10s时,加入1molZ,此时v正(Z)<v逆(Z) |
| C.25s时,X的转化率为45% |
| D.30s时,加入1molY和2molZ,再次平衡时体系压强增大 |
您最近一年使用:0次
名校
4 .  时,向容积为
时,向容积为 的密闭容器中充入一定量的
的密闭容器中充入一定量的 和
和 ,发生如下反应:
,发生如下反应: 。反应过程中测得的部分数据如表所示,下列说法中,不正确的是
。反应过程中测得的部分数据如表所示,下列说法中,不正确的是
 时,向容积为
时,向容积为 的密闭容器中充入一定量的
的密闭容器中充入一定量的 和
和 ,发生如下反应:
,发生如下反应: 。反应过程中测得的部分数据如表所示,下列说法中,不正确的是
。反应过程中测得的部分数据如表所示,下列说法中,不正确的是| t | 0 | 10 | 20 | 30 |
| n(CO) | 0.10 | 0.04 | 0.02 | |
| n(H2) | 0.20 | 0.04 |
A.反应在前 内的平均速率为 内的平均速率为 |
B. 时,该反应的平衡常数数值为 时,该反应的平衡常数数值为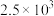 |
C.保持其他条件不变,升高温度,平衡时 ,则反应的 ,则反应的 |
D. 时,平衡时 时,平衡时 |
您最近一年使用:0次
名校
解题方法
5 . 一定条件下,在一容积为2L的刚性密闭容器中,将4molN气体和2molM气体混合,发生如下反应: ,10min末反应达到平衡,生成0.6molR,测得Q的浓度为0.9mol·L-1。下列说法中错误的是
,10min末反应达到平衡,生成0.6molR,测得Q的浓度为0.9mol·L-1。下列说法中错误的是
 ,10min末反应达到平衡,生成0.6molR,测得Q的浓度为0.9mol·L-1。下列说法中错误的是
,10min末反应达到平衡,生成0.6molR,测得Q的浓度为0.9mol·L-1。下列说法中错误的是| A.前l0min内用M表示的化学反应速率为0.06mol·L-1·min-1 |
| B.化学方程式中x的值为3 |
| C.N的转化率为60% |
| D.随着反应的进行,混合气体的平均相对分子质量会减小 |
您最近一年使用:0次
名校
6 . 利用甲烷可消除 的污染:
的污染: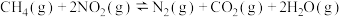 。在容积为1 L的密闭容器中,控制不同温度,分别加入0.50 mol
。在容积为1 L的密闭容器中,控制不同温度,分别加入0.50 mol  和1.2 mol
和1.2 mol  ,测得
,测得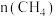 (mol)随时间变化的有关实验数据见下表。
(mol)随时间变化的有关实验数据见下表。
下列说法正确的是
 的污染:
的污染: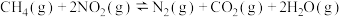 。在容积为1 L的密闭容器中,控制不同温度,分别加入0.50 mol
。在容积为1 L的密闭容器中,控制不同温度,分别加入0.50 mol  和1.2 mol
和1.2 mol  ,测得
,测得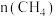 (mol)随时间变化的有关实验数据见下表。
(mol)随时间变化的有关实验数据见下表。| 组别 | 温度 | 时间/min | ||||
| 0 | 10 | 20 | 40 | 50 | ||
| ① |  | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② |  | 0.50 | 0.30 | 0.18 | 0.15 | |
A. 时,0~20 min内, 时,0~20 min内, 的降解速率为0.0125 mol⋅L 的降解速率为0.0125 mol⋅L ⋅min ⋅min |
B.由实验数据可知,实验控制的温度: |
C.40 min时,表格中 对应的数据可能为0.16 对应的数据可能为0.16 |
| D.该反应只有在高温下才能自发进行 |
您最近一年使用:0次
名校
解题方法
7 . 在一恒容密闭容器中,仅X(g)与Y(g)发生反应生成Z(g),反应速率分别用 、
、 、
、 表示。若从反应开始至达到平衡的这一段时间内,测得
表示。若从反应开始至达到平衡的这一段时间内,测得 ,
, ,则该反应的方程式为
,则该反应的方程式为
 、
、 、
、 表示。若从反应开始至达到平衡的这一段时间内,测得
表示。若从反应开始至达到平衡的这一段时间内,测得 ,
, ,则该反应的方程式为
,则该反应的方程式为A. | B. |
C.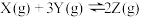 | D. |
您最近一年使用:0次
2023-12-12更新
|
119次组卷
|
3卷引用:吉林省白山市抚松县第一中学2023-2024学年高二上学期12月月考化学试题
名校
8 . 反应 的速率方程为
的速率方程为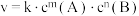 (k为速率常数,其中
(k为速率常数,其中 , A、R为常数,
, A、R为常数, 为活化能,T为开氏温度,其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
为活化能,T为开氏温度,其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
 的速率方程为
的速率方程为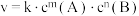 (k为速率常数,其中
(k为速率常数,其中 , A、R为常数,
, A、R为常数, 为活化能,T为开氏温度,其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
为活化能,T为开氏温度,其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是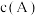 / / | 0.25 | 0.5 | 1 | 0.5 | 1 |
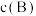 / / | 0.05 | 0.05 | 0.1 | 0.1 | 0.2 |
v/ | 1.6 | 3.2 | 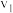 | 3.2 |  |
A.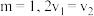 |
B. |
| C.升温、加入催化剂,缩小容积(加压),均能使k增大,导致反应的瞬时速率加快 |
D.在过量的B存在时,A剩余12.5%所需的时间是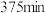 |
您最近一年使用:0次
9 . Ⅰ.某探究性学习小组利用 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
(1)通过实验A、B可探究_______ (填外部因素)的改变对反应速率的影响,其中
_______ ;
_______ ;通过实验_______ 可探究温度变化对化学反应速率的影响。
(2)若 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是_______ ;利用实验B中数据计算,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为_______ 。
Ⅱ.在 密闭容器中进行反应:
密闭容器中进行反应: ,式中m、n、p、q为化学计量数。在
,式中m、n、p、q为化学计量数。在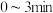 内,各物质物质的量的变化如下表所示:
内,各物质物质的量的变化如下表所示:
已知 内
内 ,
,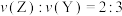 。
。
(3)确定以下物质的物质的量:起始时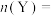
_______ ,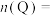
_______ 。
 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。| 实验 序号 | 实验温度/K |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时所需时间/s | ||
 |  |  |  |  | |||
| A | 293 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| B |  | 2 | 0.02 | 4 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 6 |  |


(2)若
 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为Ⅱ.在
 密闭容器中进行反应:
密闭容器中进行反应: ,式中m、n、p、q为化学计量数。在
,式中m、n、p、q为化学计量数。在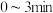 内,各物质物质的量的变化如下表所示:
内,各物质物质的量的变化如下表所示:| X | Y | Z | Q | |
| 起始/mol | 1.2 | 0 | ||
 末/mol 末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
 末/mol 末/mol | 0.8 |
 内
内 ,
,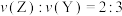 。
。(3)确定以下物质的物质的量:起始时
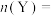
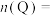
您最近一年使用:0次
名校
解题方法
10 . 含碳物质的转化是化学研究的热点之一。回答下列问题:
(1)页岩气中含有较多的乙烷,可用二氧化碳将其氧化为更有工业价值的乙烯。相关反应如下:
i.

ii.
 kJ⋅1mol
kJ⋅1mol
iii.
 kJ⋅mol
kJ⋅mol
计算
_______ kJ⋅mol ,该反应在
,该反应在_______ (填“低温”“高温”或“任意温度”)条件下能自发进行。
(2)一定温度下,将4 mol CO与2 mol 充入体积为2 L的恒容密闭容器中发生反应
充入体积为2 L的恒容密闭容器中发生反应
 体系中各物质的浓度随时间(0~6 min时段)的变化如图所示。
体系中各物质的浓度随时间(0~6 min时段)的变化如图所示。

①在0~4 min时段, 的平均反应速率
的平均反应速率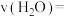
_______ ,该反应在上述温度下的平衡常数
_______ (保留1位小数)。
②该反应到4 min时,CO的转化率为_______ 。
③若保持与4 min时相同的温度,向另一容积为2 L的恒容密闭容器中同时充入0.5mol CO,1.5mol ,0.5 mol
,0.5 mol 和amol
和amol ,则当
,则当 时,上述反应向
时,上述反应向_______ (填“正反应”或“逆反应”)方向进行。若要使上述反应开始时向逆反应方向进行,a的取值范围为_______ 。
(1)页岩气中含有较多的乙烷,可用二氧化碳将其氧化为更有工业价值的乙烯。相关反应如下:
i.


ii.

 kJ⋅1mol
kJ⋅1mol
iii.

 kJ⋅mol
kJ⋅mol
计算

 ,该反应在
,该反应在(2)一定温度下,将4 mol CO与2 mol
 充入体积为2 L的恒容密闭容器中发生反应
充入体积为2 L的恒容密闭容器中发生反应
 体系中各物质的浓度随时间(0~6 min时段)的变化如图所示。
体系中各物质的浓度随时间(0~6 min时段)的变化如图所示。
①在0~4 min时段,
 的平均反应速率
的平均反应速率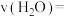

②该反应到4 min时,CO的转化率为
③若保持与4 min时相同的温度,向另一容积为2 L的恒容密闭容器中同时充入0.5mol CO,1.5mol
 ,0.5 mol
,0.5 mol 和amol
和amol ,则当
,则当 时,上述反应向
时,上述反应向
您最近一年使用:0次



