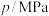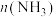解题方法
1 . 将 和
和 充入
充入 恒容密闭容器中发生反应:
恒容密闭容器中发生反应:
Ⅰ.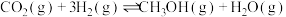
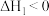 (慢反应)
(慢反应)
Ⅱ.
 (快反应)
(快反应)
测得相同时间内 、
、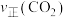 与温度的关系如图所示,下列说法错误的是
与温度的关系如图所示,下列说法错误的是
 和
和 充入
充入 恒容密闭容器中发生反应:
恒容密闭容器中发生反应:Ⅰ.
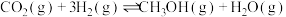
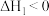 (慢反应)
(慢反应)Ⅱ.

 (快反应)
(快反应)测得相同时间内
 、
、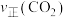 与温度的关系如图所示,下列说法错误的是
与温度的关系如图所示,下列说法错误的是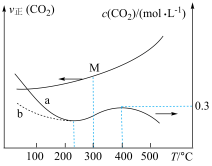
A.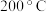 前,加入催化剂可使a线转化为b线 前,加入催化剂可使a线转化为b线 |
B. 时,M点对应的反应体系中, 时,M点对应的反应体系中, |
C. 时,若 时,若 时达到平衡,则 时达到平衡,则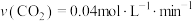 |
D. 后,温度对正反应速率的影响比浓度大 后,温度对正反应速率的影响比浓度大 |
您最近半年使用:0次
解题方法
2 . I.含碳化合物甲烷、 等是重要的化工原料,可生产氢气、甲醇、烯烃等物质。回答下列问题:
等是重要的化工原料,可生产氢气、甲醇、烯烃等物质。回答下列问题:
(1)一种甲烷催化氧化的反应历程如图所示,“*”表示微粒吸附在催化剂表面。下列叙述错误的是___________(填标号)。
Ⅱ.以氧化铟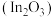 作催化剂,可实现
作催化剂,可实现 催化加氢制甲醇。
催化加氢制甲醇。
已知:ⅰ.催化剂活化: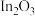 (无活性)
(无活性)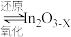 (有活性);
(有活性);
ⅱ. 与
与 在活化的催化剂表面同时发生如下反应:
在活化的催化剂表面同时发生如下反应:
反应①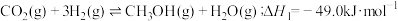
反应②
反应③: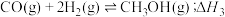
(2)反应③中
___________ 。
(3)工业上以原料气通过催化剂表面的方法生产甲醇, 是造成催化剂失活的重要原因,请用化学方程式表示催化剂失活的原因:
是造成催化剂失活的重要原因,请用化学方程式表示催化剂失活的原因:___________ 。为了减少催化剂的失活,可以采用的方法是___________ 。
(4)按 时只发生反应①,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时只发生反应①,在不同条件下达到平衡,设体系中甲醇的物质的量分数为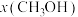 ,在t=250℃条件下的
,在t=250℃条件下的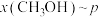 、在
、在 条件下的
条件下的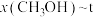 (温度)如图所示。
(温度)如图所示。___________ (填“a”或“b”),判断理由是___________ 。
ii.A、B、C、D、E、F中可能表示220℃ 时的平衡状态的点是
时的平衡状态的点是___________ 。
(5)将 和
和 按物质的量之比1:3混合通入刚性密闭容器中,在催化剂作用下只发生反应①和反应②。230℃时,容器内压强随时间的变化如下表所示:
按物质的量之比1:3混合通入刚性密闭容器中,在催化剂作用下只发生反应①和反应②。230℃时,容器内压强随时间的变化如下表所示:
反应①的速率可表示为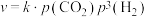 (
( 为常数),平衡时
为常数),平衡时 ,已知在
,已知在 时
时 的转化率为
的转化率为 ,则反应①的正向反应在
,则反应①的正向反应在 时的
时的
___________ (用含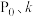 的式子表示)。
的式子表示)。
 等是重要的化工原料,可生产氢气、甲醇、烯烃等物质。回答下列问题:
等是重要的化工原料,可生产氢气、甲醇、烯烃等物质。回答下列问题:(1)一种甲烷催化氧化的反应历程如图所示,“*”表示微粒吸附在催化剂表面。下列叙述错误的是___________(填标号)。
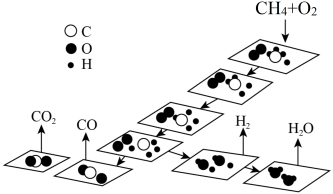
A.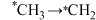 的过程中,放出能量 的过程中,放出能量 |
| B.产物从催化剂表面脱附的速率慢会降低总反应速率 |
C.适当提高 分压会降低 分压会降低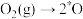 的反应速率 的反应速率 |
D. 与 与 反应生成 反应生成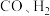 均涉及极性键、非极性键的断裂和生成 均涉及极性键、非极性键的断裂和生成 |
Ⅱ.以氧化铟
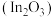 作催化剂,可实现
作催化剂,可实现 催化加氢制甲醇。
催化加氢制甲醇。已知:ⅰ.催化剂活化:
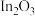 (无活性)
(无活性)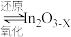 (有活性);
(有活性);ⅱ.
 与
与 在活化的催化剂表面同时发生如下反应:
在活化的催化剂表面同时发生如下反应:反应①
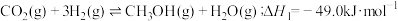
反应②

反应③:
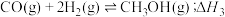
(2)反应③中

(3)工业上以原料气通过催化剂表面的方法生产甲醇,
 是造成催化剂失活的重要原因,请用化学方程式表示催化剂失活的原因:
是造成催化剂失活的重要原因,请用化学方程式表示催化剂失活的原因:(4)按
 时只发生反应①,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时只发生反应①,在不同条件下达到平衡,设体系中甲醇的物质的量分数为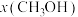 ,在t=250℃条件下的
,在t=250℃条件下的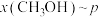 、在
、在 条件下的
条件下的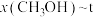 (温度)如图所示。
(温度)如图所示。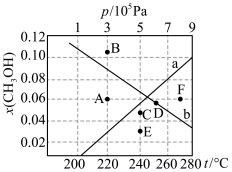
ii.A、B、C、D、E、F中可能表示220℃
 时的平衡状态的点是
时的平衡状态的点是(5)将
 和
和 按物质的量之比1:3混合通入刚性密闭容器中,在催化剂作用下只发生反应①和反应②。230℃时,容器内压强随时间的变化如下表所示:
按物质的量之比1:3混合通入刚性密闭容器中,在催化剂作用下只发生反应①和反应②。230℃时,容器内压强随时间的变化如下表所示:| 时间/min | 0 | 20 | 40 | 60 | 80 |
| 压强/MPa |  | 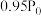 | 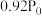 |  |  |
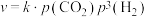 (
( 为常数),平衡时
为常数),平衡时 ,已知在
,已知在 时
时 的转化率为
的转化率为 ,则反应①的正向反应在
,则反应①的正向反应在 时的
时的
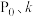 的式子表示)。
的式子表示)。
您最近半年使用:0次
解题方法
3 . 一氧化碳和氮的氧化物都是大气污染物,如何有效处理它们是科学家长期研究的课题.
(1)CO还原 的反应为:
的反应为:
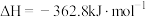 .
.
①研究者发现在气相中 催化CO与
催化CO与 反应的历程有两步:
反应的历程有两步:
第一步:
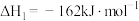
则第二步的热化学方程式为________________ ;
②在恒温恒容密闭容器中,反应一段时间后,以下能说明反应达到平衡状态的是________ (填字母);
A. B.混合气体的密度保持不变
B.混合气体的密度保持不变
C. 的体积分数保持不变 D.容器的压强保持不变
的体积分数保持不变 D.容器的压强保持不变
(2)在密闭容器中发生反应: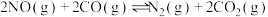
 .一段时间后达到平衡;
.一段时间后达到平衡;
①恒温恒压下,再向该容器中注入氩气,NO的平衡转化率煘小,其原因是________ ;
②一定温度下,在 恒容密闭容器中,加入
恒容密闭容器中,加入 和
和 各
各 ,反应过程中部分物质的体积分数(
,反应过程中部分物质的体积分数( )随时间(t)的变化如图1所示.曲线b代表的是
)随时间(t)的变化如图1所示.曲线b代表的是________ (填化学式)体积分数随时间的变化: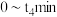 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为________  ;该温度下的平衡常数为
;该温度下的平衡常数为________  ;
;
①a电极的电极反应式为________________ ;
②电池工作一段时间,反应消耗了标准状况下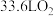 ,理论上负极区溶液增加的质量为
,理论上负极区溶液增加的质量为________ g。
(1)CO还原
 的反应为:
的反应为:
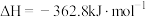 .
.①研究者发现在气相中
 催化CO与
催化CO与 反应的历程有两步:
反应的历程有两步:第一步:

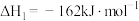
则第二步的热化学方程式为
②在恒温恒容密闭容器中,反应一段时间后,以下能说明反应达到平衡状态的是
A.
 B.混合气体的密度保持不变
B.混合气体的密度保持不变C.
 的体积分数保持不变 D.容器的压强保持不变
的体积分数保持不变 D.容器的压强保持不变(2)在密闭容器中发生反应:
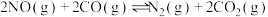
 .一段时间后达到平衡;
.一段时间后达到平衡;①恒温恒压下,再向该容器中注入氩气,NO的平衡转化率煘小,其原因是
②一定温度下,在
 恒容密闭容器中,加入
恒容密闭容器中,加入 和
和 各
各 ,反应过程中部分物质的体积分数(
,反应过程中部分物质的体积分数( )随时间(t)的变化如图1所示.曲线b代表的是
)随时间(t)的变化如图1所示.曲线b代表的是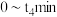 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为 ;该温度下的平衡常数为
;该温度下的平衡常数为 ;
; 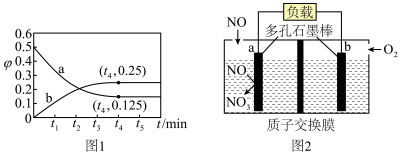
①a电极的电极反应式为
②电池工作一段时间,反应消耗了标准状况下
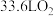 ,理论上负极区溶液增加的质量为
,理论上负极区溶液增加的质量为
您最近半年使用:0次
名校
4 . 25℃下,分别向体积均为1L的容器甲(恒温)、容器乙(绝热)中加入2molA和2molB,发生反应 ,两容器中A的转化率随时间的变化如图.下列说法正确的是
,两容器中A的转化率随时间的变化如图.下列说法正确的是
 ,两容器中A的转化率随时间的变化如图.下列说法正确的是
,两容器中A的转化率随时间的变化如图.下列说法正确的是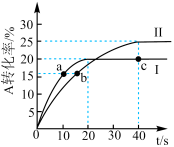
A.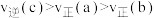 |
| B.曲线Ⅰ代表容器乙中A的转化率随时间变化 |
C.0~40s内,曲线Ⅱ中C的反应速率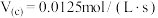 |
| D.容器乙达平衡后,缩小容器体积,达新平衡后C的物质的量增大 |
您最近半年使用:0次
解题方法
5 . 体积均为2L的多个恒容密闭容器,分别充入1mol CO(g)和1mol  (g)发生反应
(g)发生反应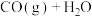

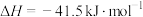 ,在不同温度下反应50s,测得正、逆反应的平衡常数的自然对数
,在不同温度下反应50s,测得正、逆反应的平衡常数的自然对数 (
( 或
或 )、
)、 体积分数与热力学温度的倒数关系如图所示,下列说法错误的是
体积分数与热力学温度的倒数关系如图所示,下列说法错误的是
 (g)发生反应
(g)发生反应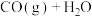

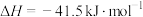 ,在不同温度下反应50s,测得正、逆反应的平衡常数的自然对数
,在不同温度下反应50s,测得正、逆反应的平衡常数的自然对数 (
( 或
或 )、
)、 体积分数与热力学温度的倒数关系如图所示,下列说法错误的是
体积分数与热力学温度的倒数关系如图所示,下列说法错误的是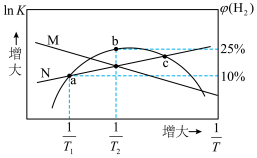
A.曲线N表示 的变化情况 的变化情况 |
B.0~50s,a点对应容器中的反应的平均速率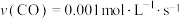 |
| C.b点时一定处于平衡状态 |
D.c点时, |
您最近半年使用:0次
解题方法
6 . 近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨。
 .在
.在 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:
反应a:

反应b:
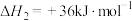
反应c: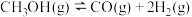

(1)已知反应b中相关化学键键能数据如下表:
计算:x=___________  ,
,
___________  。
。
(2)恒温恒容时,下列能说明反应a一定达到平衡状态的是___________(填标号)。
(3)在催化剂作用下,将物质的量之比为1:2的 和
和 的混合气体充入一恒容密闭容器中发生反应a、b,已知反应b的反应速率
的混合气体充入一恒容密闭容器中发生反应a、b,已知反应b的反应速率 ,
, ,
, 、
、 为速率常数,x为物质的量分数。
为速率常数,x为物质的量分数。
①平衡时, 转化率为60%,
转化率为60%, 和
和 的物质的量之比为1:1,若反应b的
的物质的量之比为1:1,若反应b的 ,则平衡
,则平衡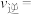
___________  。
。
②Arrhenius经验公式为 ,其中
,其中 为活化能,T为热力学温度,k为速率常数,R和C为常数,则
为活化能,T为热力学温度,k为速率常数,R和C为常数,则
___________  (用含
(用含 、
、 、T、R的代数式表示)。
、T、R的代数式表示)。
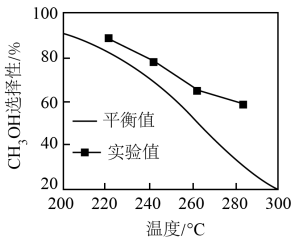
(4)其他条件相同时,反应温度对 选择性的影响如下图所示。由图可知,温度相同时
选择性的影响如下图所示。由图可知,温度相同时 选择性的实验值略高于其平衡值,可能的原因是
选择性的实验值略高于其平衡值,可能的原因是___________ 。(已知 的选择性
的选择性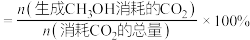 )
) .利用甲醇分解制取烯烃,涉及如下反应:
.利用甲醇分解制取烯烃,涉及如下反应:
a.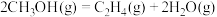
b.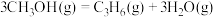
c.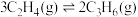
(5)恒压条件下,平衡体系中各物质的量分数随温度变化如图所示。已知650K时, ,平衡体系总压强为p,则650K反应c的平衡常数
,平衡体系总压强为p,则650K反应c的平衡常数
___________ 。
 .在
.在 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:反应a:


反应b:

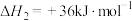
反应c:
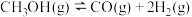

(1)已知反应b中相关化学键键能数据如下表:
| 化学键 | H-H | C=O | C≡O | H-O |
 | x | 803 | 1076 | 465 |
 ,
,
 。
。(2)恒温恒容时,下列能说明反应a一定达到平衡状态的是___________(填标号)。
A. | B.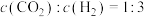 |
| C.混合气体的密度不再发生变化 | D.混合气体中 的百分含量保持不变 的百分含量保持不变 |
(3)在催化剂作用下,将物质的量之比为1:2的
 和
和 的混合气体充入一恒容密闭容器中发生反应a、b,已知反应b的反应速率
的混合气体充入一恒容密闭容器中发生反应a、b,已知反应b的反应速率 ,
, ,
, 、
、 为速率常数,x为物质的量分数。
为速率常数,x为物质的量分数。①平衡时,
 转化率为60%,
转化率为60%, 和
和 的物质的量之比为1:1,若反应b的
的物质的量之比为1:1,若反应b的 ,则平衡
,则平衡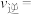
 。
。②Arrhenius经验公式为
 ,其中
,其中 为活化能,T为热力学温度,k为速率常数,R和C为常数,则
为活化能,T为热力学温度,k为速率常数,R和C为常数,则
 (用含
(用含 、
、 、T、R的代数式表示)。
、T、R的代数式表示)。(4)其他条件相同时,反应温度对
 选择性的影响如下图所示。由图可知,温度相同时
选择性的影响如下图所示。由图可知,温度相同时 选择性的实验值略高于其平衡值,可能的原因是
选择性的实验值略高于其平衡值,可能的原因是 的选择性
的选择性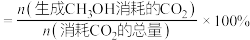 )
)
 .利用甲醇分解制取烯烃,涉及如下反应:
.利用甲醇分解制取烯烃,涉及如下反应:a.
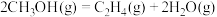
b.
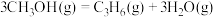
c.
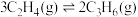
(5)恒压条件下,平衡体系中各物质的量分数随温度变化如图所示。已知650K时,
 ,平衡体系总压强为p,则650K反应c的平衡常数
,平衡体系总压强为p,则650K反应c的平衡常数

您最近半年使用:0次
7 . 回收利用 合成化工制成品是实现碳中和重要途径之一、利用二氧化碳合成二甲醚
合成化工制成品是实现碳中和重要途径之一、利用二氧化碳合成二甲醚 (DMC)的主要反应有:
(DMC)的主要反应有:
Ⅰ.
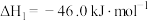
Ⅱ.
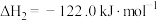
(1) 和
和 为原料制备气态
为原料制备气态 和水蒸气的热化学方程式是
和水蒸气的热化学方程式是_______ 。
(2)对于基元反应 ,若升高反应温度,平衡常数K
,若升高反应温度,平衡常数K_______ (填“增大”、“减小”或“不变”);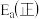
_______ 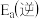 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
已知:阿伦尼乌斯经验公式为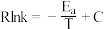 ,其中:
,其中: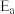 为正、逆反应的活化能,k为正、逆反应速率常数,R和C为常数。某实验小组依据实验数据获得如图曲线。曲线中表示正反应速率的是
为正、逆反应的活化能,k为正、逆反应速率常数,R和C为常数。某实验小组依据实验数据获得如图曲线。曲线中表示正反应速率的是_______ (填“m”或“n”)。
 、
、
 ,同时发生上述两个反应,装置中压强p随着时间t变化如下表:
,同时发生上述两个反应,装置中压强p随着时间t变化如下表:
①0~2min,反应Ⅱ的化学反应速率
_______  ,若其他条件不变,向该体系中充入
,若其他条件不变,向该体系中充入
 ,则
,则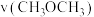
_______ (填“增大”、“减小”或“不变”)。
②平衡时测得水蒸气分压 ,反应Ⅱ生成
,反应Ⅱ生成 的选择性为
的选择性为_______ ( 选择性
选择性 ,保留1位小数)。
,保留1位小数)。
③计算反应Ⅰ的压强平衡常数
_______ (写计算表达式)。
(4)“直接二甲醚( )燃料电池”被称为绿色电源,其工作原理如图所示,写出A电极的电极反应式
)燃料电池”被称为绿色电源,其工作原理如图所示,写出A电极的电极反应式_______ 。
 合成化工制成品是实现碳中和重要途径之一、利用二氧化碳合成二甲醚
合成化工制成品是实现碳中和重要途径之一、利用二氧化碳合成二甲醚 (DMC)的主要反应有:
(DMC)的主要反应有:Ⅰ.

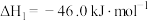
Ⅱ.

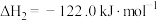
(1)
 和
和 为原料制备气态
为原料制备气态 和水蒸气的热化学方程式是
和水蒸气的热化学方程式是(2)对于基元反应
 ,若升高反应温度,平衡常数K
,若升高反应温度,平衡常数K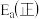
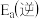 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。已知:阿伦尼乌斯经验公式为
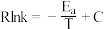 ,其中:
,其中: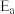 为正、逆反应的活化能,k为正、逆反应速率常数,R和C为常数。某实验小组依据实验数据获得如图曲线。曲线中表示正反应速率的是
为正、逆反应的活化能,k为正、逆反应速率常数,R和C为常数。某实验小组依据实验数据获得如图曲线。曲线中表示正反应速率的是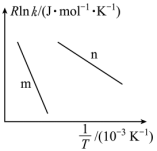

 、
、
 ,同时发生上述两个反应,装置中压强p随着时间t变化如下表:
,同时发生上述两个反应,装置中压强p随着时间t变化如下表:
| 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 16 | 13.4 | 12.8 | 12.4 | 12.2 | 12 | 12 |

 ,若其他条件不变,向该体系中充入
,若其他条件不变,向该体系中充入
 ,则
,则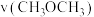
②平衡时测得水蒸气分压
 ,反应Ⅱ生成
,反应Ⅱ生成 的选择性为
的选择性为 选择性
选择性 ,保留1位小数)。
,保留1位小数)。③计算反应Ⅰ的压强平衡常数

(4)“直接二甲醚(
 )燃料电池”被称为绿色电源,其工作原理如图所示,写出A电极的电极反应式
)燃料电池”被称为绿色电源,其工作原理如图所示,写出A电极的电极反应式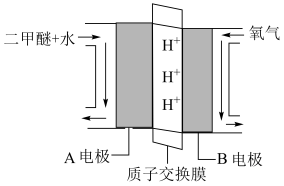
您最近半年使用:0次
解题方法
8 . 金属氧化物催化氧化制备苯甲醛是近年来的研究热点。以 为催化剂,苯乙烯、
为催化剂,苯乙烯、 为原料制备苯甲醛涉及的主要反应有:
为原料制备苯甲醛涉及的主要反应有:
(1)反应iii的
_______  。
。
(2)根据阿累尼乌斯方程 (A为指前因子,
(A为指前因子, 为活化能),
为活化能),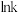 与
与 呈线性关系。据图1可知反应i的活化能
呈线性关系。据图1可知反应i的活化能_______ 反应ⅱ的活化能。(填“>”“=”或“<”) ,苯乙烯的转化率下降,可能的原因是
,苯乙烯的转化率下降,可能的原因是_______ 。

(4) 的催化反应机理如下图所示:
的催化反应机理如下图所示:_______ 。(填序号)
(5)在 催化下,甲苯可以实现气相氧化制备苯甲醛。
催化下,甲苯可以实现气相氧化制备苯甲醛。
(8)
 时,向
时,向 密闭容器中充入
密闭容器中充入 甲苯蒸气和
甲苯蒸气和 ,起始压强为
,起始压强为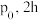 后反应达平衡时容器内气体总物质的量为
后反应达平衡时容器内气体总物质的量为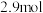 ,甲苯的转化率为
,甲苯的转化率为 。则甲苯的平均反应速率为
。则甲苯的平均反应速率为_______  ,主反应的
,主反应的
_______ ( 为平衡分压代替平衡浓度的平衡常数,气体平衡分压=总压×该气体物质的量分数,计算结果保留三位有效数字)。
为平衡分压代替平衡浓度的平衡常数,气体平衡分压=总压×该气体物质的量分数,计算结果保留三位有效数字)。
 为催化剂,苯乙烯、
为催化剂,苯乙烯、 为原料制备苯甲醛涉及的主要反应有:
为原料制备苯甲醛涉及的主要反应有:反应i: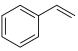 (l)+2H2O2(l)→
(l)+2H2O2(l)→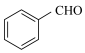 (l)+HCHO(l)+2H2O(l)
(l)+HCHO(l)+2H2O(l)
反应ii: (l)+H2O2(l)→
(l)+H2O2(l)→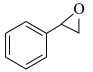 (l)+H2O(l)
(l)+H2O(l)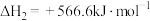
反应iii: (l)+H2O2(l)→
(l)+H2O2(l)→ (l)+HCHO(l)+H2O(l)
(l)+HCHO(l)+H2O(l)
(1)反应iii的

 。
。(2)根据阿累尼乌斯方程
 (A为指前因子,
(A为指前因子, 为活化能),
为活化能),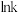 与
与 呈线性关系。据图1可知反应i的活化能
呈线性关系。据图1可知反应i的活化能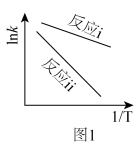
 ,苯乙烯的转化率下降,可能的原因是
,苯乙烯的转化率下降,可能的原因是
(4)
 的催化反应机理如下图所示:
的催化反应机理如下图所示: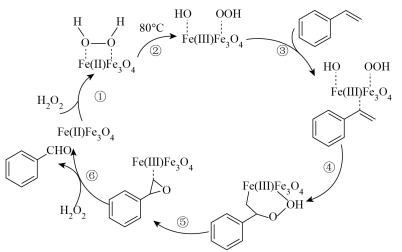
(5)在
 催化下,甲苯可以实现气相氧化制备苯甲醛。
催化下,甲苯可以实现气相氧化制备苯甲醛。(6)主反应: +O2→
+O2→ +H2O
+H2O
副反应:2 +O2→2
+O2→2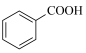
(8)
 时,向
时,向 密闭容器中充入
密闭容器中充入 甲苯蒸气和
甲苯蒸气和 ,起始压强为
,起始压强为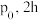 后反应达平衡时容器内气体总物质的量为
后反应达平衡时容器内气体总物质的量为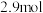 ,甲苯的转化率为
,甲苯的转化率为 。则甲苯的平均反应速率为
。则甲苯的平均反应速率为 ,主反应的
,主反应的
 为平衡分压代替平衡浓度的平衡常数,气体平衡分压=总压×该气体物质的量分数,计算结果保留三位有效数字)。
为平衡分压代替平衡浓度的平衡常数,气体平衡分压=总压×该气体物质的量分数,计算结果保留三位有效数字)。
您最近半年使用:0次
解题方法
9 . 乙醇因其含氢量高、毒性低、价格低廉且来源广泛,成为理想的液态储氢载体之一。乙醇―水催化重整可获得 ,其主要反应为:
,其主要反应为:
Ⅰ.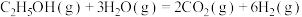

Ⅱ.

回答下列问题:
(1)已知:298K时,相关物质的相对能量如下表:
则a=___________ 。
(2)在恒温恒容条件下,投入1mol 和3mol
和3mol 发生反应
发生反应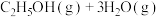
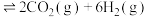 ,下列情况表明该反应达到平衡状态的是___________(填标号)。
,下列情况表明该反应达到平衡状态的是___________(填标号)。
(3)科学家研究了Grubbs催化剂作用于乙醇水溶液重整产氢的反应,测得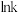 (k为速率常数)与反应温度倒数(
(k为速率常数)与反应温度倒数( )的相关关系及线性拟合如图1所示。请分析该反应的k随反应温度T的变化关系:
)的相关关系及线性拟合如图1所示。请分析该反应的k随反应温度T的变化关系:___________ 。 下,
下,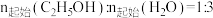 时,若仅考虑以上反应Ⅰ和Ⅱ,平衡时
时,若仅考虑以上反应Ⅰ和Ⅱ,平衡时 和CO的选择性及
和CO的选择性及 的产率随温度的变化如图2所示。
的产率随温度的变化如图2所示。 的选择性
的选择性
①图中表示 产率随温度变化的曲线是
产率随温度变化的曲线是___________ (填字母),判断依据是___________ 。
②一定温度下,加入 可以提高平衡时
可以提高平衡时 的产率,其原因是
的产率,其原因是___________ 。
(5)向一容积为2L的恒容密闭容器中通入2mol 和6mol
和6mol ,一定温度下发生反应
,一定温度下发生反应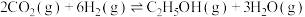 。若起始时气体的总压为p Pa,20min时达到平衡状态,测得
。若起始时气体的总压为p Pa,20min时达到平衡状态,测得 的物质的量分数为12.5%。
的物质的量分数为12.5%。
①平衡时气体的总压为___________ Pa(用含p的分数表示,需化简)。
②0~20min内,用 浓度的变化表示的平均反应速率
浓度的变化表示的平均反应速率
___________ ;该温度下,上述反应的平衡常数
___________ 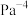 (用含p的分数表示,需化简;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用含p的分数表示,需化简;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 ,其主要反应为:
,其主要反应为:Ⅰ.
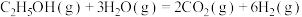

Ⅱ.


回答下列问题:
(1)已知:298K时,相关物质的相对能量如下表:
| 物质 |  |  |  |  |  |
相对能量/( ) ) | ―242 | ―393 | 0 | ―110 | a |
(2)在恒温恒容条件下,投入1mol
 和3mol
和3mol 发生反应
发生反应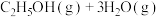
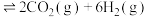 ,下列情况表明该反应达到平衡状态的是___________(填标号)。
,下列情况表明该反应达到平衡状态的是___________(填标号)。| A.混合气体的密度保持不变 | B.混合气体的总压强保持不变 |
| C.混合气体的平均摩尔质量保持不变 | D.产物的浓度之比保持不变 |
(3)科学家研究了Grubbs催化剂作用于乙醇水溶液重整产氢的反应,测得
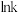 (k为速率常数)与反应温度倒数(
(k为速率常数)与反应温度倒数( )的相关关系及线性拟合如图1所示。请分析该反应的k随反应温度T的变化关系:
)的相关关系及线性拟合如图1所示。请分析该反应的k随反应温度T的变化关系: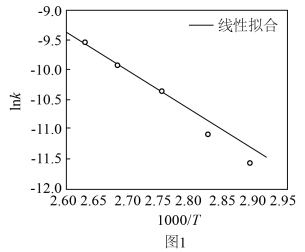
 下,
下,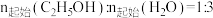 时,若仅考虑以上反应Ⅰ和Ⅱ,平衡时
时,若仅考虑以上反应Ⅰ和Ⅱ,平衡时 和CO的选择性及
和CO的选择性及 的产率随温度的变化如图2所示。
的产率随温度的变化如图2所示。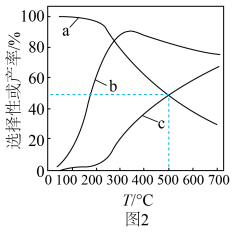
 的选择性
的选择性
①图中表示
 产率随温度变化的曲线是
产率随温度变化的曲线是②一定温度下,加入
 可以提高平衡时
可以提高平衡时 的产率,其原因是
的产率,其原因是(5)向一容积为2L的恒容密闭容器中通入2mol
 和6mol
和6mol ,一定温度下发生反应
,一定温度下发生反应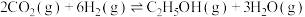 。若起始时气体的总压为p Pa,20min时达到平衡状态,测得
。若起始时气体的总压为p Pa,20min时达到平衡状态,测得 的物质的量分数为12.5%。
的物质的量分数为12.5%。①平衡时气体的总压为
②0~20min内,用
 浓度的变化表示的平均反应速率
浓度的变化表示的平均反应速率

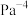 (用含p的分数表示,需化简;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用含p的分数表示,需化简;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
您最近半年使用:0次
10 . 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图示:________ 。
(2)若上述反应中X、Y、Z分别为 、
、 、
、 ,某温度下,在容积恒定为2.0L的密闭容器中充入
,某温度下,在容积恒定为2.0L的密闭容器中充入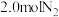 和
和 ,一段时间后反应达平衡状态,实验数据如表所示:
,一段时间后反应达平衡状态,实验数据如表所示:
0~50s内的平均反应速率
________ 。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成 过程中放出46kJ的热量。则N≡N的键能为
过程中放出46kJ的热量。则N≡N的键能为________ kJ/mol。
(4)CO与 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池的结构示意图如下。
构成的质子交换膜燃料电池的结构示意图如下。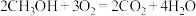 ,则c电极是
,则c电极是________ (填“正极”或“负极”)。若外电路中转移2mol电子,则上述燃料电池所消耗的 在标准状况下的体积为
在标准状况下的体积为________ L。
(5)下列反应中,属于吸热反应的是________ (填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥ 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应

(2)若上述反应中X、Y、Z分别为
 、
、 、
、 ,某温度下,在容积恒定为2.0L的密闭容器中充入
,某温度下,在容积恒定为2.0L的密闭容器中充入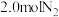 和
和 ,一段时间后反应达平衡状态,实验数据如表所示:
,一段时间后反应达平衡状态,实验数据如表所示:t/s | 0 | 50 | 150 | 250 | 350 |
| 0 | 0.36 | 0.48 | 0.50 | 0.50 |

(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成
 过程中放出46kJ的热量。则N≡N的键能为
过程中放出46kJ的热量。则N≡N的键能为(4)CO与
 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池的结构示意图如下。
构成的质子交换膜燃料电池的结构示意图如下。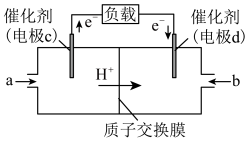
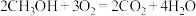 ,则c电极是
,则c电极是 在标准状况下的体积为
在标准状况下的体积为(5)下列反应中,属于吸热反应的是
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥
 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应
您最近半年使用:0次