近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨。
 .在
.在 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:
反应a:

反应b:
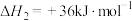
反应c: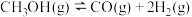

(1)已知反应b中相关化学键键能数据如下表:
计算:x=___________  ,
,
___________  。
。
(2)恒温恒容时,下列能说明反应a一定达到平衡状态的是___________(填标号)。
(3)在催化剂作用下,将物质的量之比为1:2的 和
和 的混合气体充入一恒容密闭容器中发生反应a、b,已知反应b的反应速率
的混合气体充入一恒容密闭容器中发生反应a、b,已知反应b的反应速率 ,
,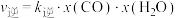 ,
, 、
、 为速率常数,x为物质的量分数。
为速率常数,x为物质的量分数。
①平衡时, 转化率为60%,
转化率为60%, 和
和 的物质的量之比为1:1,若反应b的
的物质的量之比为1:1,若反应b的 ,则平衡
,则平衡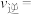
___________  。
。
②Arrhenius经验公式为 ,其中
,其中 为活化能,T为热力学温度,k为速率常数,R和C为常数,则
为活化能,T为热力学温度,k为速率常数,R和C为常数,则
___________  (用含
(用含 、
、 、T、R的代数式表示)。
、T、R的代数式表示)。
(4)其他条件相同时,反应温度对 选择性的影响如下图所示。由图可知,温度相同时
选择性的影响如下图所示。由图可知,温度相同时 选择性的实验值略高于其平衡值,可能的原因是
选择性的实验值略高于其平衡值,可能的原因是___________ 。(已知 的选择性
的选择性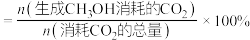 )
) .利用甲醇分解制取烯烃,涉及如下反应:
.利用甲醇分解制取烯烃,涉及如下反应:
a.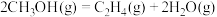
b.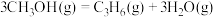
c.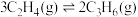
(5)恒压条件下,平衡体系中各物质的量分数随温度变化如图所示。已知650K时, ,平衡体系总压强为p,则650K反应c的平衡常数
,平衡体系总压强为p,则650K反应c的平衡常数
___________ 。
 .在
.在 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:反应a:


反应b:

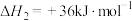
反应c:
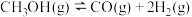

(1)已知反应b中相关化学键键能数据如下表:
| 化学键 | H-H | C=O | C≡O | H-O |
 | x | 803 | 1076 | 465 |
 ,
,
 。
。(2)恒温恒容时,下列能说明反应a一定达到平衡状态的是___________(填标号)。
A. |
B.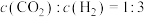 |
| C.混合气体的密度不再发生变化 |
D.混合气体中 的百分含量保持不变 的百分含量保持不变 |
 和
和 的混合气体充入一恒容密闭容器中发生反应a、b,已知反应b的反应速率
的混合气体充入一恒容密闭容器中发生反应a、b,已知反应b的反应速率 ,
,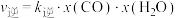 ,
, 、
、 为速率常数,x为物质的量分数。
为速率常数,x为物质的量分数。①平衡时,
 转化率为60%,
转化率为60%, 和
和 的物质的量之比为1:1,若反应b的
的物质的量之比为1:1,若反应b的 ,则平衡
,则平衡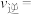
 。
。②Arrhenius经验公式为
 ,其中
,其中 为活化能,T为热力学温度,k为速率常数,R和C为常数,则
为活化能,T为热力学温度,k为速率常数,R和C为常数,则
 (用含
(用含 、
、 、T、R的代数式表示)。
、T、R的代数式表示)。(4)其他条件相同时,反应温度对
 选择性的影响如下图所示。由图可知,温度相同时
选择性的影响如下图所示。由图可知,温度相同时 选择性的实验值略高于其平衡值,可能的原因是
选择性的实验值略高于其平衡值,可能的原因是 的选择性
的选择性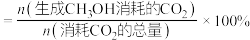 )
)
 .利用甲醇分解制取烯烃,涉及如下反应:
.利用甲醇分解制取烯烃,涉及如下反应:a.
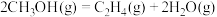
b.
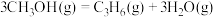
c.
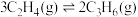
(5)恒压条件下,平衡体系中各物质的量分数随温度变化如图所示。已知650K时,
 ,平衡体系总压强为p,则650K反应c的平衡常数
,平衡体系总压强为p,则650K反应c的平衡常数
更新时间:2024-05-27 18:20:45
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】氢气、一氧化碳、二氧化碳是最常见的气体。回答下列问题:
(1)宇航员呼吸产生的CO2用镍催化剂反应处理,实现空间站中的O2循环利用。
镍催化剂反应:CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH
已知:①H2(g)+ O2(g)=H2O(g) ΔH=-akJ·mol-1,
O2(g)=H2O(g) ΔH=-akJ·mol-1,
②CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-bkJ·mol-1,
③H2O(g)=H2O(l) ΔH=-ckJ·mol-1
则镍催化剂反应的ΔH=_______ kJ·mol-1;
(2)向1L恒容密闭容器中加入2molCO、4molH2,在适当的催化剂和一定条件作用下发生反应:2CO(g)+4H2(g)⇌CH3OCH3(l)+H2O(l) ΔH=+71kJ/mol
①该反应_______ 自发进行(填“高温”、“低温”或“不能”)。其判断理由是_______ 。
②下列叙述能说明此反应达到平衡状态的是_______ 。
a.混合气体的平均相对分子质量保持不变
b.混合气体的密度保持不变
c.CO和H2的体积分数保持不变
d.CO和H2的转化率相等
e.气体总压强保持不变
f.1molCO生成的同时有1molO-H键断裂
(3)已知CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0在一定条件下,某反应过程中部分数据如下表:
①0~5min内,用H2O(g)表示的化学反应速率v(H2O)=_______ mol/(L·min)
②达到平衡时,该反应的平衡常数K=_______ (用分数表示),平衡时H2的转化率是_______ 。
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为2.8mol,则T1_______ T2(填“>”“<”或“=”),理由是_______ 。在其他条件不变的情况下,若30min时向容器中再充入1molCO2(g)和1molH2O(g),则平衡_______ 移动(填“正向”“逆向”或“不”)。
(1)宇航员呼吸产生的CO2用镍催化剂反应处理,实现空间站中的O2循环利用。
镍催化剂反应:CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH
已知:①H2(g)+
 O2(g)=H2O(g) ΔH=-akJ·mol-1,
O2(g)=H2O(g) ΔH=-akJ·mol-1,②CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-bkJ·mol-1,
③H2O(g)=H2O(l) ΔH=-ckJ·mol-1
则镍催化剂反应的ΔH=
(2)向1L恒容密闭容器中加入2molCO、4molH2,在适当的催化剂和一定条件作用下发生反应:2CO(g)+4H2(g)⇌CH3OCH3(l)+H2O(l) ΔH=+71kJ/mol
①该反应
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变
b.混合气体的密度保持不变
c.CO和H2的体积分数保持不变
d.CO和H2的转化率相等
e.气体总压强保持不变
f.1molCO生成的同时有1molO-H键断裂
(3)已知CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0在一定条件下,某反应过程中部分数据如下表:
| 反应条件 | 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 恒温恒容 (T1℃、2L) | 0min | 2 | 6 | 0 | 0 |
| 5min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 |
②达到平衡时,该反应的平衡常数K=
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为2.8mol,则T1
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】尿素是氮肥中含氮量最高的品种,是良好的中性速效肥料,且不会影响土质。由氨和二氧化碳合成尿素的总反应式为:2NH3(g)+CO(g)⇌CO(NH2)2(l)+H2O(g) ΔH=-103.7kJ/mol。回答下列问题:
(1)关于合成尿素的反应机理有多种说法,一般认为该反应是分两步进行的:
a.2NH3(g)+CO2(g)⇌NH2COONH4(1) ΔH1=-119.2k.J/mol
b.NH2COONH4(l)⇌CO(NH2)2(l)+H2O(g) ΔH2
①ΔH2=_______ 。
②已知反应b的活化能远大于反应a的,则该反应机理下的决速步骤是反应_______ (填“a”或“b”)。
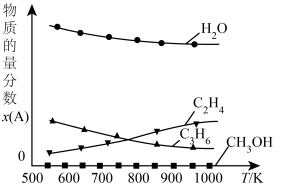
③如图为某工厂的尿素合成塔内的轴向温度测定数据,根据图示数据可以推断,合成塔下部1/3的容积内都在进行反应_______ (填“a”或“b”)。
(2)反应物料氨与二氧化碳的物质的量比称为氨碳比(下文中水碳比同理),氨碳比对尿素平衡产率的影响如下表所示(恒压20MPa下测定)
由表可见,氨碳比提高,尿素的平衡产率也提高,因为过剩的氨气既可以促进二氧化碳的转化,又能够_______ ,皆可使平衡向着生成尿素的方向移动。
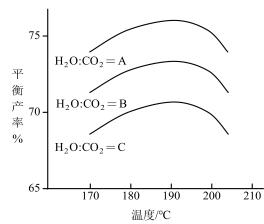
(3)如图为尿素平衡产率与温度和水碳比的关系,则图中水碳比A、B、C由大到小的关系为_______ 。由图可见,相同水碳比时平衡产率开始随温度升高而增大,若继续升温,平衡产率会逐渐下降,试结合分步的反应机理说明其中的原因_______ 。
(4)实验室模拟尿素的合成,恒定温度为160℃,在一容积可变的容器中,按照氨碳比为5充入原料气,恒定压强为20MPa进行反应直到平衡。
①以下叙述能说明反应达到平衡状态的是_______
a.容器中氨碳比保持不变
b.气体密度保持不变
c.气体平均相对分子质量保持不变
②计算该温度下的压强平衡常数Kp=_______ MPa-2(以分压表示,分压=总压×气体物质的量分数,结果保留三位小数)。
(1)关于合成尿素的反应机理有多种说法,一般认为该反应是分两步进行的:
a.2NH3(g)+CO2(g)⇌NH2COONH4(1) ΔH1=-119.2k.J/mol
b.NH2COONH4(l)⇌CO(NH2)2(l)+H2O(g) ΔH2
①ΔH2=
②已知反应b的活化能远大于反应a的,则该反应机理下的决速步骤是反应
③如图为某工厂的尿素合成塔内的轴向温度测定数据,根据图示数据可以推断,合成塔下部1/3的容积内都在进行反应

(2)反应物料氨与二氧化碳的物质的量比称为氨碳比(下文中水碳比同理),氨碳比对尿素平衡产率的影响如下表所示(恒压20MPa下测定)
| 温度/℃ | NH3:CO2物质的量之比 | |||
| 2 | 3 | 4 | 5 | |
| 140 | 43 | 55 | 62 | 73 |
| 150 | 45 | 58 | 67 | 78 |
| 160 | 46 | 61 | 70 | 80 |
| 180 | 49 | 62 | 71 | 81 |
(3)如图为尿素平衡产率与温度和水碳比的关系,则图中水碳比A、B、C由大到小的关系为

(4)实验室模拟尿素的合成,恒定温度为160℃,在一容积可变的容器中,按照氨碳比为5充入原料气,恒定压强为20MPa进行反应直到平衡。
①以下叙述能说明反应达到平衡状态的是
a.容器中氨碳比保持不变
b.气体密度保持不变
c.气体平均相对分子质量保持不变
②计算该温度下的压强平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】I、(1)普通锌锰干电池的结构如图所示。回答下列问题。

①电池中电解质溶液为________ 。
②负极反应式为______________________________________ 。
③放电时NH 向
向________ (填“正极”或“负极”)移动。
(2)废电池中的锌皮常用于实验室制氢气,废锌皮和纯锌粒分别与同浓度的稀硫酸反应,产生氢气速率较大的是________ ,若用过量的纯锌粒与一定量的稀硫酸反应,为了加快反应速率又不影响产生氢气的量,下列措施可行的是________ (填序号)。
A.微热 B.加入适量氧化铜 C.加入少量硫酸铜溶液
D.加水 E.加入少量氢氧化钡溶液
II、一定条件下,H2O2在水溶液中发生分解反应:2H2O2 2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:
2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:
(1)H2O2的分解反应________ 氧化还原反应(填“是”或“不是”)。
(2)该分解反应0~20 min的平均反应速率v(H2O2)为________ mol/(L·min)。
(3) 加入0.1 mol的MnO2粉末于50 mL过氧化氢的溶液中(密度为1.1 g/mL),在标准状况下放出气体的体积和时间的关系如图所示,反应放出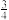 气体所需要的时间为
气体所需要的时间为________ ;A、B、C、D四点化学反应速率快慢的顺序为________ 。

(4)由合成气(组成为H2、CO、和少量CO2)直接制备二甲醚,其中主要过程包括以下四个反应:
甲醇合成反应:①CO(g)+ 2H2(g)=CH3OH(g) ΔH1=-90.1 kJ·mol-1
②CO2(g)+ 3H2(g)=CH3OH(g)+H2O(g) ΔH2=-49.0 kJ·mol-1
水煤气变换反应:③CO(g) + H2O (g)=CO2(g)+H2(g) ΔH3=-41.1 kJ·mol-1
二甲醚合成反应: ④2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH4=-24.5 kJ·mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为________________

①电池中电解质溶液为
②负极反应式为
③放电时NH
 向
向(2)废电池中的锌皮常用于实验室制氢气,废锌皮和纯锌粒分别与同浓度的稀硫酸反应,产生氢气速率较大的是
A.微热 B.加入适量氧化铜 C.加入少量硫酸铜溶液
D.加水 E.加入少量氢氧化钡溶液
II、一定条件下,H2O2在水溶液中发生分解反应:2H2O2
 2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:
2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:t/min | 0 | 20 | 40 | 60 | 80 |
c(H2O2)/(mol/L) | 0.80 | 0.40 | 0.20 | 0.10 | 0.05 |
(2)该分解反应0~20 min的平均反应速率v(H2O2)为
(3) 加入0.1 mol的MnO2粉末于50 mL过氧化氢的溶液中(密度为1.1 g/mL),在标准状况下放出气体的体积和时间的关系如图所示,反应放出
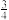 气体所需要的时间为
气体所需要的时间为
(4)由合成气(组成为H2、CO、和少量CO2)直接制备二甲醚,其中主要过程包括以下四个反应:
甲醇合成反应:①CO(g)+ 2H2(g)=CH3OH(g) ΔH1=-90.1 kJ·mol-1
②CO2(g)+ 3H2(g)=CH3OH(g)+H2O(g) ΔH2=-49.0 kJ·mol-1
水煤气变换反应:③CO(g) + H2O (g)=CO2(g)+H2(g) ΔH3=-41.1 kJ·mol-1
二甲醚合成反应: ④2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH4=-24.5 kJ·mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】 在化工生产中有重要作用.天然气法合成
在化工生产中有重要作用.天然气法合成 相关反应如下:
相关反应如下:
反应I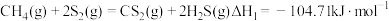
反应Ⅱ
(1) 、
、 随温度变化不大。温度不同时,反应体系中
随温度变化不大。温度不同时,反应体系中 不同。合成
不同。合成 总反应
总反应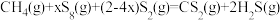 的
的 随温度T变化如图。
随温度T变化如图。
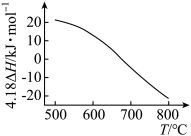
①

________  。
。
②为提高 平衡转化率,控制温度范围在
平衡转化率,控制温度范围在________ (填标号),理由是________ 。
A.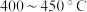 B.
B.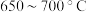 C.
C.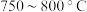 D.
D. 以上
以上
(2)合成 总反应中硫蒸气达到饱和时,反应时间t与
总反应中硫蒸气达到饱和时,反应时间t与 初始浓度
初始浓度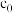 和
和 转化率
转化率 满足关系
满足关系 ,式中k为速率常数。
,式中k为速率常数。
① 、
、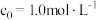 时,测得
时,测得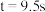 、
、 ,则
,则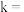
________ 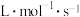 。
。
② 时,计划在
时,计划在 内转化率达
内转化率达 ,应控制初始浓度
,应控制初始浓度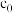 大于
大于________  。
。
(3)利用工业废气 替代硫磺矿生产
替代硫磺矿生产 的反应为
的反应为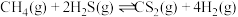 。反应物投料比采用
。反应物投料比采用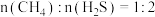 ,维持体系压强为
,维持体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
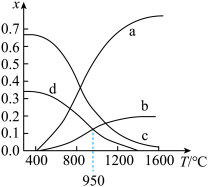
①图中表示 的曲线是
的曲线是________ (填“a”“b”“c”或“d”)。
② 时,该反应的
时,该反应的
________ (以分压表示,分压 总压
总压 物质的量分数)。
物质的量分数)。
③相比以硫磺矿为原料,使用 的优点是
的优点是________ ,缺点是________ 。
 在化工生产中有重要作用.天然气法合成
在化工生产中有重要作用.天然气法合成 相关反应如下:
相关反应如下:反应I
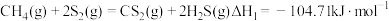
反应Ⅱ

(1)
 、
、 随温度变化不大。温度不同时,反应体系中
随温度变化不大。温度不同时,反应体系中 不同。合成
不同。合成 总反应
总反应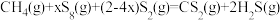 的
的 随温度T变化如图。
随温度T变化如图。
①


 。
。②为提高
 平衡转化率,控制温度范围在
平衡转化率,控制温度范围在A.
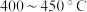 B.
B.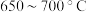 C.
C.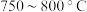 D.
D. 以上
以上(2)合成
 总反应中硫蒸气达到饱和时,反应时间t与
总反应中硫蒸气达到饱和时,反应时间t与 初始浓度
初始浓度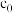 和
和 转化率
转化率 满足关系
满足关系 ,式中k为速率常数。
,式中k为速率常数。①
 、
、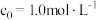 时,测得
时,测得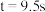 、
、 ,则
,则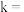
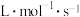 。
。②
 时,计划在
时,计划在 内转化率达
内转化率达 ,应控制初始浓度
,应控制初始浓度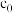 大于
大于 。
。(3)利用工业废气
 替代硫磺矿生产
替代硫磺矿生产 的反应为
的反应为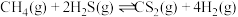 。反应物投料比采用
。反应物投料比采用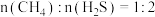 ,维持体系压强为
,维持体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
①图中表示
 的曲线是
的曲线是②
 时,该反应的
时,该反应的
 总压
总压 物质的量分数)。
物质的量分数)。③相比以硫磺矿为原料,使用
 的优点是
的优点是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】一定条件下,CO与水蒸气反应生成 和
和 的热化学方程式为
的热化学方程式为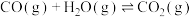
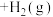 ,
, kJ·mol
kJ·mol 。
。
回答下列问题:
(1)已知1molC完全转化成水煤气(CO、 混合物)时吸收热量131.5kJ,则1molC与
混合物)时吸收热量131.5kJ,则1molC与 反应生成CO的焓变是
反应生成CO的焓变是___________ kJ·mol 。
。
(2)反应 达到平衡状态的标志是___________(填字母)。
达到平衡状态的标志是___________(填字母)。
(3)研究表明反应 的平衡常数随温度的变化如下表所示:
的平衡常数随温度的变化如下表所示:
在500℃下,CO和 的起始浓度均为2mol·L
的起始浓度均为2mol·L ,达到平衡时,CO的平衡转化率为
,达到平衡时,CO的平衡转化率为___________ 。
(4)在T℃、5MPa下,将0.1molCO与0.12mol 混合气体充入1L密闭容器发生反应,反应过程中
混合气体充入1L密闭容器发生反应,反应过程中 的物质的量浓度随时间的变化如图所示:
的物质的量浓度随时间的变化如图所示:

①在0~2min内,
___________ mol·L-1·min-1。
②T℃时该反应的平衡常数
___________ (压强代替浓度,分压=总压×物质的分数)。
③平衡后,若向容器中再充入0.2mol 和0.02mol
和0.02mol ,则再次平衡后容器内的压强与充入CO和
,则再次平衡后容器内的压强与充入CO和 前的压强比为
前的压强比为___________ 。
 和
和 的热化学方程式为
的热化学方程式为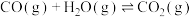
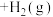 ,
, kJ·mol
kJ·mol 。
。回答下列问题:
(1)已知1molC完全转化成水煤气(CO、
 混合物)时吸收热量131.5kJ,则1molC与
混合物)时吸收热量131.5kJ,则1molC与 反应生成CO的焓变是
反应生成CO的焓变是 。
。(2)反应
 达到平衡状态的标志是___________(填字母)。
达到平衡状态的标志是___________(填字母)。| A.容器内压强不随时间变化 |
| B.容器内各物质的浓度不随时间变化 |
C.容器内CO、 的浓度之比为1:1 的浓度之比为1:1 |
D.单位时间消耗0.1molCO同时生成0.1mol |
 的平衡常数随温度的变化如下表所示:
的平衡常数随温度的变化如下表所示:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 15 | 9 | 5 |
在500℃下,CO和
 的起始浓度均为2mol·L
的起始浓度均为2mol·L ,达到平衡时,CO的平衡转化率为
,达到平衡时,CO的平衡转化率为(4)在T℃、5MPa下,将0.1molCO与0.12mol
 混合气体充入1L密闭容器发生反应,反应过程中
混合气体充入1L密闭容器发生反应,反应过程中 的物质的量浓度随时间的变化如图所示:
的物质的量浓度随时间的变化如图所示:
①在0~2min内,

②T℃时该反应的平衡常数

③平衡后,若向容器中再充入0.2mol
 和0.02mol
和0.02mol ,则再次平衡后容器内的压强与充入CO和
,则再次平衡后容器内的压强与充入CO和 前的压强比为
前的压强比为
您最近一年使用:0次
【推荐3】2023年9月23日晚,随着亚运会主火炬的点燃,第19届亚运会在杭州正式开幕。开幕式主火炬燃料创新使用零碳甲醇燃料,彰显了中国打造碳中和亚运会的成果。
I.甲醇作为火炬燃料亮相世界,为甲醇产业迎来了高光时刻,甲醇技术路线有望成为中国绿色能源重要组成部分。
目前,工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:
反应Ⅱ: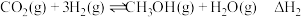
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)
(1)在一定条件下将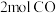 和
和 充入
充入 的密闭容器中发生反应Ⅰ,5分钟后达到平衡,测得
的密闭容器中发生反应Ⅰ,5分钟后达到平衡,测得 ,此段时间的反应速率(用
,此段时间的反应速率(用 表示)为
表示)为___________  。若此时再向容器中加入
。若此时再向容器中加入 、
、 、
、 各
各 ,则化学平衡
,则化学平衡___________ (填“正向”、“逆向”或“不”)移动。
(2)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是___________ 。
a.充入CO b.将 从体系中分离 c.升高温度 d.选用新型高效催化剂
从体系中分离 c.升高温度 d.选用新型高效催化剂
(3)一定温度下,在固定容积的密闭容器中发生反应Ⅱ,下列能判断反应达到平衡状态的是___________ 。
a.容器中的压强不再改变 b.混合气体的密度不再改变
c.混合气体的平均摩尔质量不再改变 d.消耗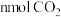 的同时生成
的同时生成
Ⅱ.近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨,二氧化碳加氢制甲醇为零碳甲醇的重要来源,在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:
Ⅰ.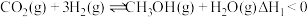
Ⅱ.
回答下列问题:
(4) 在催化剂作用下,将平均相对分子质量为16的
在催化剂作用下,将平均相对分子质量为16的 和
和 的混合气体充入一恒容密闭容器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v(正)
的混合气体充入一恒容密闭容器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v(正) (正)
(正)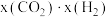 ,v(逆)
,v(逆) (逆)
(逆)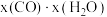 ,k(正)、k(逆)为速率常数,x为物质的量分数。
,k(正)、k(逆)为速率常数,x为物质的量分数。
①当 转化率达到
转化率达到 时,反应达到平衡状态,这时
时,反应达到平衡状态,这时 和
和 的平均相对分子质量为23,若反应Ⅱ的k(正)
的平均相对分子质量为23,若反应Ⅱ的k(正)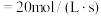 ,平衡时反应速率v(逆)
,平衡时反应速率v(逆)
___________ 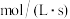 ;
;
②由实验测得,随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回16,原因是___________ 。
(5)其他条件相同时,反应温度对 选择性(转化为
选择性(转化为 的
的 在总转化量中的占比)的影响如图所示:
在总转化量中的占比)的影响如图所示:
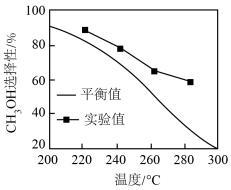
由图可知,温度相同时 选择性的实验值略高于其平衡值,可能的原因是
选择性的实验值略高于其平衡值,可能的原因是___________ 。
I.甲醇作为火炬燃料亮相世界,为甲醇产业迎来了高光时刻,甲醇技术路线有望成为中国绿色能源重要组成部分。
目前,工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:

反应Ⅱ:
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(1)在一定条件下将
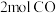 和
和 充入
充入 的密闭容器中发生反应Ⅰ,5分钟后达到平衡,测得
的密闭容器中发生反应Ⅰ,5分钟后达到平衡,测得 ,此段时间的反应速率(用
,此段时间的反应速率(用 表示)为
表示)为 。若此时再向容器中加入
。若此时再向容器中加入 、
、 、
、 各
各 ,则化学平衡
,则化学平衡(2)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是
a.充入CO b.将
 从体系中分离 c.升高温度 d.选用新型高效催化剂
从体系中分离 c.升高温度 d.选用新型高效催化剂(3)一定温度下,在固定容积的密闭容器中发生反应Ⅱ,下列能判断反应达到平衡状态的是
a.容器中的压强不再改变 b.混合气体的密度不再改变
c.混合气体的平均摩尔质量不再改变 d.消耗
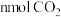 的同时生成
的同时生成
Ⅱ.近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨,二氧化碳加氢制甲醇为零碳甲醇的重要来源,在某
 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:Ⅰ.
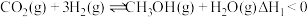
Ⅱ.

回答下列问题:
(4)
 在催化剂作用下,将平均相对分子质量为16的
在催化剂作用下,将平均相对分子质量为16的 和
和 的混合气体充入一恒容密闭容器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v(正)
的混合气体充入一恒容密闭容器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v(正) (正)
(正)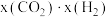 ,v(逆)
,v(逆) (逆)
(逆)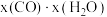 ,k(正)、k(逆)为速率常数,x为物质的量分数。
,k(正)、k(逆)为速率常数,x为物质的量分数。①当
 转化率达到
转化率达到 时,反应达到平衡状态,这时
时,反应达到平衡状态,这时 和
和 的平均相对分子质量为23,若反应Ⅱ的k(正)
的平均相对分子质量为23,若反应Ⅱ的k(正)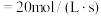 ,平衡时反应速率v(逆)
,平衡时反应速率v(逆)
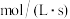 ;
;②由实验测得,随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回16,原因是
(5)其他条件相同时,反应温度对
 选择性(转化为
选择性(转化为 的
的 在总转化量中的占比)的影响如图所示:
在总转化量中的占比)的影响如图所示:
由图可知,温度相同时
 选择性的实验值略高于其平衡值,可能的原因是
选择性的实验值略高于其平衡值,可能的原因是
您最近一年使用:0次
【推荐1】在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系。
(1)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g)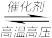 2NH3(g)。
2NH3(g)。
①合成氨的反应中的能量变化如图所示。
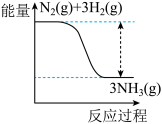
该反应是________ 反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量________ (填“大于”或“小于”)生成物化学键形成放出的总能量。
②在一定条件下,将一定量的N2和H2的混合气体充入某定容密闭容器中,一段时间后,下列叙述不能说明该反应达到平衡状态的是________ (填序号)。
A.容器中混合气体的密度不随时间变化
B.单位时间内断裂3molH-H键的同时断裂6molN-H键
C.N2、H2、NH3的物质的量之比为1:3:2
D.容器中混合气体的平均相对分子质量不随时间变化
(2)容器容积为1L,T2℃在起始体系中加入1molN2、3molH2,经过5min反应达到平衡时放出热量55.44kJ。保持容器体积和温度不变,若起始时向容器内放入2molN2和6molH2,达平衡后放出的热量为Q,则Q________ 110.88kJ(填“>”、“<”或“=”)。
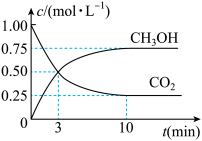
(3)目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。达平衡时容器内平衡时与起始时的压强之比
CH3OH(g)+H2O(g),在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。达平衡时容器内平衡时与起始时的压强之比________ 。
(4)有可逆反应Fe(s)+CO2(g) FeO(s)+CO(g)∆H>0。
FeO(s)+CO(g)∆H>0。
①若起始时把Fe和CO2放入体积固定的密闭容器中,CO2的起始浓度为2.0mol/L,某温度时达到平衡,此时容器中CO的浓度为1.0mol/L,则该温度下上述反应的平衡常数K=_____________ 。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件,升高温度,反应混合气体中CO2的物质的量分数_____________ 变化(选填“增大”、“减小”、“不变”)。
(1)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g)
 2NH3(g)。
2NH3(g)。①合成氨的反应中的能量变化如图所示。

该反应是
②在一定条件下,将一定量的N2和H2的混合气体充入某定容密闭容器中,一段时间后,下列叙述不能说明该反应达到平衡状态的是
A.容器中混合气体的密度不随时间变化
B.单位时间内断裂3molH-H键的同时断裂6molN-H键
C.N2、H2、NH3的物质的量之比为1:3:2
D.容器中混合气体的平均相对分子质量不随时间变化
(2)容器容积为1L,T2℃在起始体系中加入1molN2、3molH2,经过5min反应达到平衡时放出热量55.44kJ。保持容器体积和温度不变,若起始时向容器内放入2molN2和6molH2,达平衡后放出的热量为Q,则Q
(3)目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。达平衡时容器内平衡时与起始时的压强之比
CH3OH(g)+H2O(g),在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。达平衡时容器内平衡时与起始时的压强之比
(4)有可逆反应Fe(s)+CO2(g)
 FeO(s)+CO(g)∆H>0。
FeO(s)+CO(g)∆H>0。①若起始时把Fe和CO2放入体积固定的密闭容器中,CO2的起始浓度为2.0mol/L,某温度时达到平衡,此时容器中CO的浓度为1.0mol/L,则该温度下上述反应的平衡常数K=
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件,升高温度,反应混合气体中CO2的物质的量分数
您最近一年使用:0次
【推荐2】“绿水青山就是金山银山”。合理利用或转化汽车尾气中的NO、NO2等污染性气体是人们共同关注的课题:
(1)臭氧氧化法。烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知NO与O3反应过程的能量变化如图:

则反应3NO(g)+O3(g)=3NO2(g)的∆H=__ kJ·mol-1。
(2)活性炭还原法.有关反应为:C(s)+2NO(g) N2(g)+CO2(g)∆H=+172.5kJ·mol-1,一定温度下,向一个2L密闭容器中加入一定量的活性炭和2mol的NO反应。反应进行到10分钟时达到平衡,此时测得容器中NO和N2的体积比为2:1。则:
N2(g)+CO2(g)∆H=+172.5kJ·mol-1,一定温度下,向一个2L密闭容器中加入一定量的活性炭和2mol的NO反应。反应进行到10分钟时达到平衡,此时测得容器中NO和N2的体积比为2:1。则:
①10分钟内以CO2表示该反应的反应速率为__ mol·L-1min-1。
②下列说法能作为判断该反应达到化学平衡状态标志的是___ 。
a.NO的体积分数保持不变
b.某一时间内生成0.01molN2的同时也生成0.01molCO2
c.容器内气体总物质的量保持不变
d.容器内混合气体的密度保持不变
③此温度下,该反应的平衡常数为__ ,平衡时NO的转化率为__ 。
④20min时。只改变某一条件,反应重新达到平衡。平衡时测得c(NO)=0.4mol·L-1,(N2)=0.3mol·L-1,c(CO2)=0.3mol·L-1。则改变的条件是__ 。
(1)臭氧氧化法。烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知NO与O3反应过程的能量变化如图:

则反应3NO(g)+O3(g)=3NO2(g)的∆H=
(2)活性炭还原法.有关反应为:C(s)+2NO(g)
 N2(g)+CO2(g)∆H=+172.5kJ·mol-1,一定温度下,向一个2L密闭容器中加入一定量的活性炭和2mol的NO反应。反应进行到10分钟时达到平衡,此时测得容器中NO和N2的体积比为2:1。则:
N2(g)+CO2(g)∆H=+172.5kJ·mol-1,一定温度下,向一个2L密闭容器中加入一定量的活性炭和2mol的NO反应。反应进行到10分钟时达到平衡,此时测得容器中NO和N2的体积比为2:1。则:①10分钟内以CO2表示该反应的反应速率为
②下列说法能作为判断该反应达到化学平衡状态标志的是
a.NO的体积分数保持不变
b.某一时间内生成0.01molN2的同时也生成0.01molCO2
c.容器内气体总物质的量保持不变
d.容器内混合气体的密度保持不变
③此温度下,该反应的平衡常数为
④20min时。只改变某一条件,反应重新达到平衡。平衡时测得c(NO)=0.4mol·L-1,(N2)=0.3mol·L-1,c(CO2)=0.3mol·L-1。则改变的条件是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为___ 。利用反应6NO2+8NH3 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是___ L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ/mol;2NO(g)+O2(g)
2SO3(g) ΔH=-196.6kJ/mol;2NO(g)+O2(g) 2NO2(g) ΔH=-113.0kJ/mol;
2NO2(g) ΔH=-113.0kJ/mol;
①则反应NO2(g)+SO2(g) SO3(g)+NO(g) ΔH的ΔH=
SO3(g)+NO(g) ΔH的ΔH=___ kJ/mol。
②一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是___ 。
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1molSO3的同时生成1molNO2
③测得上述反应平衡时NO2与SO2的体积比为1:6,则平衡常数K=___ 。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g),ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。
CH3OH(g),ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。

该反应ΔH___ 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是___ 。
(1)NO2可用水吸收,相应的化学反应方程式为
 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是(2)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6kJ/mol;2NO(g)+O2(g)
2SO3(g) ΔH=-196.6kJ/mol;2NO(g)+O2(g) 2NO2(g) ΔH=-113.0kJ/mol;
2NO2(g) ΔH=-113.0kJ/mol;①则反应NO2(g)+SO2(g)
 SO3(g)+NO(g) ΔH的ΔH=
SO3(g)+NO(g) ΔH的ΔH=②一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1molSO3的同时生成1molNO2
③测得上述反应平衡时NO2与SO2的体积比为1:6,则平衡常数K=
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)
 CH3OH(g),ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。
CH3OH(g),ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。
该反应ΔH
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】目前,大规模和低成本制取氢能实质上都是通过烃重整实现的,该过程主要是甲烷水蒸气重整,包括以下两步气相化学催化反应:
反应Ⅰ: CH4(g)+H2O(g) CO(g)+3H2(g) ∆H=+206 kJ·mol-1
CO(g)+3H2(g) ∆H=+206 kJ·mol-1
反应Ⅱ: CO(g)+H2O(g) CO2(g)+H2(g) ∆H=-41 kJ·mol-1
CO2(g)+H2(g) ∆H=-41 kJ·mol-1
(1)反应:CH4(g)+2H2O(g) CO2(g)+4H2(g) ∆H=
CO2(g)+4H2(g) ∆H= ___________
(2)将2molCO和lmolH2O充入某容积不变的绝热密闭容器中,发生反应Ⅱ,下列说法正确的是___________ 。
A.断2个O-H键同时 断2个C=O键,能判断反应Ⅱ达到平衡
B.混合气体的密度保持不变,能判断反应Ⅱ达到平衡
C.混合气体的平均相对分子质量保持不变,能判断反应Ⅱ达到平衡
D.容器内温度不再变化,能判断反应Ⅱ达到平衡
E.反应Ⅱ平衡后,充入氮气,压强增大,平衡不移动
(3)甲烷水蒸气重整得到的CO2与H2,可以催化重整制备CH3OCH3,制备的过程中存在反应:
①2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ∆H<0;
CH3OCH3(g)+3H2O(g) ∆H<0;
②CO2(g)+H2(g) CO(g)+H2O(g) ∆H>0。
CO(g)+H2O(g) ∆H>0。
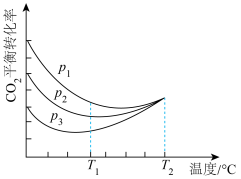
向密闭容器中以物质的量之比为1:3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示,P1、P2、 P3由大到小的顺序为___________ ;T2°C时主要发生反应___________ 。(填“①”或“②”),CO2平衡转化率随温度变化先降后升的原因为___________ 。
(4)甲烷水蒸气重整得到的CO2和H2, 也可用来制备甲醇,反应方程式CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H<0, 某温度下,将1 mol CO2和1 mol H2充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
CH3OH(g)+H2O(g) ∆H<0, 某温度下,将1 mol CO2和1 mol H2充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
①用CO2表示前2h的平均反应速率v(CO2)=___________ mol/(L·h)。
②该条件下的分压平衡常数为Kp=___________ (MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
反应Ⅰ: CH4(g)+H2O(g)
 CO(g)+3H2(g) ∆H=+206 kJ·mol-1
CO(g)+3H2(g) ∆H=+206 kJ·mol-1反应Ⅱ: CO(g)+H2O(g)
 CO2(g)+H2(g) ∆H=-41 kJ·mol-1
CO2(g)+H2(g) ∆H=-41 kJ·mol-1(1)反应:CH4(g)+2H2O(g)
 CO2(g)+4H2(g) ∆H=
CO2(g)+4H2(g) ∆H= (2)将2molCO和lmolH2O充入某容积不变的绝热密闭容器中,发生反应Ⅱ,下列说法正确的是
A.断2个O-H键同时 断2个C=O键,能判断反应Ⅱ达到平衡
B.混合气体的密度保持不变,能判断反应Ⅱ达到平衡
C.混合气体的平均相对分子质量保持不变,能判断反应Ⅱ达到平衡
D.容器内温度不再变化,能判断反应Ⅱ达到平衡
E.反应Ⅱ平衡后,充入氮气,压强增大,平衡不移动
(3)甲烷水蒸气重整得到的CO2与H2,可以催化重整制备CH3OCH3,制备的过程中存在反应:
①2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) ∆H<0;
CH3OCH3(g)+3H2O(g) ∆H<0;②CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H>0。
CO(g)+H2O(g) ∆H>0。向密闭容器中以物质的量之比为1:3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示,P1、P2、 P3由大到小的顺序为

(4)甲烷水蒸气重整得到的CO2和H2, 也可用来制备甲醇,反应方程式CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H<0, 某温度下,将1 mol CO2和1 mol H2充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
CH3OH(g)+H2O(g) ∆H<0, 某温度下,将1 mol CO2和1 mol H2充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:| 时间/h | 1 | 2 | 3 | 4 | 5 |
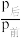 | 0.92 | 0.85 | 0.79 | 0.75 | 0.75 |
②该条件下的分压平衡常数为Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】碳及化合物在生产生活中用比较广泛。回答下列问题:
(1)已知:①H2(g)+ O2(g)=H2O(1)△H1=-285.8kJ·mol-1
O2(g)=H2O(1)△H1=-285.8kJ·mol-1
②CH3OH(1)+ O2(g)=CO2(g)+2H2O(1) △H2=-725.5kJ·mol-1
O2(g)=CO2(g)+2H2O(1) △H2=-725.5kJ·mol-1
则CO2(g)+3H2(g)=CH2OH(1)+H2O(1)的反应热 △H=____________ 。
(2)某研究小组用CO合成甲醇:CO(g)+2H2(g) CH3OH(g)△H<0,将三组混合气体分别通入到三个2L恒容密闭容器中进行反应,得到如下三组实验数据:
CH3OH(g)△H<0,将三组混合气体分别通入到三个2L恒容密闭容器中进行反应,得到如下三组实验数据:
实验1条件下平衡常数K=__________ ,a、b之间可能的关系为_____________ 。
已知反应CO(g)+2H2(g) CH3OH(g)中CO的转化率(a)与温度(T)、压强(p)的关系如右图所示:
CH3OH(g)中CO的转化率(a)与温度(T)、压强(p)的关系如右图所示:
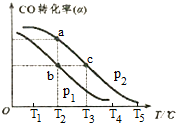
①p1______ p2(填“<”“>”“=”)。先升高温度、后增大压强,能否实现b点到c点的转化?__________ (填“能”或“不能”),原因是_____________________________________________ 。
②a、c两点的反应速率为v1________ v2(填“<”“>”“=”)。
③在不改变反应物用量情况下,为提高CO的转化率可采取的措施是_____________ (答出三条措施)。
(1)已知:①H2(g)+
 O2(g)=H2O(1)△H1=-285.8kJ·mol-1
O2(g)=H2O(1)△H1=-285.8kJ·mol-1②CH3OH(1)+
 O2(g)=CO2(g)+2H2O(1) △H2=-725.5kJ·mol-1
O2(g)=CO2(g)+2H2O(1) △H2=-725.5kJ·mol-1则CO2(g)+3H2(g)=CH2OH(1)+H2O(1)的反应热 △H=
(2)某研究小组用CO合成甲醇:CO(g)+2H2(g)
 CH3OH(g)△H<0,将三组混合气体分别通入到三个2L恒容密闭容器中进行反应,得到如下三组实验数据:
CH3OH(g)△H<0,将三组混合气体分别通入到三个2L恒容密闭容器中进行反应,得到如下三组实验数据:| 实验组 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | 达到平衡所需的时间/min | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | |||
| 1 | 650 | 2.0 | 6.0 | 0 | 1.0 | 5 | ||
| 2 | 900 | 2.0 | 6.0 | 0 | 1.2 | 2 | ||
| 3 | 650 | 1.0 | 4.0 | 2.0 | a | b | c | t |
实验1条件下平衡常数K=
已知反应CO(g)+2H2(g)
 CH3OH(g)中CO的转化率(a)与温度(T)、压强(p)的关系如右图所示:
CH3OH(g)中CO的转化率(a)与温度(T)、压强(p)的关系如右图所示:
①p1
②a、c两点的反应速率为v1
③在不改变反应物用量情况下,为提高CO的转化率可采取的措施是
您最近一年使用:0次
【推荐3】CO2的转化和利用是实现碳中和的有效途径。其中CO2转换为CH3OH被认为是最可能利用的路径,该路径涉及反应如下:
反应I: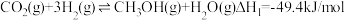
反应Ⅱ: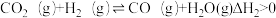
请回答下列问题:
(1)若已知H2和CO的燃烧热,计算反应Ⅱ的 H2,还需要的一个数据为
H2,还需要的一个数据为_______ 。
(2)在催化剂条件下,反应I的反应机理和相对能量变化如图(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
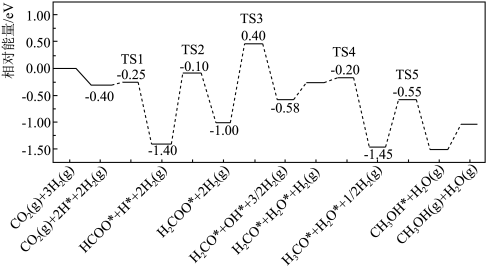
完善该反应机理中相关的化学反应方程式:
_______ ;以TS2为过渡态的反应,其正反应活化能为_______ eV。
(3)在恒温恒压下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如表。
已知:①分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;
②CH3OH的选择性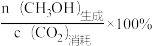
①在普通反应器(A)中,下列不能作为反应(反应I和反应Ⅱ)达到平衡状态的判据是_______ (填标号)。
A.气体的密度不再变化 B.气体的压强不再改变
C.v正(CO2)=3v逆(H2) D.各物质浓度比不再改变
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是_______ 。
③在反应器(B)中,CO2的平衡转化率明显高于反应器(A),可能的原因是_______ 。
④若反应器(A)中初始时n(CO2)=1mol,反应Ⅱ的化学平衡常数Kp(Ⅱ)=_______ (用最简的分数表示)。
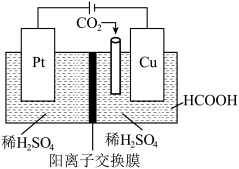
(4)近年来,有研究人员用CO2通过电催化生成HCOOH,实现CO2的回收利用,其工作原理如图所示。请写出Cu电极上的电极反应式:_______ 。
反应I:
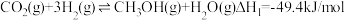
反应Ⅱ:
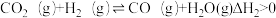
请回答下列问题:
(1)若已知H2和CO的燃烧热,计算反应Ⅱ的
 H2,还需要的一个数据为
H2,还需要的一个数据为(2)在催化剂条件下,反应I的反应机理和相对能量变化如图(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。

完善该反应机理中相关的化学反应方程式:

(3)在恒温恒压下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如表。
已知:①分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;
②CH3OH的选择性
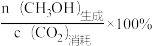
| 1.8MPa 260℃ | |||
| CO2平衡转化率 | 甲醇的选择性 | 达到平衡时间(s) | |
| 普通反应器(A) | 25.0% | 80.0% | 10.0 |
| 分子筛膜催化反应器(B) | a>25.0% | 100.0% | 8.0 |
A.气体的密度不再变化 B.气体的压强不再改变
C.v正(CO2)=3v逆(H2) D.各物质浓度比不再改变
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是
③在反应器(B)中,CO2的平衡转化率明显高于反应器(A),可能的原因是
④若反应器(A)中初始时n(CO2)=1mol,反应Ⅱ的化学平衡常数Kp(Ⅱ)=
(4)近年来,有研究人员用CO2通过电催化生成HCOOH,实现CO2的回收利用,其工作原理如图所示。请写出Cu电极上的电极反应式:

您最近一年使用:0次



