名校
1 . 某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。
【实验I】试剂:酸化的0.5mol·L-1 FeSO4溶液(pH =0.2),5%H2O2溶液(pH=5)。
(1)上述实验中H2O2溶液与FeSO4溶液反应的离子方程式是________________________ 。
(2)产生气泡的原因是______________________ 。
【实验Ⅱ】试剂:未酸化的0.5mol·L-1FeSO4溶液(pH=3),5% H2O2溶液(pH=5)
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体。取部分棕黄色沉淀洗净,加4 mol·L-1盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有Fe2O3,经检验还含有SO42-。检验棕黄色沉淀中SO42-的方法是_______________ 。
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.H2O2溶液氧化Fe2+消耗H+
ii.Fe2+氧化的产物发生了水解
①根据实验Ⅱ记录否定假设ⅰ,理由是____________________ 。
②实验验证假设ⅱ: 取__________ 溶液,加热,溶液变为红褐色,pH下降,证明假设ii成立。
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是_________________ 。
【实验Ⅲ】若用FeCl2溶液替代FeSO4溶液,其余操作与实验Ⅱ相同,除了产生与Ⅱ相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色。
(6)产生刺激性气味气体的原因是___________________ 。
(7)由实验I、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与______________ (至少写两点)有关。
【实验I】试剂:酸化的0.5mol·L-1 FeSO4溶液(pH =0.2),5%H2O2溶液(pH=5)。
| 操作 | 现象 |
| 取2mL上述FeSO4溶液于试管中,加入5滴5%H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡。测得反应后溶液pH = 0.9 |
| 向反应后的溶液中加入KSCN溶液 | 溶液变红 |
(2)产生气泡的原因是
【实验Ⅱ】试剂:未酸化的0.5mol·L-1FeSO4溶液(pH=3),5% H2O2溶液(pH=5)
| 操作 | 现象 |
| 取2mL5%H2O2溶液于试管中, 加入5滴上述FeSO4溶液, | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊。测得反应后溶液pH =1.4 |
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.H2O2溶液氧化Fe2+消耗H+
ii.Fe2+氧化的产物发生了水解
①根据实验Ⅱ记录否定假设ⅰ,理由是
②实验验证假设ⅱ: 取
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是
【实验Ⅲ】若用FeCl2溶液替代FeSO4溶液,其余操作与实验Ⅱ相同,除了产生与Ⅱ相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色。
(6)产生刺激性气味气体的原因是
(7)由实验I、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与
您最近一年使用:0次
2017-06-05更新
|
724次组卷
|
6卷引用:河北省武邑中学2018届高三上学期第三次调研考试化学试题
2 . 乙苯脱氢法是目前国内外生产苯乙烯的主要方法,研究发现,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图: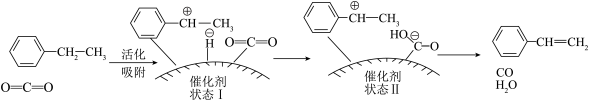
| A.乙苯和苯乙烯均为非极性分子 |
| B.催化剂表面碱性较强时有利于提高乙苯的转化率 |
C.反应涉及 、 、 断裂和 断裂和 形成 形成 |
D.该方法可减少 的排放,有利于实现“碳中和” 的排放,有利于实现“碳中和” |
您最近一年使用:0次
名校
3 . 一定条件下,一氧化二氮被镍配合物催化形成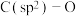 的活化机理如图所示(ii、iii、ⅳ中右上角“—”代表1个负电荷,i的右上角“0”代表不带电荷,
的活化机理如图所示(ii、iii、ⅳ中右上角“—”代表1个负电荷,i的右上角“0”代表不带电荷, 右上角“Ⅱ”代表+2价)。下列说法错误的是
右上角“Ⅱ”代表+2价)。下列说法错误的是
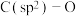 的活化机理如图所示(ii、iii、ⅳ中右上角“—”代表1个负电荷,i的右上角“0”代表不带电荷,
的活化机理如图所示(ii、iii、ⅳ中右上角“—”代表1个负电荷,i的右上角“0”代表不带电荷, 右上角“Ⅱ”代表+2价)。下列说法错误的是
右上角“Ⅱ”代表+2价)。下列说法错误的是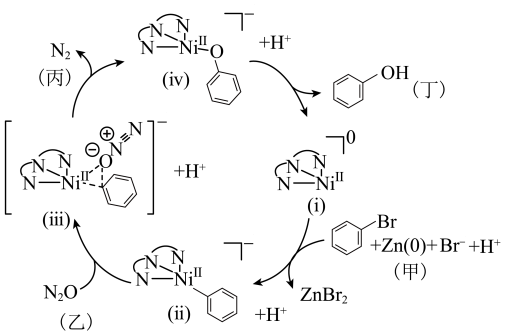
| A.ⅰ是催化剂,ⅰ、ⅱ、ⅲ是中间产物 | B.利用上述原理可实现溴苯制备苯酚 |
C. 的配合物(ⅳ)中配体只有N 的配合物(ⅳ)中配体只有N | D.ⅲ→ⅳ断裂了氮氧键和镍碳键 |
您最近一年使用:0次
名校
解题方法
4 . 铱(Ir)的配合物催化氢化 得到甲酸盐的反应机理如图所示,下列说法错误的是
得到甲酸盐的反应机理如图所示,下列说法错误的是
 得到甲酸盐的反应机理如图所示,下列说法错误的是
得到甲酸盐的反应机理如图所示,下列说法错误的是
| A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
| B.反应过程中Ir的成键数目发生了变化 |
C.转化过程总反应的化学方程式为 |
| D.反应涉及极性键和非极性键的断裂与形成 |
您最近一年使用:0次
名校
5 . 硅铝酸盐沸石离子交换分子筛M-ZSM-5(M为Fe、Co、Ni、Cu)催化N2O氧化CH4制甲醇的反应机理如图所示,下列说法错误的是
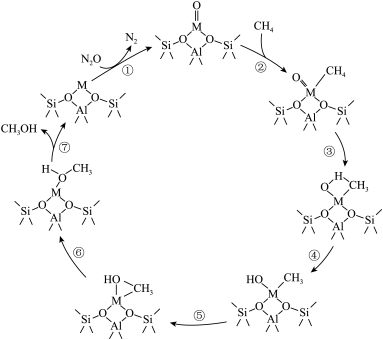
A.反应②的原子利用率为 |
B.反应①、②、③、⑥、⑦中, 的化合价发生了改变 的化合价发生了改变 |
C.M-ZSM-5能降低 氧化 氧化 制甲醇反应的活化能,改变反应的 制甲醇反应的活化能,改变反应的 |
D.总反应为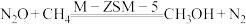 |
您最近一年使用:0次
6 . 二氧化碳和甲烷是两种温室效应气体,将二者进行转化,可得到具有高附加值的化学品或清洁燃料。
(1) 和
和 催化重整制取
催化重整制取 和
和
主反应:①
副反应:②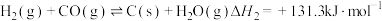
③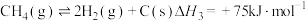
④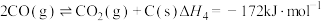
主反应的
___________ ,该反应在___________ (填“较高温度”或“较低温度”)下可自发进行。
(2) 和
和 反应可制取乙烯,反应的化学方程式为
反应可制取乙烯,反应的化学方程式为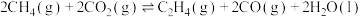 。一定温度下,向某恒容密闭容器中充入
。一定温度下,向某恒容密闭容器中充入 和
和 ,体系的初始压强为
,体系的初始压强为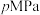 ,若平衡时
,若平衡时 的转化率为
的转化率为 ,不考虑副反应的发生,
,不考虑副反应的发生, 的平衡分压为
的平衡分压为___________ (用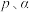 表示,下同),该反应的压强平衡常数
表示,下同),该反应的压强平衡常数
___________ 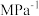 。
。
(3) 过光电化学转化
过光电化学转化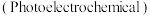 可制得乙二醇,在某催化剂作用下该反应的机理如图所示。图中
可制得乙二醇,在某催化剂作用下该反应的机理如图所示。图中 表示催化剂被光激发出电子之后产生的空穴。
表示催化剂被光激发出电子之后产生的空穴。___________ (填标号)。
A.该反应为自由基型反应
B.生成 的反应为
的反应为
C. 该反应的副产物
该反应的副产物
D.该机理中存在极性键和非极性键的断裂和形成
②以乙二醇为燃料的燃料电池工作时,乙二醇在电池___________ (填“负极”或“正极”)发生反应,若以 溶液为电解液,则该电极的反应式为
溶液为电解液,则该电极的反应式为___________ 。
(4)铜基催化剂电催化还原 制乙醇的两种途径(分别以
制乙醇的两种途径(分别以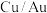 和
和 作催化剂)的相对能量变化如图所示,标“
作催化剂)的相对能量变化如图所示,标“ ”的为吸附在催化剂上的物质。分析可知,以
”的为吸附在催化剂上的物质。分析可知,以___________ 作催化剂的催化效率更高。
(1)
 和
和 催化重整制取
催化重整制取 和
和
主反应:①

副反应:②
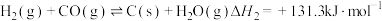
③
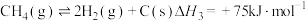
④
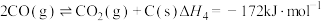
主反应的

(2)
 和
和 反应可制取乙烯,反应的化学方程式为
反应可制取乙烯,反应的化学方程式为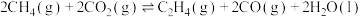 。一定温度下,向某恒容密闭容器中充入
。一定温度下,向某恒容密闭容器中充入 和
和 ,体系的初始压强为
,体系的初始压强为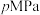 ,若平衡时
,若平衡时 的转化率为
的转化率为 ,不考虑副反应的发生,
,不考虑副反应的发生, 的平衡分压为
的平衡分压为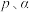 表示,下同),该反应的压强平衡常数
表示,下同),该反应的压强平衡常数
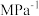 。
。(3)
 过光电化学转化
过光电化学转化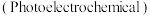 可制得乙二醇,在某催化剂作用下该反应的机理如图所示。图中
可制得乙二醇,在某催化剂作用下该反应的机理如图所示。图中 表示催化剂被光激发出电子之后产生的空穴。
表示催化剂被光激发出电子之后产生的空穴。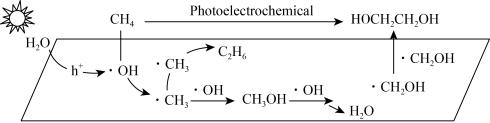
A.该反应为自由基型反应
B.生成
 的反应为
的反应为
C.
 该反应的副产物
该反应的副产物D.该机理中存在极性键和非极性键的断裂和形成
②以乙二醇为燃料的燃料电池工作时,乙二醇在电池
 溶液为电解液,则该电极的反应式为
溶液为电解液,则该电极的反应式为(4)铜基催化剂电催化还原
 制乙醇的两种途径(分别以
制乙醇的两种途径(分别以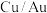 和
和 作催化剂)的相对能量变化如图所示,标“
作催化剂)的相对能量变化如图所示,标“ ”的为吸附在催化剂上的物质。分析可知,以
”的为吸附在催化剂上的物质。分析可知,以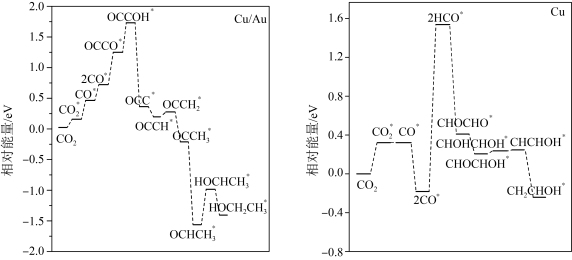
您最近一年使用:0次
7 . 烯丙醇制备丙醛的反应机理如图所示,此过程中Co的配位数不变.下列说法错误的是

A. 作催化剂 作催化剂 | B.反应过程中涉及 键的断裂与形成 键的断裂与形成 |
C.反应过程中 的化合价发生了变化 的化合价发生了变化 | D.该反应的原子利用率为 |
您最近一年使用:0次
名校
8 .  参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( ,
, 表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,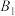 、
、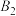 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是
 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( ,
, 表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,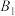 、
、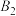 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是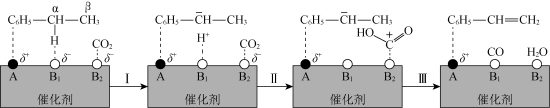
A.乙苯脱氢反应中 作氧化剂 作氧化剂 |
| B.乙苯脱氢后所得有机产物中所有原子可以共平面 |
C.步骤Ⅰ可表述为乙苯 带部分正电荷,被带部分负电荷的 带部分正电荷,被带部分负电荷的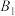 位点吸引,随后解离出 位点吸引,随后解离出 并吸附在 并吸附在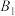 位点上 位点上 |
D.步骤Ⅱ可描述为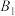 位点上的 位点上的 与 与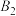 位点上 位点上 中带部分负电荷的C作用生成 中带部分负电荷的C作用生成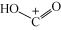 ,带部分正电荷的C吸附在带部分负电荷的 ,带部分正电荷的C吸附在带部分负电荷的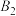 位点上 位点上 |
您最近一年使用:0次
2024-03-14更新
|
620次组卷
|
2卷引用:2024届河北省部分高三下学期一模化学试题
名校
9 . 某实验小组为探究影响H2O2分解的因素设计表中实验,下列有关说法错误的是
| 溶液 | 温度 | 时间(收集50mLO2) | |
| ① | 10mL15%H2O2溶液 | 25℃ | 160s |
| ② | 10mL30%H2O2溶液 | 25℃ | 120s |
| ③ | 10mL15%H2O2溶液 | 50℃ | 50s |
| ④ | 10mL15%H2O2溶液+1mL5%FeCl3溶液 | 50℃ | 20s |
| A.实验①和②,可探究H2O2浓度对H2O2分解速率的影响 |
| B.实验①和③,可探究温度对H2O2分解速率的影响 |
| C.实验①和④,可探究催化剂对H2O2分解速率的影响 |
| D.由上述实验可知,增大H2O2浓度、升高温度都能加快H2O2分解速率 |
您最近一年使用:0次
2023-10-04更新
|
146次组卷
|
4卷引用:河北省唐县第一中学2022-2023学年高一下学期3月月考化学试题
河北省唐县第一中学2022-2023学年高一下学期3月月考化学试题(已下线)第05讲 化学反应的速率与限度-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)江西省宜春市宜丰中学2023-2024学年高一下学期3月月考化学试题江苏省盐城市五校联考2023-2024学年高一下学期3月月考化学试题
名校
10 . 对水样中影响M分解速率的因素进行研究。在相同温度下、M的物质的量浓度c(M)随时间(t)的变化如图所示。下列说法不正确的是
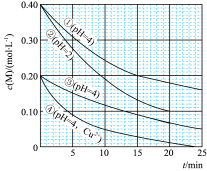

| A.水样pH越大,M的分解速率越慢 |
| B.水样中添加Cu2+,能加快M的分解速率 |
| C.由①,③得,反应物浓度越大,M的分解速率越快 |
| D.在0~20min内,②中M的分解速率为0.15mol·L-1·min-1 |
您最近一年使用:0次



