1 . 下列实验能达到目的的是
| 实验目的 | 实验方法或操作 | |
| A | 测定中和反应的反应热 | 用保温杯替代烧杯更有利于减少热量散失,同时可以用温度传感器采集反应溶液的温度,实现化学实验数字化、形象化 |
| B | 探究浓度对化学反应速率的影响 | 量取同体积不同浓度的NaClO溶液,分别加入等体积等浓度的 溶液,对比现象 溶液,对比现象 |
| C | 探究催化剂对反应速率的影响 | 将等体积等浓度的氯化铁和硫酸铜溶液分别加入到体积相同的2%和10%的 溶液中,对比产生气泡的快慢 溶液中,对比产生气泡的快慢 |
| D | 检验 的存在 的存在 | 向待测液中先加入氯化钡溶液,再加入稀盐酸,观察是否有白色沉淀产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。
Ⅰ. 某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照下表所示的方案完成实验。
(1)实验①和②的目的是___ 。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是__________ (写出一种即可)。
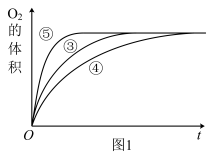
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图1所示。分析该图能够得出的实验结论是____ 。
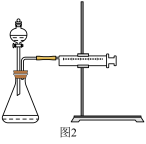
Ⅱ. MnO2对H2O2的分解有催化作用,某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将状态不同的0.1 g MnO2分别加入盛有50 mL等浓度的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出大试管中发生反应的化学方程式:__ ,该反应是____ 反应(填“放热”或“吸热”)。
(2)实验结果表明,催化剂的催化效果与____ 有关。
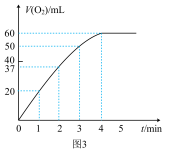
(3)实验过程中放出气体的体积(标准状况)和时间的关系如图3所示。解释反应速率变化的原因:__ ,计算H2O2的初始物质的量浓度为____ 。(保留两位有效数字)
Ⅰ. 某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照下表所示的方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液+1 mL H2O | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+1 mL HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+1 mL NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图1所示。分析该图能够得出的实验结论是



Ⅱ. MnO2对H2O2的分解有催化作用,某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将状态不同的0.1 g MnO2分别加入盛有50 mL等浓度的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
| MnO2状态 | 触摸试管情况 | 观察结果 | 反应完成所需时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 4 min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(2)实验结果表明,催化剂的催化效果与
(3)实验过程中放出气体的体积(标准状况)和时间的关系如图3所示。解释反应速率变化的原因:
您最近一年使用:0次
2019-06-12更新
|
255次组卷
|
3卷引用:四川省内江市威远中学2020-2021学年高一下学期期中考试化学试题
名校
3 . 下列有关实验能够达到相应实验目的的是
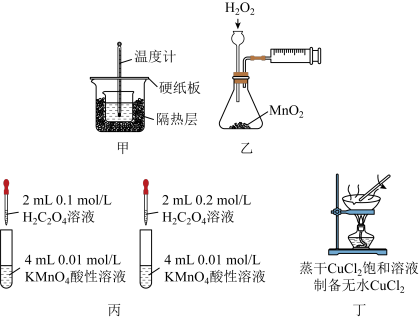

| A.图甲中补充环形玻璃搅拌棒即可用于中和热的测定 |
| B.图乙可用于测定H2O2溶液的分解速率 |
| C.图丙的实验设计可以探究浓度对化学反应速率的影响 |
| D.图丁可蒸干CuCl2饱和溶液制备无水CuCl2 |
您最近一年使用:0次
2023-04-08更新
|
402次组卷
|
4卷引用:四川省内江市威远中学校2022-2023学年高二下学期期中考试化学试题



