解题方法
1 . 下列实验装置能达到相应实验目的的是
选项 | A | B | C | D |
实验装置 |
|
|
|
|
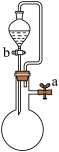
实验目的 | 验证牺牲阳极法保护铁 | 制备并收集氨气 | 验证 | 关闭a、打开b,可检查装置的气密性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
2 . 下列所示装置或操作能达到实验目的的是
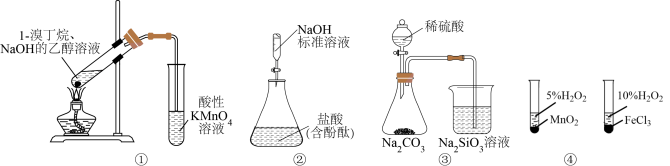

| A.图①:验证1-溴丁烷发生消去反应 |
B.图②: 标准溶液滴定盐酸 标准溶液滴定盐酸 |
| C.图③:比较硫、碳、硅三种元素的非金属性强弱 |
| D.图④:比较不同催化剂对反应速率的影响 |
您最近半年使用:0次
名校
3 . 用下列实验装置进行相应实验,能达到实验目的的是


| A.用装置甲定量测定化学反应速率 |
B.用装置乙实现反应: |
| C.用装置丙准确测定中和反应的反应热 |
D.用装置丁验证 对 对 分解反应有催化作用 分解反应有催化作用 |
您最近半年使用:0次
2023-12-02更新
|
845次组卷
|
9卷引用:天津市和平区天津市耀华中学2023-2024学年高三上学期第三次月考化学试卷
名校
解题方法
4 . 用下列实验装置进行相应实验,能达到实验目的的是
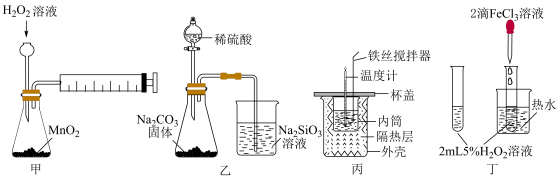

| A.用装置甲定量测定化学反应速率 |
| B.证明非金属性:S>C>Si |
| C.用装置丙准确测定中和反应的反应热 |
D.用装置丁验证 对 对 分解反应有催化作用 分解反应有催化作用 |
您最近半年使用:0次
名校
5 . 实现 的有效转化成为科研工作者的研究热点。
的有效转化成为科研工作者的研究热点。
I.以 作催化剂,可使
作催化剂,可使 在温和条件下转化为甲醇,反应经历如下:
在温和条件下转化为甲醇,反应经历如下:
i.催化剂活化: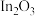 (无活性)
(无活性)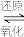
 (有活性)
(有活性)
ii. 与
与 在活化的催化剂表面发生反应
在活化的催化剂表面发生反应
①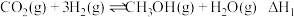
②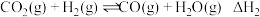 (副反应)
(副反应)
(1)写出 电子式
电子式___________ 。
(2)在恒温密闭容器中, 和
和 按物质的量之比1∶1开始反应,当以下数值不变时,能说明反应②达到平衡状态的是
按物质的量之比1∶1开始反应,当以下数值不变时,能说明反应②达到平衡状态的是___________ (填序号)。
a.混合气体的密度 b.混合气体的平均相对分子质量
c. 的体积分数 d.
的体积分数 d. 和
和 的体积比
的体积比
(3)某温度下, 与
与 的混合气体以不同流速通过恒容反应器,随气体流速的增大,
的混合气体以不同流速通过恒容反应器,随气体流速的增大, 转化率变小,而
转化率变小,而 的选择性增大
的选择性增大
已知: 选择性
选择性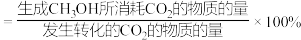
 的选择性随气体流速增大而升高的原因可能有:
的选择性随气体流速增大而升高的原因可能有:
①___________ 。
②气体流速增大可减少产物中 的积累,减少催化剂的失活,从而提高
的积累,减少催化剂的失活,从而提高 选择性。请用化学方程式表示催化剂失活的原因:
选择性。请用化学方程式表示催化剂失活的原因:___________ 。
Ⅱ.以二氧化碳为原料,电化学法制备甲酸(甲酸盐)工作原理如图所示。___________ 极,阴极表面发生的电极反应式___________ 。
(5)若有 通过质子交换膜时,该装置内生成
通过质子交换膜时,该装置内生成 和
和 的物质的量共计
的物质的量共计_______  。
。
 的有效转化成为科研工作者的研究热点。
的有效转化成为科研工作者的研究热点。I.以
 作催化剂,可使
作催化剂,可使 在温和条件下转化为甲醇,反应经历如下:
在温和条件下转化为甲醇,反应经历如下:i.催化剂活化:
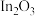 (无活性)
(无活性)
 (有活性)
(有活性)ii.
 与
与 在活化的催化剂表面发生反应
在活化的催化剂表面发生反应①
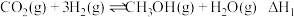
②
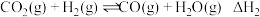 (副反应)
(副反应)(1)写出
 电子式
电子式(2)在恒温密闭容器中,
 和
和 按物质的量之比1∶1开始反应,当以下数值不变时,能说明反应②达到平衡状态的是
按物质的量之比1∶1开始反应,当以下数值不变时,能说明反应②达到平衡状态的是a.混合气体的密度 b.混合气体的平均相对分子质量
c.
 的体积分数 d.
的体积分数 d. 和
和 的体积比
的体积比(3)某温度下,
 与
与 的混合气体以不同流速通过恒容反应器,随气体流速的增大,
的混合气体以不同流速通过恒容反应器,随气体流速的增大, 转化率变小,而
转化率变小,而 的选择性增大
的选择性增大已知:
 选择性
选择性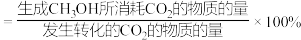
 的选择性随气体流速增大而升高的原因可能有:
的选择性随气体流速增大而升高的原因可能有:①
②气体流速增大可减少产物中
 的积累,减少催化剂的失活,从而提高
的积累,减少催化剂的失活,从而提高 选择性。请用化学方程式表示催化剂失活的原因:
选择性。请用化学方程式表示催化剂失活的原因:Ⅱ.以二氧化碳为原料,电化学法制备甲酸(甲酸盐)工作原理如图所示。
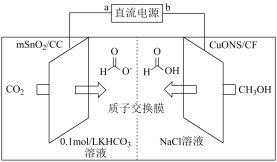
(5)若有
 通过质子交换膜时,该装置内生成
通过质子交换膜时,该装置内生成 和
和 的物质的量共计
的物质的量共计 。
。
您最近半年使用:0次
2023-04-26更新
|
243次组卷
|
2卷引用:天津市部分区学校2023届高三下学期质量调查(二)化学试题
6 . 亚硝酰硫酸(NOSO4H)是一种浅黄色液体,遇水易分解,溶于浓硫酸,主要用于染料、医药领域的重氮化反应。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品中杂质硝酸的含量。
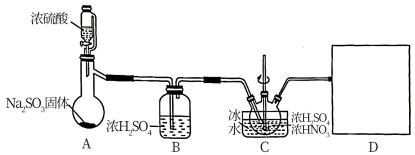
回答下列问题:
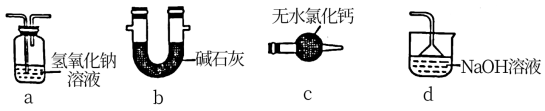
(1)装置A中盛装Na2SO3固体的仪器名称是_______ ,装置D最好选用_______ (填序号)。
(2)装置C中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①装置C中温度过高产率降低的原因是_______ 。
②开始通SO2时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是_______ 。
(3)测定亚硝酰硫酸产品中杂质硝酸的含量。
称取1.400g产品放入250mL锥形瓶中,加80mL浓硫酸,用
 标准溶液滴定,消耗标准溶液20.00mL。
标准溶液滴定,消耗标准溶液20.00mL。
已知: 可与NO生成粉红色的FeSO4·NO。
可与NO生成粉红色的FeSO4·NO。
①锥形瓶中加入浓硫酸的作用是_______ 。
②判断滴定达到终点的现象是_______ 。
③亚硝酰硫酸中硝酸的含量为_______ 。

回答下列问题:
(1)装置A中盛装Na2SO3固体的仪器名称是

(2)装置C中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①装置C中温度过高产率降低的原因是
②开始通SO2时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是
(3)测定亚硝酰硫酸产品中杂质硝酸的含量。
称取1.400g产品放入250mL锥形瓶中,加80mL浓硫酸,用

 标准溶液滴定,消耗标准溶液20.00mL。
标准溶液滴定,消耗标准溶液20.00mL。已知:
 可与NO生成粉红色的FeSO4·NO。
可与NO生成粉红色的FeSO4·NO。①锥形瓶中加入浓硫酸的作用是
②判断滴定达到终点的现象是
③亚硝酰硫酸中硝酸的含量为
您最近半年使用:0次
2021-05-28更新
|
618次组卷
|
3卷引用:2021年天津高考化学试题变式题13-16

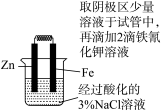

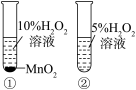
 是
是 分解的催化剂
分解的催化剂

