名校
解题方法
1 . 已知反应2NO + 2H2 = N2 + 2H2O的速率方程为υ= kc2(NO)· c(H2)(k为速率常数),其反应历程如下:
① 2NO + H2 → N2+H2O2 慢 ; ② H2O2 + H2 → 2H2O 快
下列说法不正确 的是
① 2NO + H2 → N2+H2O2 慢 ; ② H2O2 + H2 → 2H2O 快
下列说法
| A.升高温度,可提高反应①、②的反应速率 |
| B.c (NO) 、c(H2)增大相同的倍数,对总反应的反应速率的影响程度相同 |
| C.该反应的快慢主要取决于反应① |
| D.可逆反应使用催化剂加快反应速率时,正逆反应的活化能均减小 |
您最近一年使用:0次
名校
2 . 科研人员提出以 为原料,在特定催化剂作用下合成
为原料,在特定催化剂作用下合成 的一种反应历程如图,下列说法错误的是
的一种反应历程如图,下列说法错误的是
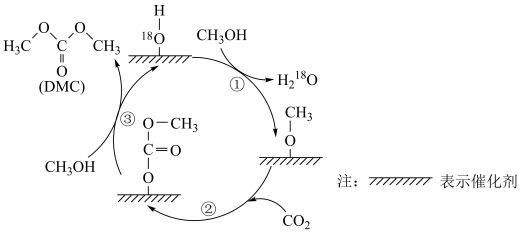
 为原料,在特定催化剂作用下合成
为原料,在特定催化剂作用下合成 的一种反应历程如图,下列说法错误的是
的一种反应历程如图,下列说法错误的是
A. 分子中均不含非极性键 分子中均不含非极性键 |
| B.反应①中有碳氧单键的断裂和形成 |
| C.生成DMC总反应的原子利用率小于100% |
| D.催化剂可提高单位时间内甲醇的转化率 |
您最近一年使用:0次
名校
3 . 目前,汽车尾气系统中均安装了催化转化器,这种方法是处理 的“储存还原技术法”,简称NSR,NO在催化剂表面物质转化的关系如图所示,下列说法中错误的是
的“储存还原技术法”,简称NSR,NO在催化剂表面物质转化的关系如图所示,下列说法中错误的是
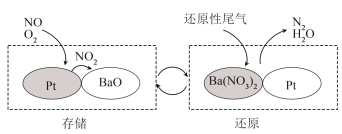
 的“储存还原技术法”,简称NSR,NO在催化剂表面物质转化的关系如图所示,下列说法中错误的是
的“储存还原技术法”,简称NSR,NO在催化剂表面物质转化的关系如图所示,下列说法中错误的是
A. 和 和 都是该反应过程的催化剂 都是该反应过程的催化剂 |
B.还原性尾气可以为 、 、 等 等 |
| C.催化剂的作用是改变了反应的历程,提高化学反应速率 |
D.如果汽车所用汽油含硫量较高, 吸收 吸收 的能力会显著下降 的能力会显著下降 |
您最近一年使用:0次
名校
解题方法
4 . 多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如下:

下列说法正确的是

下列说法正确的是
| A.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g) ΔH=+akJ/mol(a>0) |
| B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量 |
| C.选择优良的催化剂降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗 |
| D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂 |
您最近一年使用:0次
2024-01-21更新
|
146次组卷
|
5卷引用:湖北省武汉市第四中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
5 . 通过理论计算发现,CH2=CH-C≡CH与HBr发生加成反应时,通过不同的路径都可以生成有机物④,其反应过程及相对能量变化如下图所示。下列说法错误的是
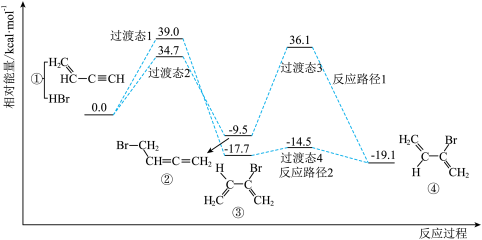

| A.反应物经过渡态2生成中间体发生的是加成反应 |
| B.推测物质的稳定性顺序为:④>③>② |
| C.反应路径1中决速步的活化能为39.0kcal/mol |
D.催化剂不会改变总反应的 |
您最近一年使用:0次
名校
解题方法
6 . 某实验小组用如下实验测定海带预处理后所得溶液的碘含量,实验步骤及现象如下:
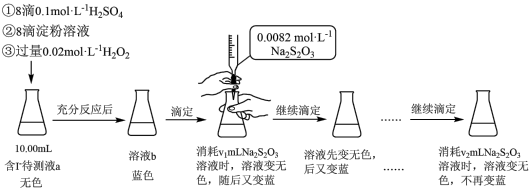
已知: ,下列说法不正确的是:
,下列说法不正确的是:

已知:
 ,下列说法不正确的是:
,下列说法不正确的是:| A.淀粉溶液为该反应的指示剂 |
B.溶液b为蓝色是因为发生了反应: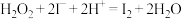 |
C.溶液反复由无色变蓝的原因可能是H2O2氧化 的反应速率比 的反应速率比 还原 还原 的反应速率快 的反应速率快 |
| D.上述实验不能准确测定待测液中的碘含量,应补充实验步骤:滴定前向溶液b中加少量MnO2,反应至不再产生气泡,过滤,对滤液进行滴定 |
您最近一年使用:0次
名校
7 . 在某一恒容容器中发生反应:
 。当反应达到平衡时,
。当反应达到平衡时, 、
、 、
、 、
、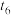 改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是
改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是

 。当反应达到平衡时,
。当反应达到平衡时, 、
、 、
、 、
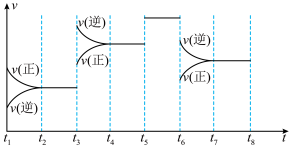
、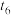 改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是
改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是
A. 时刻,改变的条件可能是适当降低温度 时刻,改变的条件可能是适当降低温度 |
B. 时可能增大了反应物活化分子百分数 时可能增大了反应物活化分子百分数 |
C. 时刻,改变的条件一定是催化剂 时刻,改变的条件一定是催化剂 |
D.Q(g)的体积分数最高的时间段是 |
您最近一年使用:0次
名校
解题方法
8 . 通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一,下列实验操作、现象和解释或者结论不正确的有
| 实验操作 | 现象 | 解释或者结论 | |
| A | 分别在20℃、30℃下,取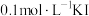 液,向其中先加入淀粉溶液,再加入 液,向其中先加入淀粉溶液,再加入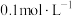 的硫酸( 的硫酸( ) ) | 30℃下,溶液更快出现蓝色 | 温度越高,化学反应速率越快 |
| B | 用 计测定 计测定 溶液和 溶液和 溶液的 溶液的 |  溶液的 溶液的 较大 较大 |  酸性弱于 酸性弱于 |
| C | 向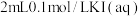 中加入 中加入 ,充分反应,用四氯化碳充分萃取后取上层溶液滴加 ,充分反应,用四氯化碳充分萃取后取上层溶液滴加 | 四氯化碳层显紫色,上层溶液试样变红 |  和 和 的反应存在限度 的反应存在限度 |
| D | 向盛有 溶液的试管中加入酸化后的 溶液的试管中加入酸化后的 溶液 溶液 | 溶液变为棕黄色且出现无色气泡 | 生成了 ,同时 ,同时 催化分解 催化分解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 合成氨工艺是氮肥工业的基础,影响了人类的生存和发展。
(1)甲烷水蒸气重整是传统的主要的制氢方法,发生的反应为
 。已知:甲烷和氢气的燃烧热分别是893 kJ∙mol-1和286 kJ∙mol-1,
。已知:甲烷和氢气的燃烧热分别是893 kJ∙mol-1和286 kJ∙mol-1,
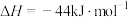 。回答下列问题:
。回答下列问题:
①△H1=___________ 。
②容器中通入物质的量之比为1∶2的甲烷和水蒸气,在一定条件下发生上述反应,平衡时H2的体积分数为φ,CH4的体积分数=___________ 。
(2)N2、H2在Fe催化剂作用下的反应历程为(*表示吸附态)
化学吸附:(ⅰ)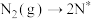 ;(ⅱ)
;(ⅱ)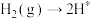 ;
;
表面反应:(ⅲ)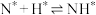 ;(ⅳ)
;(ⅳ)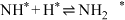 ;(ⅴ)
;(ⅴ)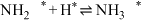
脱附:(ⅵ)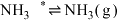
回答下列问题:
①反应(ⅰ)决定了合成氨的整体反应速率。在上述历程中,(ⅰ)的反应速率最_____ (填“大”、“小”),原因是:_____ 。
②反应过程中,如果仅增多Fe催化剂的量(不改变比表面积),下列选项有变化的是_____ 。
A.反应热 B.化学平衡常数
C.单位时间内NH3的产量 D.活化能
(3)一定温度下发生合成氨反应时,反应物分子百分数和分子能量的关系如图,其中E表示分子的平均能量,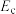 是活化分子具有的最低能量。
是活化分子具有的最低能量。
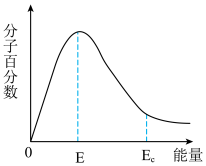
回答下列问题:
①活化能=_____ (用含Ec、E的式子表示)。
②在上图中作出升高温度时,E~EC间分子百分数和能量的关系曲线______________ 。
(1)甲烷水蒸气重整是传统的主要的制氢方法,发生的反应为

 。已知:甲烷和氢气的燃烧热分别是893 kJ∙mol-1和286 kJ∙mol-1,
。已知:甲烷和氢气的燃烧热分别是893 kJ∙mol-1和286 kJ∙mol-1,
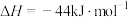 。回答下列问题:
。回答下列问题:①△H1=
②容器中通入物质的量之比为1∶2的甲烷和水蒸气,在一定条件下发生上述反应,平衡时H2的体积分数为φ,CH4的体积分数=
(2)N2、H2在Fe催化剂作用下的反应历程为(*表示吸附态)
化学吸附:(ⅰ)
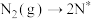 ;(ⅱ)
;(ⅱ)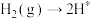 ;
;表面反应:(ⅲ)
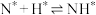 ;(ⅳ)
;(ⅳ) ;(ⅴ)
;(ⅴ)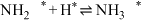
脱附:(ⅵ)
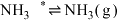
回答下列问题:
①反应(ⅰ)决定了合成氨的整体反应速率。在上述历程中,(ⅰ)的反应速率最
②反应过程中,如果仅增多Fe催化剂的量(不改变比表面积),下列选项有变化的是
A.反应热 B.化学平衡常数
C.单位时间内NH3的产量 D.活化能
(3)一定温度下发生合成氨反应时,反应物分子百分数和分子能量的关系如图,其中E表示分子的平均能量,
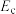 是活化分子具有的最低能量。
是活化分子具有的最低能量。
回答下列问题:
①活化能=
②在上图中作出升高温度时,E~EC间分子百分数和能量的关系曲线
您最近一年使用:0次
名校
解题方法
10 . 下列生产或实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 室温下,分别向2支试管中加入相同体积、相同浓度的 溶液,再分别加入相同体积不同浓度的稀硫酸,比较析出沉淀所需时间 溶液,再分别加入相同体积不同浓度的稀硫酸,比较析出沉淀所需时间 | 当其他条件不变时,反应物浓度增大,化学反应速率加快 |
| B | 向含有少量I2的淀粉溶液中加入NaOH溶液并加热,蓝色褪去 | NaOH是淀粉水解的催化剂 |
| C | 往黄色固体难溶物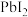 中加水,振荡,静置。取上层清液,然后加入NaI固体,产生黄色沉淀 中加水,振荡,静置。取上层清液,然后加入NaI固体,产生黄色沉淀 | 难溶物存在沉淀溶解平衡 |
| D | A、B两支试管中分别加入等体积5%的 溶液,在B中加入2~3滴 溶液,在B中加入2~3滴 溶液,B试管中产生气泡快 溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-28更新
|
160次组卷
|
3卷引用:湖北省鄂东南省级师范高中教育教学改革联盟学校2023-2024学年高二上学期期中联考化学试题
湖北省鄂东南省级师范高中教育教学改革联盟学校2023-2024学年高二上学期期中联考化学试题湖北省武昌实验中学2023-2024学年高二上学期12月月考化学试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)



