名校
解题方法
1 . 氮的化合物在生产、生活中有着重要作用。如何增加氨的产量,减少机动车尾气中NOx和CO的排放是科学家一直关注研究的课题。
(1)工业合成氨:N2(g)+3H2(g) 2NH3(g) △H=akJ·mol-1的反应历程和能量变化如图所示,标注“*”表示在催化剂表面吸附的物质。
2NH3(g) △H=akJ·mol-1的反应历程和能量变化如图所示,标注“*”表示在催化剂表面吸附的物质。
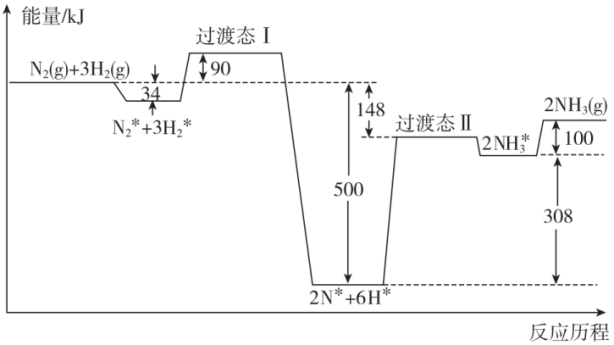
①a=_______ ;用化学方程式表示出对总反应速率影响较大的步骤_______ 。
②控制压强为P0 MPa、温度在700K,将N2(g)和H2(g)按照体积比1:3充入密闭容器合成NH3(g)。反应达到平衡状态时体系中NH3的体积分数为60%,则化学平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,气体分压=气体总压×气体体积分数)。
(2)汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除CO、NO等污染物。反应机理如下[Pt(s)表示催化剂,右上角带“*”表示吸附状态]:
I.NO+Pt(s)=NO* II.CO+Pt(s)=CO* III.NO*=N*+O*
IV.CO*+O*=CO2+Pt(s) V.N*+ N*=N2+Pt(s) VI.NO*+N*=N2O+Pt(s)
经测定汽车尾气中反应物浓度及生成物浓度随温度T变化关系如图1和图2所示。
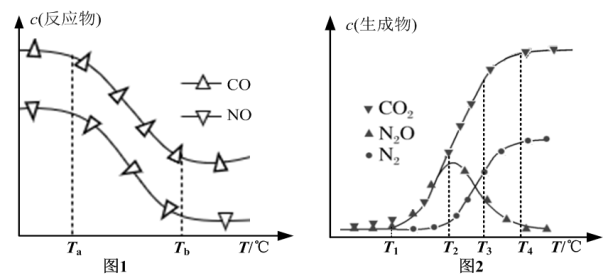
①图1中温度从Ta升至Tb的过程中,反应物浓度急剧减小的主要原因是_______ 。
②图2中温度T2℃时反应V的活化能_______ 反应VI的活化能(填“<”、“>”或“=”);温度T3℃时发生的主要反应为_______ (填“IV”、“V”或“VI”)。
③模拟汽车的“催化转化器”,将2 mol NO(g)和2mol CO(g)充入1L的密闭容器中,发生反应2NO(g)+2CO(g) N2(g)+2CO2(g),测得CO的平衡转化率α随温度T变化曲线如图所示。
N2(g)+2CO2(g),测得CO的平衡转化率α随温度T变化曲线如图所示。
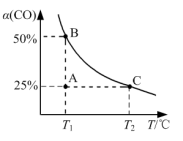
图象中A点逆反应速率_______ C点正反应速率(填“>”“=”或“<”);实验测得:v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2),k正、k逆分别是正、逆反应速率常数。则T1℃时A点处对应的v正:v逆=_______ 。
(1)工业合成氨:N2(g)+3H2(g)
 2NH3(g) △H=akJ·mol-1的反应历程和能量变化如图所示,标注“*”表示在催化剂表面吸附的物质。
2NH3(g) △H=akJ·mol-1的反应历程和能量变化如图所示,标注“*”表示在催化剂表面吸附的物质。
①a=
②控制压强为P0 MPa、温度在700K,将N2(g)和H2(g)按照体积比1:3充入密闭容器合成NH3(g)。反应达到平衡状态时体系中NH3的体积分数为60%,则化学平衡常数Kp=
(2)汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除CO、NO等污染物。反应机理如下[Pt(s)表示催化剂,右上角带“*”表示吸附状态]:
I.NO+Pt(s)=NO* II.CO+Pt(s)=CO* III.NO*=N*+O*
IV.CO*+O*=CO2+Pt(s) V.N*+ N*=N2+Pt(s) VI.NO*+N*=N2O+Pt(s)
经测定汽车尾气中反应物浓度及生成物浓度随温度T变化关系如图1和图2所示。

①图1中温度从Ta升至Tb的过程中,反应物浓度急剧减小的主要原因是
②图2中温度T2℃时反应V的活化能
③模拟汽车的“催化转化器”,将2 mol NO(g)和2mol CO(g)充入1L的密闭容器中,发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g),测得CO的平衡转化率α随温度T变化曲线如图所示。
N2(g)+2CO2(g),测得CO的平衡转化率α随温度T变化曲线如图所示。
图象中A点逆反应速率
您最近一年使用:0次
2021-04-04更新
|
782次组卷
|
5卷引用:辽宁省沈阳市第二中学2023-2024学年高二上学期10月阶段考试化学试题
辽宁省沈阳市第二中学2023-2024学年高二上学期10月阶段考试化学试题山东省济南大学城实验高中2021-2022学年高三2月阶段性调研化学试题山东省烟台市2021届高考一模(诊断性测试)化学试题(已下线)难点5 化学反应速率与化学平衡图表分析-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)专题15 化学反应原理综合-备战2022年高考化学真题及地市好题专项集训【山东专用】
名校
2 . Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下:
①Cl2(g)⇌2Cl•(g) 快
②CO(g)+Cl•(g)⇌COCl•(g) 快
③COCl•(g)+Cl2(g)⇌COCl2(g)+Cl•(g) 慢
反应②的速率方程为v正=k正c(CO)×c(Cl•),v逆=k逆c(COCl•)。下列说法错误的是
①Cl2(g)⇌2Cl•(g) 快
②CO(g)+Cl•(g)⇌COCl•(g) 快
③COCl•(g)+Cl2(g)⇌COCl2(g)+Cl•(g) 慢
反应②的速率方程为v正=k正c(CO)×c(Cl•),v逆=k逆c(COCl•)。下列说法错误的是
| A.反应①的活化能大于反应③的活化能 |
B.反应②的平衡常数K= |
| C.要提高合成COCl2的速率,关键是提高反应③的速率 |
| D.选择合适的催化剂能提高单位时间内COCl2的产率 |
您最近一年使用:0次
2021-01-28更新
|
614次组卷
|
8卷引用:辽宁省东北育才学校高中部2023-2024学年高二上学期第一次月考化学试题
解题方法
3 . 能量与化学反应关系密切,下列说法正确的是
| A.放热反应的速率一定比吸热反应快 | B.合适的催化剂能将放热反应转化为吸热反应 |
| C.化学反应一定伴随着能量的变化 | D.吸热反应的逆反应也可能为吸热反应 |
您最近一年使用:0次
2020-12-26更新
|
211次组卷
|
2卷引用:辽宁省朝阳育英高考补习学校2021-2022学年高二10月月考化学试题
20-21高三上·江西南昌·期中
名校
解题方法
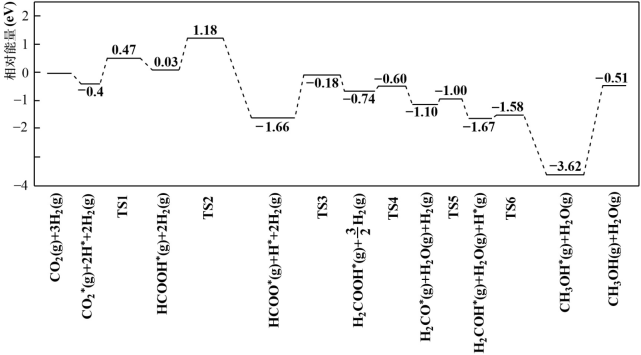
4 . 反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究发现,一定条件下,Pt单原子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态。下列说法正确的是( )
CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究发现,一定条件下,Pt单原子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态。下列说法正确的是( )
 CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究发现,一定条件下,Pt单原子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态。下列说法正确的是( )
CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究发现,一定条件下,Pt单原子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态。下列说法正确的是( )
| A.经历TS1,CO2共价键发生断裂,且生成羧基 |
| B.Pt为固体催化剂,其表面积对催化效果无影响 |
C.能垒(活化能)为1.48eV的反应为HCOOH*(g)+2H2(g)=H2COOH*(g)+ H2 H2 |
| D.如果换用铜系催化剂,所得反应历程与图示相同 |
您最近一年使用:0次
2020-12-08更新
|
190次组卷
|
3卷引用:辽宁省沈阳市第十五中学2023-2024学年高二上学期12月月考化学试题
辽宁省沈阳市第十五中学2023-2024学年高二上学期12月月考化学试题甘肃省庆阳市等3地2022-2023学年高二上学期12月期中化学试题(已下线)【南昌新东方】9.2020年11月江西南昌三中高三上学期期中化学
10-11高二下·浙江台州·期末
名校
解题方法
5 . 下列说法不正确的是
| A.增大压强,活化分子百分数不变,化学反应速率增大 |
| B.升高温度,活化分子百分数增大,化学反应速率增大 |
| C.加入反应物,活化分子百分数增大,化学反应速率增大 |
| D.使用催化剂,活化分子百分数增大,化学反应速率增大 |
您最近一年使用:0次
2020-11-25更新
|
195次组卷
|
32卷引用:辽宁省大连市瓦房店市实验高级中学2020-2021学年高二上学期10月月考化学试题
辽宁省大连市瓦房店市实验高级中学2020-2021学年高二上学期10月月考化学试题2014-2015学年内蒙古巴市一中高二10月月考化学试卷2015-2016学年河北大名县第一中学高二上学期第一次月考试化学试卷2016-2017学年河北省卓越联盟高二上第一次月考化学试卷河北省涞水波峰中学2017-2018学年高二(实验班)上学期9月月考化学试题【全国百强校】浙江省台州中学2018-2019学年高二上学期第二次统练化学试题浙江省杭州市西湖高级中学2018-2019学年高二4月月考化学试题江苏省常州礼嘉中学2018-2019学年高二6月月考化学试题(已下线)【新东方】高中化学5016甘肃省临夏中学2019-2020学年高二上学期第一次月考化学试题河北省邢台市2020-2021学年高二上学期第一次9月联考化学试题黑龙江省绥化市青冈县第一中学2020-2021学年高二上学期10月月考(筑梦班)化学试题黑龙江省青冈县第一中学2020-2021学年高二上学期月考(腾飞班)化学试题广东省湛江市雷州市第二中学2020-2021学年高二上学期第一次月考化学试题广西贺州市中学2020-2021学年高二上学期第三次月考化学试题河南省新蔡县第一高级中学2021-2022学年高二10月月考化学试题(已下线)2010~2011学年浙江省台州市高二下学期期末测试化学(已下线)2010—2011学年山东省邹城市第一中学高二下学期期末考试化学试卷2015-2016学年浙江省台州中学高二上期中测试化学试卷2015-2016学年浙江省桐乡市高级中学高二上期中(普通班)化学试卷2015-2016学年福建省长泰县第一中学高二上学期期末化学试卷2016-2017学年浙江省慈溪市高二上学期期中化学试卷2016-2017学年安徽省马鞍山二中高二下学期期中(理科)考试化学试卷天津市红桥区2017-2018学年高二上学期期中考试化学试题高二人教版选修4 第二章 章末基础排查(二)(已下线)2019年9月8日《每日一题》 选修4 每周一测(已下线)【新东方】 2020-3河北省尚义县第一中学2020-2021学年高二上学期期中考试化学试题四川省南充市白塔中学2020-2021学年高一下学期第二次月考(6月)化学试题广东省深圳市福田区外国语高级中学2021-2022学年高二上学期期中考试化学试题浙江省诸暨市第二高级中学2021-2022学年高二上学期期中考试化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末模拟考试化学试题
解题方法
6 . 某温度下,在2L容器中有3种气体物质进行反应,X、Y、Z三种物质的量随时间的变化曲线如图所示。
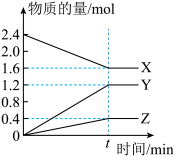
(1)该反应的化学方程式是___________________ 。
(2)若t=10 min,则Y的平均反应速率是__________ ,想要提高反应速率,可适当采取的措施是________ ,________ ,_______ 。(填三个)

(1)该反应的化学方程式是
(2)若t=10 min,则Y的平均反应速率是
您最近一年使用:0次
名校
解题方法
7 . 三元催化器是重要的汽车尾气净化装置,其工作原理如图所示,下列说法错误的是


| A.催化剂能降低反应的活化能 |
| B.汽车尾气中的CO主要来源于燃油的不完全燃烧 |
| C.汽车尾气中的氮氧化物主要来自空气中氮气和氧气反应的生成物 |
| D.催化器中,NOx、CO、碳氢化合物均作还原剂 |
您最近一年使用:0次
2020-10-31更新
|
140次组卷
|
2卷引用:辽宁省协作校2020-2021学年高二上学期第一次联考化学试题
2019高二上·全国·专题练习
名校
解题方法
8 . 已知反应: 2NO(g)+Br2(g) 2NOBr(g) ΔH=-a kJ·mol-1(a>0),其反应机理如下
2NOBr(g) ΔH=-a kJ·mol-1(a>0),其反应机理如下
①NO(g)+Br2(g) NOBr2(g)快
NOBr2(g)快
②NO(g)+NOBr2(g) 2NOBr(g)慢
2NOBr(g)慢
下列有关该反应的说法正确的是( )
 2NOBr(g) ΔH=-a kJ·mol-1(a>0),其反应机理如下
2NOBr(g) ΔH=-a kJ·mol-1(a>0),其反应机理如下①NO(g)+Br2(g)
 NOBr2(g)快
NOBr2(g)快②NO(g)+NOBr2(g)
 2NOBr(g)慢
2NOBr(g)慢下列有关该反应的说法正确的是( )
| A.该反应的速率主要取决于①的快慢 |
| B.NOBr2是该反应的催化剂 |
| C.正反应的活化能比逆反应的活化能小a kJ·mol-1 |
| D.增大 Br2(g)浓度能增大活化分子百分数, 加快反应速率 |
您最近一年使用:0次
2020-10-31更新
|
1758次组卷
|
41卷引用:辽宁省大连市一〇三中学2020-2021学年高二10月月考化学试题
辽宁省大连市一〇三中学2020-2021学年高二10月月考化学试题辽宁省葫芦岛市第八高级中学2020届高三10月月考化学试题福建省永安市第三中学2019-2020学年高二下学期期初综合检测试化学试题安徽省池州市第一中学2020-2021学年高二上学期9月月考化学试题湖北省黄石市育英高中2020-2021学年高二上学期第一次月考化学试题黑龙江省八校2020-2021学年高二上学期摸底考试化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研化学试题辽宁省大连市金普新区2020-2021学年高二下学期开学检测化学试题安徽省芜湖市第一中学2021-2022学年高二上学期第一次月末诊断测试化学试题河南省南阳市第一中学校2021-2022学年高二上学期第二次月考化学试题河南省重点高中2021-2022学年高二上学期阶段性调研联考二化学试题福建省三明第一中学2023-2024学年高二上学期10月月考化学试题河北省保定市保定部分高中2023-2024学年高二上学期9月月考化学试题河北省邯郸市永年区第二中学 2023-2024学年高二年级上学期第一次月考化学试题福建省漳州市正兴学校2023-2024学年高二上学期10月月考化学试卷(已下线)2019年9月8日《每日一题》 选修4 每周一测河北省衡水中学2020届高三上学期第四次调研考试化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第3节 化学反应的速率 课时2 浓度、温度、催化剂对化学反应速率的影响人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第一节 化学反应速率 课时3 活化能河南省郑州市郑州中学2020-2021学年高二上学期期中考试化学试题黑龙江省大庆市铁人中学2020-2021学年高二上学期期末考试化学试题选择性必修1(SJ)专题2第一单元课时2 影响化学反应速率的因素河南省郑州国庆中学2021-2022学年高二上学期期中考试化学试题安徽省淮北师范大学附属实验中学2021-2022学年高二上学期期中考试化学试题四川省内江市2021-2022学年高二上学期期末检测题化学试题河南省中原名校联盟2021-2022学年高二上学期第三次适应性联考化学试题山东省济南市莱芜凤城高级中学2021-2022学年高二上学期期中考试化学试题福建省南平市高级中学2022-2023学年高二上学期期中考试化学(选考)试题山东省枣庄市第三中学(实验班)2022-2023学年高二11月线上测试化学试题 山东省济宁市泗水县2022-2023学年高二上学期期中考试化学试题广东省深圳罗湖区202-2023学年高二上学期期末质量检测化学试题山东省青岛第十七中学2022-2023学年高二上学期期末考试化学试题2.1.2影响化学反应速率的因素 课后福建省南平市浦城县2022-2023学年高二上学期11月期中化学试题河北省新乐市第一中学2022-2023学年高二上学期11月期中考试化学试题福建省永安市第九中学2023-2024学年高二上学期期中考试化学试题河北省邯郸市永年区高级中学2023-2024学年高二上学期期中考试化学试题新疆实验中学2023-2024学年高二上学期期中考试化学试题内蒙古赤峰学院附属中学2023-2024学年高二上学期12月期中考试化学试题(已下线)考点06 化学能与热能-2020年高考化学命题预测与模拟试题分类精编河北省石家庄市第二中学2019-2020高一下期末考试化学模拟试题(三)
9 . 根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液 | B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| B | 取5 mL 0.1 mol·L-1KI溶液,加入1 mL 0.1 mol·L-1FeCl3溶液,萃取分液后,向水层滴入KSCN溶液 | 溶液变成血红色 | Fe3+与I-所发生的反应为可逆反应 |
| C | 相同温度下,2 mL 0.1mol/L H2C2O4溶液分别与4mL 0.01mol/L KMnO4溶液及4mL 0.1mol/L KMnO4溶液反应 | 紫色褪去 | 可测定浓度对反应速率的影响 |
| D | 将C12通入小苏打溶液中 | 有气泡产生 | 可制取较高浓度的次氯酸溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 科学家提出如下光分解法制备氢气:
①2Ce4+(aq)+H2O(l)=2Ce3+(aq)+ O2(g)+2H+(aq) ΔH1
O2(g)+2H+(aq) ΔH1
②Ce3+(aq)+H2O(l)=Ce4+(aq)+ H2(g)+OH-(aq) ΔH2
H2(g)+OH-(aq) ΔH2
③H2O(l)=H+(aq)+OH-(aq) ΔH3
④2H2O(l)=2H2(g)+O2(g) ΔH4
下列说法不正确的是( )
①2Ce4+(aq)+H2O(l)=2Ce3+(aq)+
 O2(g)+2H+(aq) ΔH1
O2(g)+2H+(aq) ΔH1②Ce3+(aq)+H2O(l)=Ce4+(aq)+
 H2(g)+OH-(aq) ΔH2
H2(g)+OH-(aq) ΔH2③H2O(l)=H+(aq)+OH-(aq) ΔH3
④2H2O(l)=2H2(g)+O2(g) ΔH4
下列说法不正确的是( )
| A.Ce4+能够降低水分解反应的活化能,提高反应速率 |
| B.Ce3+是反应②和反应③的催化剂 |
| C.上述反应中,ΔH4=2ΔH1+4ΔH2-4ΔH3 |
| D.通常条件下,反应④中生成H2、O2的速率之比为2∶1 |
您最近一年使用:0次
2020-10-17更新
|
271次组卷
|
4卷引用:辽宁省实验中学东戴河分校2020-2021学年高二10月月考化学试题



