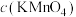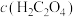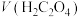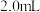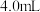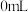名校
解题方法
1 . 某兴趣小组同学将 的酸性
的酸性 溶液和
溶液和 溶液按如下比例混合,探究浓度对反应速率的影响。
溶液按如下比例混合,探究浓度对反应速率的影响。
现象:实验①溶液很快由紫色变为青绿色,而实验②慢一点;变为青绿色后,实验②溶液很快褪至无色,而实验①褪色慢一点。
资料: 与
与 很难形成配合物;
很难形成配合物;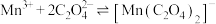 (青绿色),
(青绿色), 有强氧化性,而
有强氧化性,而 氧化性极弱。
氧化性极弱。
下列说法错误的是
 的酸性
的酸性 溶液和
溶液和 溶液按如下比例混合,探究浓度对反应速率的影响。
溶液按如下比例混合,探究浓度对反应速率的影响。序号 | 温度 |
|
|
|
|
|
① | 20℃ |
|
|
|
|
|
② | 20℃ |
|
|
|
|
|
资料:
 与
与 很难形成配合物;
很难形成配合物;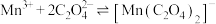 (青绿色),
(青绿色), 有强氧化性,而
有强氧化性,而 氧化性极弱。
氧化性极弱。下列说法错误的是
A. |
B. 溶液中能通过加盐酸酸化调 溶液中能通过加盐酸酸化调 |
C.溶液由青绿色褪至无色过程中,实验①中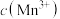 较小,导致褪色速率较慢 较小,导致褪色速率较慢 |
D.由实验可知,加入 越多, 越多, 溶液由紫色褪至无色的速率越快 溶液由紫色褪至无色的速率越快 |
您最近一年使用:0次
2023-06-02更新
|
234次组卷
|
2卷引用:河北省2022-2023学年高三下学期1月大联考化学试题
名校
解题方法
2 . 已知:酸性高锰酸钾溶液与草酸(H2C2O4,二元弱酸)溶液反应时,Mn元素被还原为 (在水溶液中呈无色),氧化产物是CO2.某小组设计下列对比实验探究化学反应速率的影响因素。
(在水溶液中呈无色),氧化产物是CO2.某小组设计下列对比实验探究化学反应速率的影响因素。
回答下列问题:
(1)该反应的离子方程式为___________ 。
(2)该实验需要测定的物理量是___________ 。
(3)实验2和实验3的目的是探究___________ 对反应速率的影响;实验测得实验2的反应速率大于实验1,原因是___________ ,KMnO4氧化性越强,反应速率越快。
(4)要达到对比实验的目的,则a的取值应为___________ ,实验测得实验4的反应速率明显大于实验1,其原因可能是___________ 。
 (在水溶液中呈无色),氧化产物是CO2.某小组设计下列对比实验探究化学反应速率的影响因素。
(在水溶液中呈无色),氧化产物是CO2.某小组设计下列对比实验探究化学反应速率的影响因素。| 实验 | 温度/℃ | 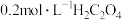 溶液/mL 溶液/mL | 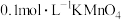 溶液/mL 溶液/mL | 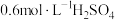 溶液/mL 溶液/mL | 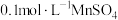 溶液/mL 溶液/mL | 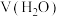 /mL /mL |
| 1 | 25 | 3.0 | 2.0 | 1.0 | 0 | 2.0 |
| 2 | 25 | 3.0 | 2.0 | 2.0 | 0 | 1.0 |
| 3 | 25 | 4.0 | 2.0 | 2.0 | 0 | 0 |
| 4 | 25 | 3.0 | 2.0 | 1.0 | 0.5 | a |
(1)该反应的离子方程式为
(2)该实验需要测定的物理量是
(3)实验2和实验3的目的是探究
(4)要达到对比实验的目的,则a的取值应为
您最近一年使用:0次
2023-05-19更新
|
148次组卷
|
2卷引用:河北省河北南宫中学2022-2023学年高一下学期5月月考化学试题
名校
3 . 作为绿色氧化剂和消毒剂, 在工业生产及日常生活中应用广泛。已知:
在工业生产及日常生活中应用广泛。已知:
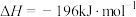 。回答下列问题:
。回答下列问题:
(1)实验表明,在54℃下恒温储存两周, 的浓度仍然保持为原来的99%,这说明
的浓度仍然保持为原来的99%,这说明 分解反应的
分解反应的_______ 。
(2) 催化
催化 分解的原理分为两步:第一步反应的热化学方程式为
分解的原理分为两步:第一步反应的热化学方程式为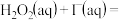
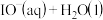
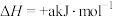 (a>0),则第二步反应的热化学方程式为
(a>0),则第二步反应的热化学方程式为_______ 。已知第一步反应为慢反应,第二步反应为快反应,则能正确表示 催化
催化 分解原理的示意图为
分解原理的示意图为_______ (填标号)。 在不同条件下分解的反应速率,实验室测量气体体积的常用方法如图所示,其中有明显错误的是
在不同条件下分解的反应速率,实验室测量气体体积的常用方法如图所示,其中有明显错误的是_______ (填标号),应当怎样改正?_______ ;四种测量气体体积方法的图示中均用到的仪器包括导管、_______ ;比较 在不同条件下分解的反应速率时,实验中需要测定的数据为
在不同条件下分解的反应速率时,实验中需要测定的数据为_______ 。 催化
催化 分解反应的影响如图所示。
分解反应的影响如图所示。 时,0~10min内
时,0~10min内 分解反应的平均速率
分解反应的平均速率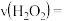
_______  。
。
②下列对图象的分析正确的是_______ (填标号)。
A.相同条件下, 的浓度越小,分解速率越大
的浓度越小,分解速率越大
B.相同条件下,溶液的酸性越强, 的分解速率越大
的分解速率越大
C.在0~50min内, 时
时 的分解百分率比
的分解百分率比 时大
时大
 在工业生产及日常生活中应用广泛。已知:
在工业生产及日常生活中应用广泛。已知:
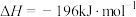 。回答下列问题:
。回答下列问题:(1)实验表明,在54℃下恒温储存两周,
 的浓度仍然保持为原来的99%,这说明
的浓度仍然保持为原来的99%,这说明 分解反应的
分解反应的(2)
 催化
催化 分解的原理分为两步:第一步反应的热化学方程式为
分解的原理分为两步:第一步反应的热化学方程式为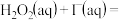
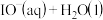
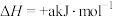 (a>0),则第二步反应的热化学方程式为
(a>0),则第二步反应的热化学方程式为 催化
催化 分解原理的示意图为
分解原理的示意图为
 在不同条件下分解的反应速率,实验室测量气体体积的常用方法如图所示,其中有明显错误的是
在不同条件下分解的反应速率,实验室测量气体体积的常用方法如图所示,其中有明显错误的是 在不同条件下分解的反应速率时,实验中需要测定的数据为
在不同条件下分解的反应速率时,实验中需要测定的数据为A.  B.
B. 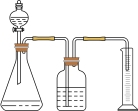 C.
C.  D.
D. 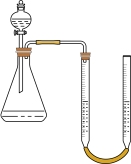
 催化
催化 分解反应的影响如图所示。
分解反应的影响如图所示。
 时,0~10min内
时,0~10min内 分解反应的平均速率
分解反应的平均速率
 。
。②下列对图象的分析正确的是
A.相同条件下,
 的浓度越小,分解速率越大
的浓度越小,分解速率越大B.相同条件下,溶液的酸性越强,
 的分解速率越大
的分解速率越大C.在0~50min内,
 时
时 的分解百分率比
的分解百分率比 时大
时大
您最近一年使用:0次
2022-09-29更新
|
145次组卷
|
3卷引用:河北省唐县第一中学2023-2024学年高二上学期10月考试化学化学
名校
4 . 某研究性学习小组利用 溶液和酸性
溶液和酸性 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)通过实验①、②,可探究出___________ (填外部因素)的改变对化学反应速率的影响;通过实验___________ (填实验序号)可探究出温度变化对化学反应速率的影响。
(2)若 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是___________ ;忽略溶液体积的变化,利用实验②中数据计算,0~8s内,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
___________ 。
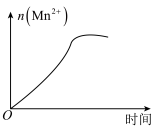
(3)该小组的一位同学通过查阅资料发现,上述实验过程中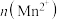 随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对
随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对 与草酸之间的反应有某种特殊作用,则该作用是
与草酸之间的反应有某种特殊作用,则该作用是___________ ,相应的粒子最可能是___________ (填粒子符号)。
 溶液和酸性
溶液和酸性 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:| 实验序号 | 试验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
酸性 溶液 溶液 |  溶液 溶液 |  | |||||
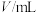 | 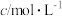 | 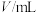 | 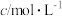 | 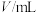 | |||
| ① | 293 | 2 | 0.02 | 4 | 0.1 | 0 |  |
| ② |  | 2 | 0.02 | 3 | 0.1 |  | 8 |
| ③ | 313 | 2 | 0.02 |  | 0.1 | 1 |  |
(2)若
 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应速率
的浓度变化表示的反应速率
(3)该小组的一位同学通过查阅资料发现,上述实验过程中
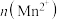 随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对
随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对 与草酸之间的反应有某种特殊作用,则该作用是
与草酸之间的反应有某种特殊作用,则该作用是
您最近一年使用:0次
2023-08-09更新
|
267次组卷
|
2卷引用:河北省保定市保定部分高中2023-2024学年高二上学期9月月考化学试题
2023·江苏南通·一模
解题方法
5 . 化学需氧量(COD)是指用强氧化剂将1L废水中的还原性物质氧化为二氧化碳和水所消耗的氧化剂的量,并换算成以 为氧化剂时所消耗
为氧化剂时所消耗 的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一、Fenton(
的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一、Fenton( )法能产生
)法能产生 和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
(1)羟基自由基(·OH)的电子式为_______ 。
(2)分别取初始pH=4、COD=80的废水200mL,加入200mL ,改变起始投加
,改变起始投加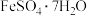 的量,反应相同时间。测得反应后水样COD随
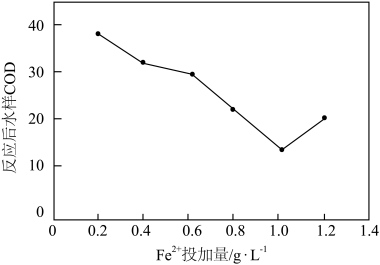
的量,反应相同时间。测得反应后水样COD随 投加量的关系如图所示。当
投加量的关系如图所示。当 投加量超过1
投加量超过1 时,反应后水样COD不降反升的原因可能是
时,反应后水样COD不降反升的原因可能是_______ 。
(3)已知·OH更容易进攻有机物分子中电子云密度较大的基团。1-丁醇比正戊烷更容易受到·OH进攻的原因是_______ 。
(4)在Fenton法的基础上改进的基于硫酸根自由基(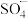 )的氧化技术引起关注。研究发现,一种
)的氧化技术引起关注。研究发现,一种 石墨烯纳米复合材料对催化活化
石墨烯纳米复合材料对催化活化 产生
产生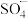 具有很好的效果。
具有很好的效果。 结构为
结构为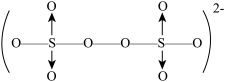 。
。
①与 试剂相比,
试剂相比, 一石墨烯/
一石墨烯/ 的使用范围更广。
的使用范围更广。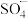 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:_______ 。
②一种制取 一石墨烯纳米复合材料的物种转化关系可表示为(GO表示石墨烯)
一石墨烯纳米复合材料的物种转化关系可表示为(GO表示石墨烯)
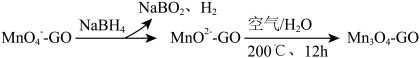
在石墨烯表面制得1mol ,理论上需要消耗
,理论上需要消耗 的物质的量为
的物质的量为_______ mol。
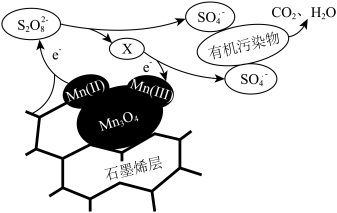
③利用该复合材料催化活化 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为_______ 。
 为氧化剂时所消耗
为氧化剂时所消耗 的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一、Fenton(
的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一、Fenton( )法能产生
)法能产生 和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。(1)羟基自由基(·OH)的电子式为
(2)分别取初始pH=4、COD=80的废水200mL,加入200mL
 ,改变起始投加
,改变起始投加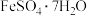 的量,反应相同时间。测得反应后水样COD随
的量,反应相同时间。测得反应后水样COD随 投加量的关系如图所示。当
投加量的关系如图所示。当 投加量超过1
投加量超过1 时,反应后水样COD不降反升的原因可能是
时,反应后水样COD不降反升的原因可能是
(3)已知·OH更容易进攻有机物分子中电子云密度较大的基团。1-丁醇比正戊烷更容易受到·OH进攻的原因是
(4)在Fenton法的基础上改进的基于硫酸根自由基(
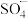 )的氧化技术引起关注。研究发现,一种
)的氧化技术引起关注。研究发现,一种 石墨烯纳米复合材料对催化活化
石墨烯纳米复合材料对催化活化 产生
产生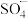 具有很好的效果。
具有很好的效果。 结构为
结构为 。
。①与
 试剂相比,
试剂相比, 一石墨烯/
一石墨烯/ 的使用范围更广。
的使用范围更广。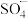 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:②一种制取
 一石墨烯纳米复合材料的物种转化关系可表示为(GO表示石墨烯)
一石墨烯纳米复合材料的物种转化关系可表示为(GO表示石墨烯)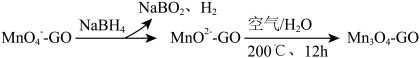
在石墨烯表面制得1mol
 ,理论上需要消耗
,理论上需要消耗 的物质的量为
的物质的量为③利用该复合材料催化活化
 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
您最近一年使用:0次
名校
6 . 根据以下实验操作及现象能得出正确结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有2mL 溶液的试管中滴加1mL 溶液的试管中滴加1mL NaCl溶液,再向其中滴加4~5滴 NaCl溶液,再向其中滴加4~5滴 KI溶液 KI溶液 | 先有白色沉淀生成,后又产生黄色沉淀 |  |
| B | 向等浓度等体积的 中分别加入等浓度等体积的 中分别加入等浓度等体积的 溶液和 溶液和 溶液 溶液 | 前者产生气泡速率快 |  的催化效果比 的催化效果比 好 好 |
| C | 将银粉加到HI溶液中 | 产生无色气体和黄色沉淀 |  和 和 形成沉淀,促进Ag和 形成沉淀,促进Ag和 反应 反应 |
| D | 用铂电极电解等物质的量浓度的 和 和 混合溶液 混合溶液 | 开始时阴极无红色物质析出 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 化学创造美好生活。下列生产活动与对应化学原理没有关联或关联性错误的是
| 选项 | 生产活动 | 化学原理 |
| A | 社区服务:用84消毒液清洗公共桌椅 | 84消毒液中的 有强氧化性 有强氧化性 |
| B | 实践活动:用酵母菌发酵面粉 | 催化剂可以加快反应速率 |
| C | 自主探究:将铁丝分别放在有水和无水环境中观察较长时间 | 钢铁在有水存在的条件下更容易生锈 |
| D | 家务劳动:厨房纸巾擦拭清理电饼铛 | 厨房纸巾表面积大,吸附油污能力强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-26更新
|
546次组卷
|
5卷引用:河北省保定市唐县第一中学2023-2024学年高三上学期11月期中考试化学试题
名校
8 . 用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定。单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如图1所示(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定。单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如图1所示(KMnO4溶液已酸化):

(1)该实验探究的是___________ 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是①___________ ②(填“>”、“<”或“=”)。
(2)若实验①在2 min末收集了4.48 mLCO2(标准状况下),则在2 min末c(MnO )=
)=___________ mol•L-1(假设混合溶液体积为50 mL)
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定___________ 来比较化学反应速率。
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②___________ 。

 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定。单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如图1所示(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定。单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如图1所示(KMnO4溶液已酸化):
| 实验序号 | A溶液 | B溶液 |
| ① | 20 mL0.1 mol•L-1H2C2O4溶液 | 30 mL0.1 mol•L-1KMnO4溶液 |
| ② | 20 mL0.2 mol•L-1H2C2O4溶液 | 30 mL0.1 mol•L-1KMnO4溶液 |
(2)若实验①在2 min末收集了4.48 mLCO2(标准状况下),则在2 min末c(MnO
 )=
)=(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②

您最近一年使用:0次
2021-10-12更新
|
98次组卷
|
3卷引用:河北省邯郸市鸡泽县第一中学2022-2023学年高一下学期第一次月考化学试题
9 . 天津大学某团队通过Ba掺杂 ,缩短Co—Co键长,促进OH吸附,引发O—O偶联的OPM路径,提升酸性体系中的水氧化性能。其历程如图所示。下列叙述错误的是
,缩短Co—Co键长,促进OH吸附,引发O—O偶联的OPM路径,提升酸性体系中的水氧化性能。其历程如图所示。下列叙述错误的是
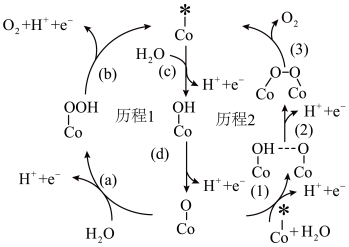
 ,缩短Co—Co键长,促进OH吸附,引发O—O偶联的OPM路径,提升酸性体系中的水氧化性能。其历程如图所示。下列叙述错误的是
,缩短Co—Co键长,促进OH吸附,引发O—O偶联的OPM路径,提升酸性体系中的水氧化性能。其历程如图所示。下列叙述错误的是
| A.历程1中,(a)反应断裂了极性键 | B.历程1中,(b)发生了氧化反应 |
| C.历程2中的基元反应比历程1中多 | D.历程2中,析氧后溶液pH升高 |
您最近一年使用:0次
22-23高三上·河北衡水·阶段练习
10 . 利用“萨巴蒂尔反应”,空间站的水气整合系统将 转化为
转化为 和水蒸气,配合
和水蒸气,配合 生成系统可实现
生成系统可实现 的再生。回答下列问题:
的再生。回答下列问题:
Ⅰ.萨巴蒂尔反应为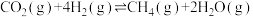

(1)已知25℃和101kPa时,
① 的燃烧热
的燃烧热 ;
;
② 的燃烧热
的燃烧热 ;
;
③
 。
。
则萨巴蒂尔反应的
_______  。
。
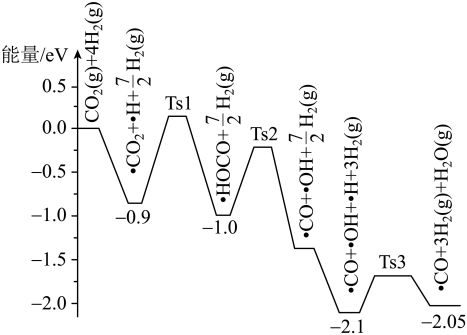
(2)萨巴蒂尔反应的前三步反应历程如图所示,其中吸附在催化剂 表面的物质用“·”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
表面的物质用“·”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会_______ (填“放出”或“吸收”)热量,反应历程中最小能垒(活化能)步骤的化学方程式为_______ 。
Ⅱ. 在一定条件下能与
在一定条件下能与 发生氧再生反应:
发生氧再生反应:

(3)恒压p0条件下,按 投料,进行氧再生反应,测得不同温度下平衡时体系中各物质浓度的关系如图所示。350℃时,该反应的平衡常数
投料,进行氧再生反应,测得不同温度下平衡时体系中各物质浓度的关系如图所示。350℃时,该反应的平衡常数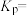
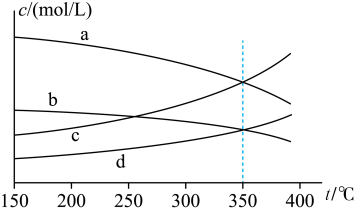
_______ (以分压表示,分压=总压×物质的量分数)。为了提高 的转化率,除升高温度外,还可采取的措施为
的转化率,除升高温度外,还可采取的措施为_______ (写出一条)。
(4)氧再生反应还可以通过酸性条件下半导体光催化转化实现,反应机理如图甲所示:
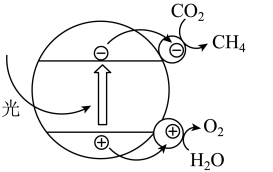
图甲
①光催化 转化为
转化为 时,阴极的电极反应式为
时,阴极的电极反应式为_______ 。
②催化剂的催化效率和 的生成速率随温度的变化关系如图乙所示。300~400℃之间,
的生成速率随温度的变化关系如图乙所示。300~400℃之间, 生成速率加快的原因是
生成速率加快的原因是_______ 。
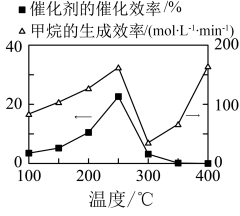
图乙
(5)氧再生反应所需的能量可由合成氨反应提供。合成氨反应的焓变和熵变:

 ,常温(298K)下,合成氨反应的自由能
,常温(298K)下,合成氨反应的自由能
_______  。
。
 转化为
转化为 和水蒸气,配合
和水蒸气,配合 生成系统可实现
生成系统可实现 的再生。回答下列问题:
的再生。回答下列问题:Ⅰ.萨巴蒂尔反应为
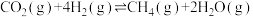

(1)已知25℃和101kPa时,
①
 的燃烧热
的燃烧热 ;
;②
 的燃烧热
的燃烧热 ;
;③

 。
。则萨巴蒂尔反应的

 。
。(2)萨巴蒂尔反应的前三步反应历程如图所示,其中吸附在催化剂
 表面的物质用“·”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
表面的物质用“·”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
Ⅱ.
 在一定条件下能与
在一定条件下能与 发生氧再生反应:
发生氧再生反应:

(3)恒压p0条件下,按
 投料,进行氧再生反应,测得不同温度下平衡时体系中各物质浓度的关系如图所示。350℃时,该反应的平衡常数
投料,进行氧再生反应,测得不同温度下平衡时体系中各物质浓度的关系如图所示。350℃时,该反应的平衡常数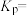
 的转化率,除升高温度外,还可采取的措施为
的转化率,除升高温度外,还可采取的措施为
(4)氧再生反应还可以通过酸性条件下半导体光催化转化实现,反应机理如图甲所示:

图甲
①光催化
 转化为
转化为 时,阴极的电极反应式为
时,阴极的电极反应式为②催化剂的催化效率和
 的生成速率随温度的变化关系如图乙所示。300~400℃之间,
的生成速率随温度的变化关系如图乙所示。300~400℃之间, 生成速率加快的原因是
生成速率加快的原因是
图乙
(5)氧再生反应所需的能量可由合成氨反应提供。合成氨反应的焓变和熵变:


 ,常温(298K)下,合成氨反应的自由能
,常温(298K)下,合成氨反应的自由能
 。
。
您最近一年使用:0次