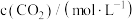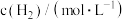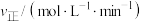1 . 碳达峰、碳中和是现在需要继续完成的环保任务, 的综合利用成为热点研究对象,
的综合利用成为热点研究对象, 作为碳源加氢是再生能源的有效方法,
作为碳源加氢是再生能源的有效方法, 加氢可以合成甲醇,
加氢可以合成甲醇, 提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过
提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过 加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:
加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:
反应I: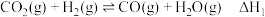
反应Ⅱ:
(1)①相关键能如下表,则
_______ ,该反应的活化能 (正)
(正)_______  (逆)(填“大于”“小于”或“等于”)。
(逆)(填“大于”“小于”或“等于”)。
②已知 的正反应速率
的正反应速率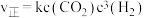 (k为正反应的速率常数),某温度时测得数据如下:
(k为正反应的速率常数),某温度时测得数据如下:
则此温度下,表中
______ 。
(2)据文献报道, 基纳米材料作为高性能催化剂可将
基纳米材料作为高性能催化剂可将 电还原为高能量密度的
电还原为高能量密度的 ,不同催化剂对生成
,不同催化剂对生成 的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是
的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是_______ 。 的转化率随温度和压强的变化如图,判断
的转化率随温度和压强的变化如图,判断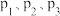 的大小关系:
的大小关系:__________ ;解释压强一定时, 的平衡转化率呈现如图变化的原因:
的平衡转化率呈现如图变化的原因:_________________ 。 ,向容积为
,向容积为 的恒容密闭容器中充入
的恒容密闭容器中充入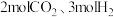 发生反应I、Ⅱ,平衡时
发生反应I、Ⅱ,平衡时 的转化率是
的转化率是 ,体系内剩余
,体系内剩余 ,则反应Ⅱ的平衡常数
,则反应Ⅱ的平衡常数
_______  ,体系内甲醇的平衡分压
,体系内甲醇的平衡分压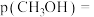
_____  (用含
(用含 的式子表示)。
的式子表示)。
 的综合利用成为热点研究对象,
的综合利用成为热点研究对象, 作为碳源加氢是再生能源的有效方法,
作为碳源加氢是再生能源的有效方法, 加氢可以合成甲醇,
加氢可以合成甲醇,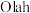 提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过
提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过 加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:
加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:反应I:
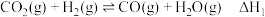
反应Ⅱ:

(1)①相关键能如下表,则

 (正)
(正) (逆)(填“大于”“小于”或“等于”)。
(逆)(填“大于”“小于”或“等于”)。化学键 |
|
|
|
|
键能 | 436 | 1071 | 464 | 803 |
 的正反应速率
的正反应速率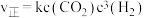 (k为正反应的速率常数),某温度时测得数据如下:
(k为正反应的速率常数),某温度时测得数据如下:
|
|
| |
1 | 0.02 | 0.01 |
|
2 | 0.02 | 0.02 | a |

(2)据文献报道,
 基纳米材料作为高性能催化剂可将
基纳米材料作为高性能催化剂可将 电还原为高能量密度的
电还原为高能量密度的 ,不同催化剂对生成
,不同催化剂对生成 的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是
的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是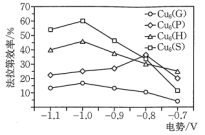
 的转化率随温度和压强的变化如图,判断
的转化率随温度和压强的变化如图,判断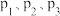 的大小关系:
的大小关系: 的平衡转化率呈现如图变化的原因:
的平衡转化率呈现如图变化的原因:
 ,向容积为
,向容积为 的恒容密闭容器中充入
的恒容密闭容器中充入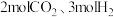 发生反应I、Ⅱ,平衡时
发生反应I、Ⅱ,平衡时 的转化率是
的转化率是 ,体系内剩余
,体系内剩余 ,则反应Ⅱ的平衡常数
,则反应Ⅱ的平衡常数
 ,体系内甲醇的平衡分压
,体系内甲醇的平衡分压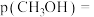
 (用含
(用含 的式子表示)。
的式子表示)。
您最近一年使用:0次
2 . 甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:
(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________。
(2)在一定体积的密闭容器中,进行如下化学反应: 其化学平衡常数K和温度t的关系如下:
其化学平衡常数K和温度t的关系如下:
回答下列问题:
①该反应___________ 反应(选填吸热、放热),平衡常数表达式K=___________ 。
②能判断该反应是否达到化学平衡状态的依据是___________ 。
a.容器中压强不变 b.混合气体中c(CO)不变
c. v正(H2)=v逆(H2O) d. c(CO2)=c(CO)
③830℃时,若起始时加入CO2、H2均为0.05mol,该温度下达到平衡时CO2转化率是___________ 。

(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________。
| A.随时将CH3OH与反应混合物分离 | B.降低反应温度 |
| C.增大体系压强 | D.使用高效催化剂 |
 其化学平衡常数K和温度t的关系如下:
其化学平衡常数K和温度t的关系如下:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应
②能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中c(CO)不变
c. v正(H2)=v逆(H2O) d. c(CO2)=c(CO)
③830℃时,若起始时加入CO2、H2均为0.05mol,该温度下达到平衡时CO2转化率是
您最近一年使用:0次
2021-11-08更新
|
56次组卷
|
2卷引用:陕西省渭南市尚德中学2021-2022学年高二上学期第二次质量检测化学试题
名校
解题方法
3 . 甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。
Ⅰ.用CO2生产甲醇
(1)已知:H2的燃烧热为-285.8kJ/mol,CH3OH(l)的燃烧热为-725.8kJ/mol,
CH3OH(g)=CH3OH(l) ΔH=-37.3kJ/mol
则CO2(g)+3H2(g) CH3OH(g)+H2O(l)ΔH=
CH3OH(g)+H2O(l)ΔH=__ kJ/mol。
(2)将CO2和H2按物质的量之比1:3充入体积为2.0L的恒容密闭容器中反应,如图1两条曲线分别表示压强为0.1MPa和5.0MPa下CO2转化率随温度的变化关系。

其中a点的平衡常数表达式为:__ 。
②a,b两点化学反应速率分别用Va、Vb表示,则Va__ Vb(填“大于”、“小于”或“等于”)。
(3)在1.0L恒容密闭容器中投入1molCO2和2.75molH2发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是
CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是__ 。
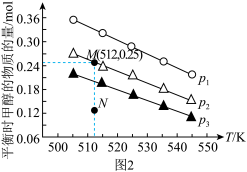
A.该反应的正反应为放热反应
B.压强大小关系为p1<p2<p3
C.M点对应的平衡常数K的值约为1.04×10-2
D.在p2及512K时,图中N点v(正)<v(逆)
Ⅱ.用CO生产甲醇
(4)已知:CO(g)+2H2(g) CH3OH(g),如图3是该反应在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g),如图3是该反应在不同温度下CO的转化率随时间变化的曲线。
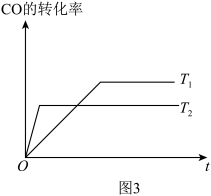
①该反应的焓变ΔH__ 0(填“ ”、“ ”或“ ”)。
②T1和T2温度下的平衡常数大小关系是K1___ K2(填“>”、“<”或“=”)。
Ⅲ.甲醇的应用
(5)甲醇制氢气。甲醇水蒸气重整制氢反应:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49kJ/mol。某温度下,将[n(H2O):n(CH3OH)]=1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为___ 。
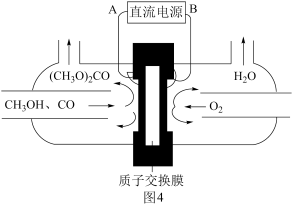
(6)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图4所示。阳极的电极反应式为__ 。
Ⅰ.用CO2生产甲醇
(1)已知:H2的燃烧热为-285.8kJ/mol,CH3OH(l)的燃烧热为-725.8kJ/mol,
CH3OH(g)=CH3OH(l) ΔH=-37.3kJ/mol
则CO2(g)+3H2(g)
 CH3OH(g)+H2O(l)ΔH=
CH3OH(g)+H2O(l)ΔH=(2)将CO2和H2按物质的量之比1:3充入体积为2.0L的恒容密闭容器中反应,如图1两条曲线分别表示压强为0.1MPa和5.0MPa下CO2转化率随温度的变化关系。

其中a点的平衡常数表达式为:
②a,b两点化学反应速率分别用Va、Vb表示,则Va
(3)在1.0L恒容密闭容器中投入1molCO2和2.75molH2发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是
CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是
A.该反应的正反应为放热反应
B.压强大小关系为p1<p2<p3
C.M点对应的平衡常数K的值约为1.04×10-2
D.在p2及512K时,图中N点v(正)<v(逆)
Ⅱ.用CO生产甲醇
(4)已知:CO(g)+2H2(g)
 CH3OH(g),如图3是该反应在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g),如图3是该反应在不同温度下CO的转化率随时间变化的曲线。
①该反应的焓变ΔH
②T1和T2温度下的平衡常数大小关系是K1
Ⅲ.甲醇的应用
(5)甲醇制氢气。甲醇水蒸气重整制氢反应:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49kJ/mol。某温度下,将[n(H2O):n(CH3OH)]=1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为
(6)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图4所示。阳极的电极反应式为

您最近一年使用:0次