1 . 化学与生产、生活密切相关。下列说法错误的是
A.葡萄酒中添加适量的 可以起到杀菌和抗氧化的作用 可以起到杀菌和抗氧化的作用 |
| B.碳酸钡在医疗上可被用作消化系统X射线检查的内服药剂,俗称“钡餐” |
| C.制玻璃过程中加入某些金属氧化物或盐可以得到有色玻璃 |
| D.合成氨工业一般选择400~500℃的主要原因是让催化剂的活性大,反应速率快 |
您最近一年使用:0次
名校
解题方法
2 . 下图所示为工业合成氨的流程图。下列有关生产条件的调控作用分析错误的是
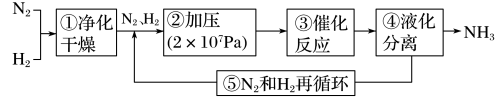
| A.步骤①中“净化”可以防止杂质对催化剂产生影响 |
| B.步骤②中“加压”可以加快反应速率,因此压强越大越好 |
| C.步骤③一般选择控制反应温度为400~500℃左右 |
| D.步骤④⑤有利于提高原料的利用率,能节约生产成本 |
您最近一年使用:0次
名校
解题方法
3 . “中国芯”的发展离不开单晶硅,工业上制高纯硅,先制得粗硅,再制高纯硅。
Ⅰ.请回答:
(1)工业制粗硅反应的化学方程式为___________ 。
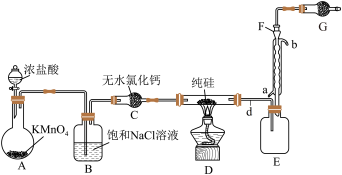
Ⅱ.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
① ,
, ;
;
② 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。
请回答下列问题:
(2)装无水氯化钙的仪器名称是___________ 。
(3)若拆去B装置,可能的后果是___________ (写出一个即可)。
(4)有同学最初将E、F、G装置设计成图甲所示装置,图甲装置的主要缺点是___________ (写出一个即可)。 在高温条件下易分解生成
在高温条件下易分解生成 和
和 。利用
。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图乙,写出该反应的化学方程式:
)的装置如图乙,写出该反应的化学方程式:___________ 。利用尾气制备盐酸,宜选择下列装置中的___________ (填序号)。
(6) 也是制取高纯硅的重要原料,它在浓的
也是制取高纯硅的重要原料,它在浓的 溶液中的反应方程式为
溶液中的反应方程式为___________ 。
Ⅰ.请回答:
(1)工业制粗硅反应的化学方程式为
Ⅱ.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
①
 ,
, ;
;②
 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。请回答下列问题:
(2)装无水氯化钙的仪器名称是
(3)若拆去B装置,可能的后果是
(4)有同学最初将E、F、G装置设计成图甲所示装置,图甲装置的主要缺点是
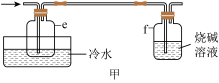
 在高温条件下易分解生成
在高温条件下易分解生成 和
和 。利用
。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图乙,写出该反应的化学方程式:
)的装置如图乙,写出该反应的化学方程式: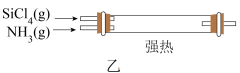

(6)
 也是制取高纯硅的重要原料,它在浓的
也是制取高纯硅的重要原料,它在浓的 溶液中的反应方程式为
溶液中的反应方程式为
您最近一年使用:0次
2024-01-06更新
|
1091次组卷
|
4卷引用:河北省廊坊市2023-2024学年高一下学期3月月考化学试题
河北省廊坊市2023-2024学年高一下学期3月月考化学试题贵州省贵阳市第一中学2023-2024学年高三上学期11月高考适应性月考化学试卷(三)(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
4 . 二氧化氯(ClO2)具有强氧化性,是优良的饮用水消毒剂。ClO2常温下为黄绿色气体,熔点-59℃,沸点11℃,极易溶于水且不与水反应,浓的ClO2受热时易爆炸。我国广泛使用的方法是用干燥的Cl2与NaClO2固体反应制取ClO2,实验室模拟制备ClO2装置如图所示:
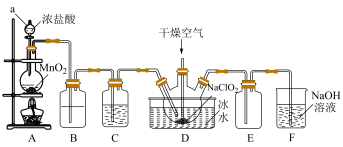
(1)仪器a的名称是:___________ ,装置A中反应的离子方程式为:___________ 。
(2)装置B中盛装的试剂是___________ ,装置C中试剂的作用是:___________ 。
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②___________ 。
(4)装置E为ClO2的收集装置,应将其置于___________ 水浴中(填“热”或“冰”)。
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:___________ 。
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若___________ (填“实验现象”),则假设1成立。

(1)仪器a的名称是:
(2)装置B中盛装的试剂是
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②
(4)装置E为ClO2的收集装置,应将其置于
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若
您最近一年使用:0次
2023-11-06更新
|
632次组卷
|
2卷引用:江西省广信中学2023-2024学年高一上学期11月月考化学试题
5 . 工业合成氨反应为N2(g)+3H2(g)⇌2NH3(g),氨在工农业生产中应用广泛。
(1)已知:键能是1mol化学键完全断裂形成气态原子所需要吸收的能量,部分化学键的键能如表格所示。计算每合成2molNH3可以_______ (填“放出”或“吸收”)热量_______ kJ。
(2)实验室中模拟合成氨过程,将1mol 和2.7mol
和2.7mol 置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是_______ (填序号)。
a.反应不再进行,已经停止
b.单位时间内生成nmol 的同时生成3nmol
的同时生成3nmol
c.2υ(H2)=υ(NH3)
d. 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2
e.混合气体的压强不再改变
f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2 mol∙L−1,则用氨气表示的0~10min内的平均化学反应速率为_______ 。
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
实际生产时,通常采用铁触媒作为催化剂、在400~500℃和10~30MPa的条件下合成氨。结合所学知识以及上述表格数据分析,工业上采用400~500℃反应的原因是_______ 。
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。
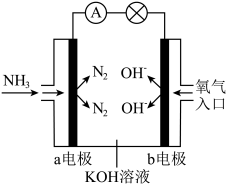
a电极是_______ (填“正极”或“负极”)。b电极的电极反应式是_______ 。
| 化学键 | H−H | N−H | N≡N |
键能( ) ) | 436 | 391 | 945.6 |
(1)已知:键能是1mol化学键完全断裂形成气态原子所需要吸收的能量,部分化学键的键能如表格所示。计算每合成2molNH3可以
(2)实验室中模拟合成氨过程,将1mol
 和2.7mol
和2.7mol 置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是a.反应不再进行,已经停止
b.单位时间内生成nmol
 的同时生成3nmol
的同时生成3nmol
c.2υ(H2)=υ(NH3)
d.
 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2e.混合气体的压强不再改变
f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2 mol∙L−1,则用氨气表示的0~10min内的平均化学反应速率为
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
压强(MPa)氨的平衡 含量(%) 温度(摄氏度) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。

a电极是
您最近一年使用:0次
6 . 一种锌电解阳极,主要成分为Ag、MnO2、PbSO4和ZnO,还有少量锰铅氧化物Pb2Mn8O16(Mn元素化合价为+2和+4两种),可用于回收金属元素锌、锰、铅和银的工艺,如图所示。回答下列问题:
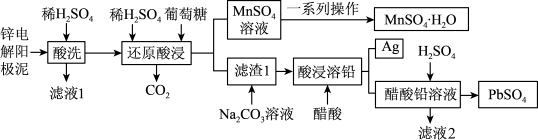
已知:①MnSO4·H2O易溶于水,不溶于乙醇。
②在较高温度及酸性催化条件下,葡萄糖能发生如下反应:
葡萄糖(C6H12O6)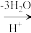
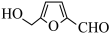
 + HCOOH
+ HCOOH
③在一定条件下, + PbSO4=PbCO3+
+ PbSO4=PbCO3+
(1)经过“酸洗"后的滤渣中主要的成分有___________ 。
(2)“还原酸浸”过程中主要反应的化学方程式为___________ 。
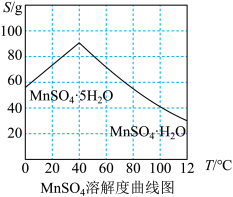
(3)结合MnSO4溶解度曲线图分析,由MnSO4溶液制得MnSO4·H2O晶体的“一系列操作”是___________ ,用___________ (填物质的名称)洗涤、干燥。
(4)实际锰浸出最适宜的葡萄糖加入量远大于理论加入量,其原因是___________ ,为提高葡萄糖的有效利用率(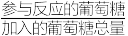 ×100%),除了充分搅拌外还可以
×100%),除了充分搅拌外还可以___________ 。
(5)关于流程中有关物质的说法正确的是___________(填标号)。

已知:①MnSO4·H2O易溶于水,不溶于乙醇。
②在较高温度及酸性催化条件下,葡萄糖能发生如下反应:
葡萄糖(C6H12O6)
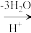

 + HCOOH
+ HCOOH③在一定条件下,
 + PbSO4=PbCO3+
+ PbSO4=PbCO3+
(1)经过“酸洗"后的滤渣中主要的成分有
(2)“还原酸浸”过程中主要反应的化学方程式为
(3)结合MnSO4溶解度曲线图分析,由MnSO4溶液制得MnSO4·H2O晶体的“一系列操作”是

(4)实际锰浸出最适宜的葡萄糖加入量远大于理论加入量,其原因是
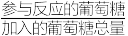 ×100%),除了充分搅拌外还可以
×100%),除了充分搅拌外还可以(5)关于流程中有关物质的说法正确的是___________(填标号)。
| A.为了提高“还原酸浸”的浸出效率,可以大幅提高温度 |
| B.滤液1中含有Mn2+、Pb2+和Zn2+ |
| C.可以采用金属Na与ZnSO4溶液反应,置换出金属锌 |
| D.流程中的“滤液2”可循环利用 |
您最近一年使用:0次
名校
解题方法
7 . 金属钛具有密度小、强度高、耐腐蚀、无毒等优点,已广泛应用于航空航天工业,并逐步进入了化工、船舶、汽车、体育器材、医疗等民用领域,并显示出了巨大的发展潜力。还原法是工业上冶炼钛常用方法之一,该方法是以金红石(主要含 )为原料来制取,其主要工艺流程如下:
)为原料来制取,其主要工艺流程如下:
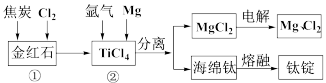
试回答下列问题:
(1)已知反应①通常在800~900℃的条件下进行,产物中有一种可燃性无色气体,写出反应①的化学方程式___________ 。
(2)反应②通常在800℃的条件下进行,通入氩气的目的是___________ ;
(3)下列推断不合理的是___________
(4)分离反应2的产物所得到的海绵钛中常混有少量杂质,应如何除去杂质?___________ 简述操作过程)。
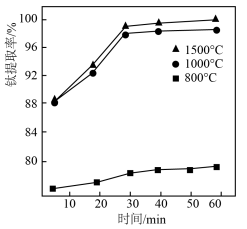
(5)②中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为___________ ℃。
 )为原料来制取,其主要工艺流程如下:
)为原料来制取,其主要工艺流程如下:
试回答下列问题:
(1)已知反应①通常在800~900℃的条件下进行,产物中有一种可燃性无色气体,写出反应①的化学方程式
(2)反应②通常在800℃的条件下进行,通入氩气的目的是
(3)下列推断不合理的是___________
| A.钛在高温下可能易与氧气反应 |
| B.镁的熔点比钛的熔点高 |
| C.钛的金属活动性比镁的金属活动性强 |
D.反应②产生的 可作为电解法制取镁的原料 可作为电解法制取镁的原料 |
(5)②中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为

您最近一年使用:0次
名校
解题方法
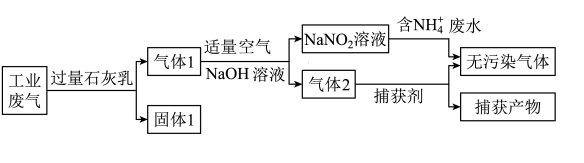
8 . 自国家实施“青山绿水”工程以来,对于“工业三废”的处理越来越受到人们的重视。某工厂为综合处理含 废水和工业废气(主要含有N2、SO2、NO、CO,不考虑其他成分)而设计的工艺流程如图所示。
废水和工业废气(主要含有N2、SO2、NO、CO,不考虑其他成分)而设计的工艺流程如图所示。
已知: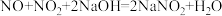 ;
; 。
。
(1)固体1的成分为Ca(OH)2和___________ ;由捕获剂所捕获的气体为___________ 。
(2)在处理气体1时,通入空气不宜过量的原因是___________ 。
(3)使用NaNO2溶液处理含 废水的离子方程式为
废水的离子方程式为___________ ,采用此方法每处理1 mol ,转移电子的物质的量为
,转移电子的物质的量为___________ 。
(4)研究发现采用Fe0.35(CeZr)x催化剂可将CO、NO同时转化为无污染气体,反应方程式为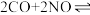
 。不过,该过程常伴有副反应
。不过,该过程常伴有副反应 ,生成有害气体N2O。如图是采用不同铈锆掺杂量的Fe0.35(CeZr)x样品处理工业废气的结果。其中,N2选择性
,生成有害气体N2O。如图是采用不同铈锆掺杂量的Fe0.35(CeZr)x样品处理工业废气的结果。其中,N2选择性 ,N2选择性越高,发生的副反应越少。
,N2选择性越高,发生的副反应越少。
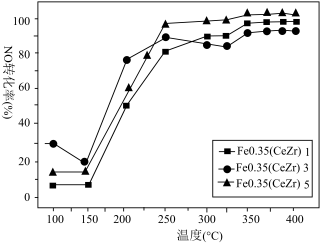
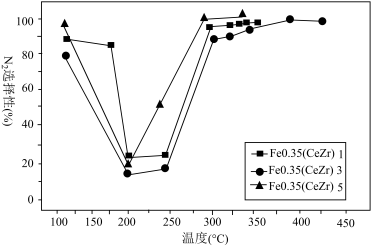
①由图可知,采用该方法处理工业废气的最佳催化剂和温度是___________ 。
②假设NO的起始物质的量为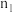 ,采用该方法处理达到平衡时生成N2的物质的量为
,采用该方法处理达到平衡时生成N2的物质的量为 ,N2选择性为S,则此时NO转化率为
,N2选择性为S,则此时NO转化率为___________ 。(用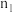 、
、 、S的代数式表示)
、S的代数式表示)
 废水和工业废气(主要含有N2、SO2、NO、CO,不考虑其他成分)而设计的工艺流程如图所示。
废水和工业废气(主要含有N2、SO2、NO、CO,不考虑其他成分)而设计的工艺流程如图所示。
已知:
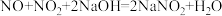 ;
; 。
。(1)固体1的成分为Ca(OH)2和
(2)在处理气体1时,通入空气不宜过量的原因是
(3)使用NaNO2溶液处理含
 废水的离子方程式为
废水的离子方程式为 ,转移电子的物质的量为
,转移电子的物质的量为(4)研究发现采用Fe0.35(CeZr)x催化剂可将CO、NO同时转化为无污染气体,反应方程式为
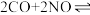
 。不过,该过程常伴有副反应
。不过,该过程常伴有副反应 ,生成有害气体N2O。如图是采用不同铈锆掺杂量的Fe0.35(CeZr)x样品处理工业废气的结果。其中,N2选择性
,生成有害气体N2O。如图是采用不同铈锆掺杂量的Fe0.35(CeZr)x样品处理工业废气的结果。其中,N2选择性 ,N2选择性越高,发生的副反应越少。
,N2选择性越高,发生的副反应越少。

①由图可知,采用该方法处理工业废气的最佳催化剂和温度是
②假设NO的起始物质的量为
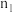 ,采用该方法处理达到平衡时生成N2的物质的量为
,采用该方法处理达到平衡时生成N2的物质的量为 ,N2选择性为S,则此时NO转化率为
,N2选择性为S,则此时NO转化率为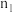 、
、 、S的代数式表示)
、S的代数式表示)
您最近一年使用:0次
2023-05-03更新
|
330次组卷
|
2卷引用:北京市第五中学2022-2023学年高一下学期第一次阶段检测化学试题
9 . 工厂烟气(主要污染物 、NO)直接排放会造成空气污染,需处理后才能排放。
、NO)直接排放会造成空气污染,需处理后才能排放。
(1)①用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中 的相关反应的热化学方程式如下:
的相关反应的热化学方程式如下:
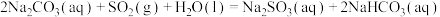
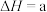 kJ·mol
kJ·mol
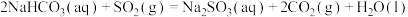
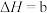 kJ·mol
kJ·mol
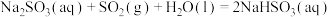
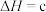 kJ·mol
kJ·mol
反应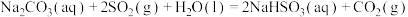 的
的
______ kJ·mol
②已知拆开1 mol 键,1 mol
键,1 mol  键,1 mol
键,1 mol  键分别需要的能量是436 kJ、391 kJ、946 kJ,则
键分别需要的能量是436 kJ、391 kJ、946 kJ,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为______
(2) 氧化。
氧化。
40℃时向一定量 溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。
溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。
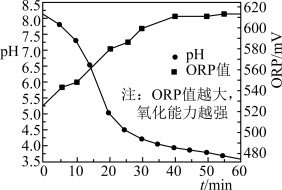
①写出溶液中NO与 反应生成
反应生成 和
和 的离子方程式:
的离子方程式:______ 。
②烟气中含有少量 ,NO的脱除率比不含
,NO的脱除率比不含 的烟气高,可能原因是
的烟气高,可能原因是______ 。
(3) 光催化。主要是利用
光催化。主要是利用 光催化剂在紫外线作用下产生的高活性自由基(
光催化剂在紫外线作用下产生的高活性自由基(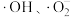 )和
)和 (
( 代表空位,空位有很强的得电子能力),将烟气中的
代表空位,空位有很强的得电子能力),将烟气中的 、NO等氧化除去。
、NO等氧化除去。 光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知
光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知 中电子跃迁的能量
中电子跃迁的能量 eV。
eV。
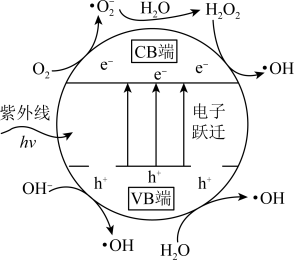
 光催化剂在紫外线作用下产生·OH的过程可描述为
光催化剂在紫外线作用下产生·OH的过程可描述为______ 。
 、NO)直接排放会造成空气污染,需处理后才能排放。
、NO)直接排放会造成空气污染,需处理后才能排放。(1)①用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中
 的相关反应的热化学方程式如下:
的相关反应的热化学方程式如下: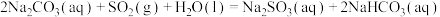
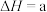 kJ·mol
kJ·mol
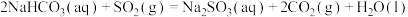
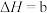 kJ·mol
kJ·mol
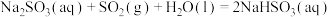
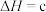 kJ·mol
kJ·mol
反应
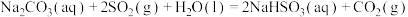 的
的

②已知拆开1 mol
 键,1 mol
键,1 mol  键,1 mol
键,1 mol  键分别需要的能量是436 kJ、391 kJ、946 kJ,则
键分别需要的能量是436 kJ、391 kJ、946 kJ,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为(2)
 氧化。
氧化。40℃时向一定量
 溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。
溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。
①写出溶液中NO与
 反应生成
反应生成 和
和 的离子方程式:
的离子方程式:②烟气中含有少量
 ,NO的脱除率比不含
,NO的脱除率比不含 的烟气高,可能原因是
的烟气高,可能原因是(3)
 光催化。主要是利用
光催化。主要是利用 光催化剂在紫外线作用下产生的高活性自由基(
光催化剂在紫外线作用下产生的高活性自由基(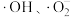 )和
)和 (
( 代表空位,空位有很强的得电子能力),将烟气中的
代表空位,空位有很强的得电子能力),将烟气中的 、NO等氧化除去。
、NO等氧化除去。 光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知
光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知 中电子跃迁的能量
中电子跃迁的能量 eV。
eV。
 光催化剂在紫外线作用下产生·OH的过程可描述为
光催化剂在紫外线作用下产生·OH的过程可描述为
您最近一年使用:0次
名校
解题方法
10 . 规范、科学处置废旧锂离子电池具有重要的环保意义和经济价值。废磷酸铁锂粉主要成分为LiFePO4,还含有杂质铝、铜、镁。回收LiCl的工艺流程如下:
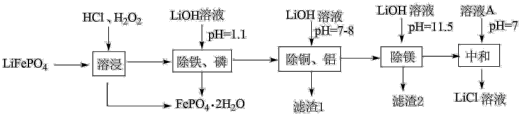
(1)LiFePO4中Fe的化合价为_______ ,Fe在周期表中的位置为_______ 。
(2)溶液A为_______ 。
(3)“溶浸”可得到含氯化锂的浸出液,材料中的杂质铝、铜、镁等金属杂质也会溶入浸出液,生成氯化铜的离子方程式为_______ 。生成FePO4·2H2O的离子方程式为_______ 。
(4)工业通过处理废旧钴酸锂电池正极材料(主要成分为LiCoO2,含少量金属Cu等)回收Co和Li。
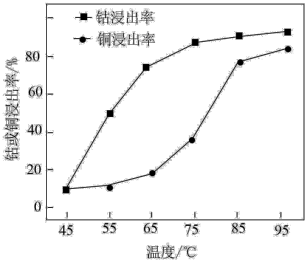
①将预处理后的正极材料粉碎,加入3mol·L-1硫酸和30%H2O2的混合溶液。写出酸浸时生成Li2SO4和CoSO4的化学方程式:_______ 。其他条件相同,浸泡1h,不同温度下钴或铜的浸出率如下图所示。从75℃~85℃,铜浸出率增大的幅度明显高于65℃~75℃增大的幅度,原因是_______ 。
②沉钴,回收Co(OH)2,测定Co(OH)2的含量。Co(OH)2在空气中易被氧化为CoOOH。在稀硫酸中加入0.1000gCo(OH)2样品,待样品完全溶解后加入1.000gKI固体。充分反应后,调节溶液pH=3~4。以淀粉作指示剂,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液25.00mL。已知:Co3++I-→Co2++I2(未配平);I2+S2O →I-+S4O
→I-+S4O (未配平)。计算样品中Co(OH)2的质量分数
(未配平)。计算样品中Co(OH)2的质量分数_______ (写出计算过程)。

(1)LiFePO4中Fe的化合价为
(2)溶液A为
(3)“溶浸”可得到含氯化锂的浸出液,材料中的杂质铝、铜、镁等金属杂质也会溶入浸出液,生成氯化铜的离子方程式为
(4)工业通过处理废旧钴酸锂电池正极材料(主要成分为LiCoO2,含少量金属Cu等)回收Co和Li。
①将预处理后的正极材料粉碎,加入3mol·L-1硫酸和30%H2O2的混合溶液。写出酸浸时生成Li2SO4和CoSO4的化学方程式:

②沉钴,回收Co(OH)2,测定Co(OH)2的含量。Co(OH)2在空气中易被氧化为CoOOH。在稀硫酸中加入0.1000gCo(OH)2样品,待样品完全溶解后加入1.000gKI固体。充分反应后,调节溶液pH=3~4。以淀粉作指示剂,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液25.00mL。已知:Co3++I-→Co2++I2(未配平);I2+S2O
 →I-+S4O
→I-+S4O (未配平)。计算样品中Co(OH)2的质量分数
(未配平)。计算样品中Co(OH)2的质量分数
您最近一年使用:0次



