名校
解题方法
1 . SO2和H2S是大气污染物,这两种气体的转化研究对资源综合利用和环境保护有重要意义。
Ⅰ.水煤气还原法
已知:①2H2(g)+SO2(g)=S(1)+2H2O(g) ΔH1=+45.4kJ·mol-1
②2CO(g)+SO2(g)=S(1)+2CO2(g) ΔH2=-37.0kJ·mol-1
(1)写出CO(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式___________ ;若该反应在恒温恒容体系中进行,则其达到平衡的标志为___________ (填字母)。
A.单位时间内,生成nmolCO的同时生成nmolCO2
B.混合气体的平均摩尔质量保持不变
C.混合气体的总压强保持不变
D.CO2(g)与H2(g)的体积比保持不变
(2)在温度为T℃下,将1.4molH2和1molSO2通入2L恒容密闭容器中发生上述反应①2H2(g)+SO2(g)=S(1)+2H2O(g),反应体系中气体的总压强随时间变化如图所示。SO2的平衡转化率α(SO2)=___________ 。

(3)某密闭容器中发生上述反应②2CO(g)+SO2(g)=S(1)+2CO2(g),平衡时CO的体积分数(%)与压强和温度的关系如图所示。

则T1、T2、T3由小到大的关系顺序是___________ ,判断的理由是___________ 。
Ⅱ.碱液吸收法
(4)用K2CO3溶液吸收H2S,其原理为CO +H2S=HS-+HCO
+H2S=HS-+HCO 。该反应的平衡常数K=
。该反应的平衡常数K=___________ 。(已知H2CO3的Ka1=4.2×10-7,Ka2=5.6×10-11;H2S的Ka1=5.6×10-8,Ka2=1.2×10-15)
Ⅰ.水煤气还原法
已知:①2H2(g)+SO2(g)=S(1)+2H2O(g) ΔH1=+45.4kJ·mol-1
②2CO(g)+SO2(g)=S(1)+2CO2(g) ΔH2=-37.0kJ·mol-1
(1)写出CO(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式
A.单位时间内,生成nmolCO的同时生成nmolCO2
B.混合气体的平均摩尔质量保持不变
C.混合气体的总压强保持不变
D.CO2(g)与H2(g)的体积比保持不变
(2)在温度为T℃下,将1.4molH2和1molSO2通入2L恒容密闭容器中发生上述反应①2H2(g)+SO2(g)=S(1)+2H2O(g),反应体系中气体的总压强随时间变化如图所示。SO2的平衡转化率α(SO2)=

(3)某密闭容器中发生上述反应②2CO(g)+SO2(g)=S(1)+2CO2(g),平衡时CO的体积分数(%)与压强和温度的关系如图所示。

则T1、T2、T3由小到大的关系顺序是
Ⅱ.碱液吸收法
(4)用K2CO3溶液吸收H2S,其原理为CO
 +H2S=HS-+HCO
+H2S=HS-+HCO 。该反应的平衡常数K=
。该反应的平衡常数K=
您最近一年使用:0次
名校
2 . CO和NO是汽车尾气中的主要污染物,易引起酸雨、温室效应和光化学烟雾等环境污染问题。随着我国机动车保有量的飞速发展,汽车尾气的有效处理变得迫在眉睫。其中的一种方法为2CO(g)+2NO(g)=N2(g)+2CO2(g),请回答下列问题:
(1)已知该反应为自发反应,则该反应的反应热△H___________ 0(填“>”或“<”或“=”)
(2)已知:N2 (g) + O2(g)=2NO(g) △H= a kJ•mol-1
C(s) + O2 (g)=CO2 (g) △H= b kJ•mol-1
2C(s) + O2 (g)=2CO(g) △H= c kJ•mol-1
则 2CO(g)+2NO(g)=N2 (g)+2CO2 (g) △H=___________ kJ•mol-1 (用含 a、b、c 的表达式表示)。
(3)一定温度下,将 2molCO、4molNO 充入一恒压密闭容器。已知起始压强为 1MPa,到达平衡时, 测得N2的物质的量为 0.5 mol,则:
①该温度此反应用平衡分压代替平衡浓度的平衡常数Kp=___________ (可用分数表示)
②该条件下,可判断此反应到达平衡的标志是___________
A.单位时间内,断裂 2 molC=O 同时形成 1 mol N≡N。
B.混合气体的密度不再改变。
C.混合气体的平均相对分子质量不再改变。
D.CO与NO的转化率比值不再改变。
(4)某研究小组探究催化剂对 CO、NO 转化的影响。将 CO 和 NO 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中 N2的含量,从而确定尾气脱氮率(即 NO 的转化率),结果如图所示:

①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为___________ ,
②高于 200℃,图中曲线 I 脱氮率随温度升高降低的主要原因为___________ 。
(5)已知常温下,Kb(NH3·H2O)=1.8×10-5,Ka1(H2CO3) =4.4×10-7,Ka2(H2CO3) =4.4×10-11。此温度下某氨水的浓度为 2mol/L,则溶液中c(OH-)=___________ mol/L,将脱氮反应后生成CO2通入氨水中使溶液恰好呈中性,则此时 =
=___________ 。(保留小数点后4位数字)
(6)电解NO制备NH4NO3,其工作原理如图所示:

写出阳极反应的电极反应方程式___________ ,为使电解产物全部转化为NH4NO3,需要补充物质A,A是___________ 。
(1)已知该反应为自发反应,则该反应的反应热△H
(2)已知:N2 (g) + O2(g)=2NO(g) △H= a kJ•mol-1
C(s) + O2 (g)=CO2 (g) △H= b kJ•mol-1
2C(s) + O2 (g)=2CO(g) △H= c kJ•mol-1
则 2CO(g)+2NO(g)=N2 (g)+2CO2 (g) △H=
(3)一定温度下,将 2molCO、4molNO 充入一恒压密闭容器。已知起始压强为 1MPa,到达平衡时, 测得N2的物质的量为 0.5 mol,则:
①该温度此反应用平衡分压代替平衡浓度的平衡常数Kp=
②该条件下,可判断此反应到达平衡的标志是
A.单位时间内,断裂 2 molC=O 同时形成 1 mol N≡N。
B.混合气体的密度不再改变。
C.混合气体的平均相对分子质量不再改变。
D.CO与NO的转化率比值不再改变。
(4)某研究小组探究催化剂对 CO、NO 转化的影响。将 CO 和 NO 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中 N2的含量,从而确定尾气脱氮率(即 NO 的转化率),结果如图所示:

①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为
②高于 200℃,图中曲线 I 脱氮率随温度升高降低的主要原因为
(5)已知常温下,Kb(NH3·H2O)=1.8×10-5,Ka1(H2CO3) =4.4×10-7,Ka2(H2CO3) =4.4×10-11。此温度下某氨水的浓度为 2mol/L,则溶液中c(OH-)=
 =
=(6)电解NO制备NH4NO3,其工作原理如图所示:

写出阳极反应的电极反应方程式
您最近一年使用:0次
解题方法
3 . 某温度时,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
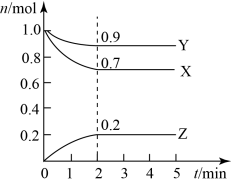
(1)由图中所给数据进行分析,该反应的化学方程式为___________ 。
(2)反应从开始至2min,平均反应速率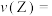
___________  。
。
(3)1min时,
___________ (填“>”、“<”或“=”)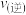 。
。
(4)能说明该反应已达到平衡状态的是___________(填字母)。
(5)2min后反应达平衡,容器内混合气体的平均相对分子质量比起始时_____ (填“增大”“减小”或“不变”,下同):混合气体的密度比起始时___________ 。

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)反应从开始至2min,平均反应速率
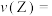
 。
。(3)1min时,

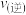 。
。(4)能说明该反应已达到平衡状态的是___________(填字母)。
A.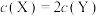 | B.消耗1molY的同时生成2molZ |
C. | D.容器内Z的浓度保持不变 |
您最近一年使用:0次
解题方法
4 . 某温度下,可逆反应: 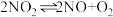 在体积固定的密闭容器中反应,达到平衡的标志是
在体积固定的密闭容器中反应,达到平衡的标志是
①单位时间内生成nmolO2的同时,生成2nmolNO2
②单位时间内生成nmolO2的同时,生成2nmolNO
③混合气体的颜色不再改变的状态
④混合气体的密度不再改变的状态
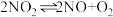 在体积固定的密闭容器中反应,达到平衡的标志是
在体积固定的密闭容器中反应,达到平衡的标志是①单位时间内生成nmolO2的同时,生成2nmolNO2
②单位时间内生成nmolO2的同时,生成2nmolNO
③混合气体的颜色不再改变的状态
④混合气体的密度不再改变的状态
| A.③④ | B.①③ | C.②③ | D.①② |
您最近一年使用:0次
解题方法
5 . 在恒温恒容条件,可逆反应A(g)+3B(g)⇌2C(g)达到平衡的标志是
| A.容器中压强不再变化 | B.A、B、C的浓度相等 |
| C.A、B、C的分子数比为1:3:2 | D.单位时间消耗nmolA,同时生成2nmolC |
您最近一年使用:0次
解题方法
6 . 在  的恒容密闭容器中,加入
的恒容密闭容器中,加入  和
和 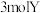 ,在一定条件下发生如下反应:
,在一定条件下发生如下反应: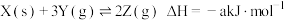 (
( ),3s后生成 Z的物质的量为
),3s后生成 Z的物质的量为  。下列说法不正确的是
。下列说法不正确的是
 的恒容密闭容器中,加入
的恒容密闭容器中,加入  和
和 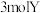 ,在一定条件下发生如下反应:
,在一定条件下发生如下反应: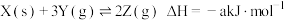 (
( ),3s后生成 Z的物质的量为
),3s后生成 Z的物质的量为  。下列说法不正确的是
。下列说法不正确的是| A.达到化学平衡状态时,正反应速率大于零 |
| B.混合气体的密度不变时,反应达到化学平衡状态 |
C. ,Y的平均反应速率为 ,Y的平均反应速率为 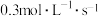 |
D.充分反应后,放出的热量为  |
您最近一年使用:0次
解题方法
7 . 一定温度下的密闭容器中发生可逆反应2SO2(g)+O2(g)⇌2SO3(g),不能说明该反应一定达到平衡状态的是
| A.压强保持不变 |
| B.SO2、O2、SO3的物质的量之比为2︰1︰2 |
| C.SO2的消耗速率和SO2的生成速率相等 |
| D.SO2的百分含量保持不变 |
您最近一年使用:0次
解题方法
8 . 一定温度下,在恒容密闭容器中发生反应:N2(g) +3H2(g) 2NH3(g)。能说明该反应已达化学平衡状态的是
2NH3(g)。能说明该反应已达化学平衡状态的是
 2NH3(g)。能说明该反应已达化学平衡状态的是
2NH3(g)。能说明该反应已达化学平衡状态的是| A.正、逆反应速率都等于零 | B. N2和H2全部转化为NH3 |
| C. N2、H2和NH3的浓度不再变化 | D. N2、H2和NH3的物质的量之比为1:3:2 |
您最近一年使用:0次
解题方法
9 . 在一定温度下的恒容密闭容器中,发生反应 ,下列能判断该反应已达到化学平衡状态的标志是
,下列能判断该反应已达到化学平衡状态的标志是
 ,下列能判断该反应已达到化学平衡状态的标志是
,下列能判断该反应已达到化学平衡状态的标志是A. 和 和 的物质的量浓度之和不再变化 的物质的量浓度之和不再变化 | B.混合气体的分子总数不再变化 |
| C.混合气体的密度不再变化 | D. 的物质的量不再变化 的物质的量不再变化 |
您最近一年使用:0次
名校
解题方法
10 . 在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g)⇌2Z(g)此反应达到平衡的标志是
| A.容器内压强不随时间变化 |
| B.容器内X、Y、Z的浓度之比为1︰2︰2 |
| C.容器内各物质的浓度随时间变化 |
| D.单位时间消耗0.1molX同时生成0.2molZ |
您最近一年使用:0次
2022-12-02更新
|
214次组卷
|
2卷引用:陕西省安康市汉滨区五里高级中学2021-2022学年高二上学期期中考试化学试题



