1 . 甲醇是一种高效清洁的新能源,已知在常温常压下:
① CO2(g)+3H2(g) = CH3OH(l)+ H2O(l) ΔH1=-184.0 kJ/mol
② 2H2 (g)+ O2(g) = 2H2O(l) ΔH2=-572.0 kJ/mol
(1)则表示CH3OH(l)燃烧热的热化学方程式__________________________________ 。
在恒温恒容的密闭容器中,工业上常用反应①:CO(g)+2H2(g)⇌CH3OH(g) ΔH1<0 制备甲醇;其中的原料气常用反应②:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH2 来制备。根据题意完成下列各题:
(2)判断反应①达到平衡状态的标志是__________ (填字母)。
a.容器中气体的压强不变 b.CO 和CH3OH 浓度相等
c.V 消耗(CH3OH)= V 生成(CO) d.容器中混合气体的密度保持不变
e.混合气体的平均相对分子质量不发生变化
(3)欲提高反应①中CO 的转化率,下列措施可行的是_____ (填字母)。
a. 减小容器容积 b.升高温度
c.向装置中再充入He d.向装置中再充入H2
(4)一定条件下,反应②中CH4的平衡转化率与温度的关系如图所示。

则△H2_______ 0(填“<”、“>”或“=”),在T ℃ 时的10L 密闭容器中,充入2 mol CH4和 3mol H2O(g)发生反应②,经过 5 min 达到平衡,此时 CH4的转化率为50%,则从开始到平衡,H2的平均反应速率为____________ 。若向此10L 密闭容器中,加入2molCH4、5molH2O(g)、2molCO、和3mol H2发生反应②,若温度仍为T ℃,此时V(正)_____ V(逆)(填“<”、“>”或“=”)。
(5)若某温度下,将 2mol CH4(g) 和2mol H2O(g) 加入压强为200 kPa 的恒压密闭容器中发生反应②,正反应速率 V正 = K 正 × P(CH4) × P(H2O), 逆反应速率V逆 = K逆×P(CO)×P3(H2),P 为分压(分压=总压x 物质的量分数),则该反应的压强平衡常数KP =_____________ ( 以K正、K逆表示)。若 K正 = 4.4×104 kPa-1· s-1,当CH4消耗20% 时,V正=___________ kPa-1· s-1 (保留两位有效数字)
① CO2(g)+3H2(g) = CH3OH(l)+ H2O(l) ΔH1=-184.0 kJ/mol
② 2H2 (g)+ O2(g) = 2H2O(l) ΔH2=-572.0 kJ/mol
(1)则表示CH3OH(l)燃烧热的热化学方程式
在恒温恒容的密闭容器中,工业上常用反应①:CO(g)+2H2(g)⇌CH3OH(g) ΔH1<0 制备甲醇;其中的原料气常用反应②:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH2 来制备。根据题意完成下列各题:
(2)判断反应①达到平衡状态的标志是
a.容器中气体的压强不变 b.CO 和CH3OH 浓度相等
c.V 消耗(CH3OH)= V 生成(CO) d.容器中混合气体的密度保持不变
e.混合气体的平均相对分子质量不发生变化
(3)欲提高反应①中CO 的转化率,下列措施可行的是
a. 减小容器容积 b.升高温度
c.向装置中再充入He d.向装置中再充入H2
(4)一定条件下,反应②中CH4的平衡转化率与温度的关系如图所示。

则△H2
(5)若某温度下,将 2mol CH4(g) 和2mol H2O(g) 加入压强为200 kPa 的恒压密闭容器中发生反应②,正反应速率 V正 = K 正 × P(CH4) × P(H2O), 逆反应速率V逆 = K逆×P(CO)×P3(H2),P 为分压(分压=总压x 物质的量分数),则该反应的压强平衡常数KP =
您最近一年使用:0次
2021-05-22更新
|
475次组卷
|
2卷引用:四川省达州市大竹中学2020-2021学年高二下学期3月月考化学试题
解题方法
2 . 减少二氧化碳的排放、捕集利用二氧化碳是我国能源领域的一个重要战略方向。
(1)以金属钌作催化剂可以从空气中捕获CO2直接转化为甲醇,其转化如图所示。

如图所示转化中,由第1步至第4步生成1molCH3OH(l)的反应热(ΔH)依次是akJ·mol-1、bkJ·mol-1、ckJ·mol-1、dkJ·mol-1,则该转化总反应的热化学方程式是_______ 。
(2)工业上用CO2和H2反应合成甲醚:2CO2(g)+6H2(g)= CH3OCH3(g)+3H2O(g) ΔH<0。
①向一绝热恒容密闭容器中,加入2molCO2和5molH2发生上述反应,能够说明该反应达到平衡状态的是_______ (填字母)。
a.2υ(CO2)=υ(CH3OCH3) b.容器内气体密度保持不变
c.容器内温度保持不变 d.容器内 比值保持不变
比值保持不变
②在催化剂存在的恒容密闭容器里,保持CO2、H2初始加入量不变,测得在不同温度下,反应相同的时间,容器内H2的物质的量与温度的关系如图1所示。氢气的物质的量在温度高于800K后增大的可能原因是_______ (写出一条即可)。

(3)一定条件下,CO2与NH3可合成尿素[CO(NH2)2]:2NH3(g)+CO2(g)= CO(NH2)2(g)+H2O(g)。某温度下,在容积为1L的恒容密闭容器中,按不同氨碳比加入总量为3mol的CO2和NH3混合气体发生反应。反应达到平衡时有关量随氨碳比的变化曲线如图2所示。其中,c表示尿素在平衡体系中的体积百分比。
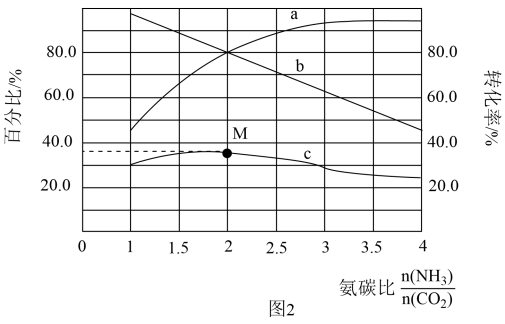
①表示NH3转化率的曲线是_______ (填“a”或“b”);
②M点对应的百分比y=_______ (保留三位有效数字)。
(4)科研人员通过电解酸化的CO2制备CH3OCH3,装置如图所示。
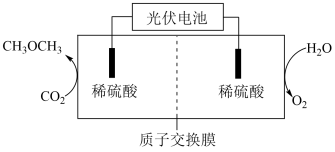
电解过程中,阴极的电极反应式为_______ ,产生1molO2时,通过质子交换膜的质子的物质的量为_______ 。
(1)以金属钌作催化剂可以从空气中捕获CO2直接转化为甲醇,其转化如图所示。

如图所示转化中,由第1步至第4步生成1molCH3OH(l)的反应热(ΔH)依次是akJ·mol-1、bkJ·mol-1、ckJ·mol-1、dkJ·mol-1,则该转化总反应的热化学方程式是
(2)工业上用CO2和H2反应合成甲醚:2CO2(g)+6H2(g)= CH3OCH3(g)+3H2O(g) ΔH<0。
①向一绝热恒容密闭容器中,加入2molCO2和5molH2发生上述反应,能够说明该反应达到平衡状态的是
a.2υ(CO2)=υ(CH3OCH3) b.容器内气体密度保持不变
c.容器内温度保持不变 d.容器内
 比值保持不变
比值保持不变②在催化剂存在的恒容密闭容器里,保持CO2、H2初始加入量不变,测得在不同温度下,反应相同的时间,容器内H2的物质的量与温度的关系如图1所示。氢气的物质的量在温度高于800K后增大的可能原因是

(3)一定条件下,CO2与NH3可合成尿素[CO(NH2)2]:2NH3(g)+CO2(g)= CO(NH2)2(g)+H2O(g)。某温度下,在容积为1L的恒容密闭容器中,按不同氨碳比加入总量为3mol的CO2和NH3混合气体发生反应。反应达到平衡时有关量随氨碳比的变化曲线如图2所示。其中,c表示尿素在平衡体系中的体积百分比。

①表示NH3转化率的曲线是
②M点对应的百分比y=
(4)科研人员通过电解酸化的CO2制备CH3OCH3,装置如图所示。

电解过程中,阴极的电极反应式为
您最近一年使用:0次
3 . 含氮化合物广泛存在于自然界,是一类常见的化合物。
(1)汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应: ,是导致汽车尾气中含有NO的原因之一,已知CO可以催化还原NO以达到消除污染的目的。
,是导致汽车尾气中含有NO的原因之一,已知CO可以催化还原NO以达到消除污染的目的。

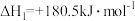
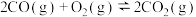
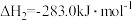
写出CO与NO反应的热化学方程式:___________ ,该反应在___________ (填“高温”或“低温”)条件下可自发进行。
(2)已知工业上常利用NO和Cl2反应来制备有机合成中的重要试剂亚硝酰氯(NOCl),化学方程式为 。该反应的正反应速率方程表达式为v=k正cm(NO)cn(Cl2),其中k正为速率常数,只与温度有关。根据下列数据推断m=
。该反应的正反应速率方程表达式为v=k正cm(NO)cn(Cl2),其中k正为速率常数,只与温度有关。根据下列数据推断m=_______ ,k正的数值为________ 。
(3)尿素是一种重要的化工原料,工业上可用氨和二氧化碳来合成尿素: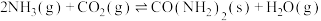
 。一定条件下,向10 L恒容密闭容器中充入2 mol NH3和1 mol CO2,5 min后达到平衡状态,测得CO2和H2O(g)的体积分数之比为2∶3。回答下列问题:
。一定条件下,向10 L恒容密闭容器中充入2 mol NH3和1 mol CO2,5 min后达到平衡状态,测得CO2和H2O(g)的体积分数之比为2∶3。回答下列问题:
①该反应的反应速率v(NH3)=___________ 。
②下列说法中,可以说明该反应已经达到平衡状态的有___________ (填序号)。
A.NH3和CO2的浓度之比为2∶1
B.
C.气体的密度不变
D.容器内总压强不变
③达到平衡后,再向容器中充入1 mol H2O (g),则达到新平衡时,CO2的体积分数___________ (填“增大”“减小”或“不变”)
(4)N2O5是一种新型绿色硝化剂,其制备可以采用电解法。图甲是NaBH4燃料电池,图乙是电解制备N2O5装置。已知电解时电极a与电极d相连,电极c的反应式为___________ 。若制得10.8 g N2O5,则消耗NaBH4的质量为___________ g。

(1)汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应:
 ,是导致汽车尾气中含有NO的原因之一,已知CO可以催化还原NO以达到消除污染的目的。
,是导致汽车尾气中含有NO的原因之一,已知CO可以催化还原NO以达到消除污染的目的。
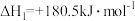
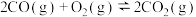
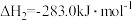
写出CO与NO反应的热化学方程式:
(2)已知工业上常利用NO和Cl2反应来制备有机合成中的重要试剂亚硝酰氯(NOCl),化学方程式为
 。该反应的正反应速率方程表达式为v=k正cm(NO)cn(Cl2),其中k正为速率常数,只与温度有关。根据下列数据推断m=
。该反应的正反应速率方程表达式为v=k正cm(NO)cn(Cl2),其中k正为速率常数,只与温度有关。根据下列数据推断m=| c(NO) | 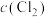 | 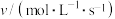 |
| 0.50 | 0.50 | 1.14 |
| 1.00 | 0.50 | 4.56 |
| 1.00 | 1.00 | 9.12 |
(3)尿素是一种重要的化工原料,工业上可用氨和二氧化碳来合成尿素:
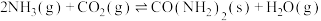
 。一定条件下,向10 L恒容密闭容器中充入2 mol NH3和1 mol CO2,5 min后达到平衡状态,测得CO2和H2O(g)的体积分数之比为2∶3。回答下列问题:
。一定条件下,向10 L恒容密闭容器中充入2 mol NH3和1 mol CO2,5 min后达到平衡状态,测得CO2和H2O(g)的体积分数之比为2∶3。回答下列问题:①该反应的反应速率v(NH3)=
②下列说法中,可以说明该反应已经达到平衡状态的有
A.NH3和CO2的浓度之比为2∶1
B.

C.气体的密度不变
D.容器内总压强不变
③达到平衡后,再向容器中充入1 mol H2O (g),则达到新平衡时,CO2的体积分数
(4)N2O5是一种新型绿色硝化剂,其制备可以采用电解法。图甲是NaBH4燃料电池,图乙是电解制备N2O5装置。已知电解时电极a与电极d相连,电极c的反应式为

您最近一年使用:0次
4 . 二甲醚(DME)(CH3OCH3)被誉为“21 世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
①CO(g) + 2H2(g)⇌CH3OH(g) △H1= -90.7kJ·mol-1
②2CH3OH(g)⇌CH3OCH3(g) + H2O △H2= -23.5kJ·mol-1
③CO(g) + H2O(g)⇌CO2 (g)+H2(g) △H3= -41.2kJ·mol-1
回答下列问题:
(1)则反应 3H2(g)+3CO(g)⇌CH3OCH3(g)+CO2 (g) △H=_______ kJ/mol。
(2)以下说法能说明反应 3H2(g) + 3CO(g)⇌CH3OCH3(g) +CO2 (g)达到平衡状态的有_______ 。
A.H2 和 CO2 的浓度之比为 3︰1
B.单位时间内断裂 3 个 H—H 同时断裂 1 个 C=O
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(3)如图所示装置,装置 A 是二甲醚燃料电池,已知该装置工作时电子从 b 极流出,a 极流入。

①A池中a电极反应式为_______ 。
②当装置A中消耗0.25mol二甲醚时,此时转移的电子的物质的量为_______ ;装置A中溶液的pH会_______ (填写“增大”“减小”或“不变”)。
(4)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(S)+CO2(g)⇌2CO(g)平衡时,体系中气体体积分数与温度的关系如图所示:

①该反应ΔH_______ (填“>”“<”或“=”)0,550℃时,平衡后若充入惰性气体,平衡_______ (填“正移”“逆移”或“不移动”)。
②650℃时,反应达平衡后CO2的转化率为_______ 。
①CO(g) + 2H2(g)⇌CH3OH(g) △H1= -90.7kJ·mol-1
②2CH3OH(g)⇌CH3OCH3(g) + H2O △H2= -23.5kJ·mol-1
③CO(g) + H2O(g)⇌CO2 (g)+H2(g) △H3= -41.2kJ·mol-1
回答下列问题:
(1)则反应 3H2(g)+3CO(g)⇌CH3OCH3(g)+CO2 (g) △H=
(2)以下说法能说明反应 3H2(g) + 3CO(g)⇌CH3OCH3(g) +CO2 (g)达到平衡状态的有
A.H2 和 CO2 的浓度之比为 3︰1
B.单位时间内断裂 3 个 H—H 同时断裂 1 个 C=O
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(3)如图所示装置,装置 A 是二甲醚燃料电池,已知该装置工作时电子从 b 极流出,a 极流入。

①A池中a电极反应式为
②当装置A中消耗0.25mol二甲醚时,此时转移的电子的物质的量为
(4)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(S)+CO2(g)⇌2CO(g)平衡时,体系中气体体积分数与温度的关系如图所示:

①该反应ΔH
②650℃时,反应达平衡后CO2的转化率为
您最近一年使用:0次
20-21高一下·浙江·阶段练习
5 . 实验室利用下列装置模拟工业生产制备少量硝酸。

(1)B中反应的化学方程式为___ ,NaOH溶液的作用是___ 。
(2)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,之后催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是____ (填选项)



(3)高温时,2NO2(g) 2NO(g)+O2(g),因此氨气与氧气反应难以生成NO2。根据下列数据计算,当2molNO2分解时,反应会
2NO(g)+O2(g),因此氨气与氧气反应难以生成NO2。根据下列数据计算,当2molNO2分解时,反应会____ (填“吸收”或“放出”)____ kJ能量。
NO2(g)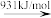 N(g)+2O(g)
N(g)+2O(g)
NO(g)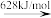 N(g)+O(g)
N(g)+O(g)
O2(g)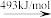 2O(g)
2O(g)
(4)在恒容绝热容器内发生反应2NO2(g) 2NO(g)+O2(g),下列能说明已达平衡的是
2NO(g)+O2(g),下列能说明已达平衡的是___ 。
a.单位时间内,每生成一定物质的量浓度的NO,同时有相同物质的量浓度的O2生成
b.2v正(NO2)=v逆(O2)
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气的密度不再改变

(1)B中反应的化学方程式为
(2)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,之后催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是



(3)高温时,2NO2(g)
 2NO(g)+O2(g),因此氨气与氧气反应难以生成NO2。根据下列数据计算,当2molNO2分解时,反应会
2NO(g)+O2(g),因此氨气与氧气反应难以生成NO2。根据下列数据计算,当2molNO2分解时,反应会NO2(g)
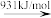 N(g)+2O(g)
N(g)+2O(g)NO(g)
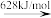 N(g)+O(g)
N(g)+O(g)O2(g)
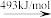 2O(g)
2O(g)(4)在恒容绝热容器内发生反应2NO2(g)
 2NO(g)+O2(g),下列能说明已达平衡的是
2NO(g)+O2(g),下列能说明已达平衡的是a.单位时间内,每生成一定物质的量浓度的NO,同时有相同物质的量浓度的O2生成
b.2v正(NO2)=v逆(O2)
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气的密度不再改变
您最近一年使用:0次
6 . 减少二氧化碳的排放、捕集利用二氧化碳是我国能源领域的一个重要战略方向。
(1)科学家研究利用回收的CO2制取甲醛(HCHO),已知:
①HCHO(g)+O2(g)=CO2(g)+H2O(g)∆H1=-480kJ/mol
②2H2(g)+O2(g)=2H2O(g)∆H2=-486kJ/mol
则由CO2和H2合成甲醛的热化学方程式为:___ 。
(2)工业上用CO2和H2反应合成甲醚:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)∆H<0。
CH3OCH3(g)+3H2O(g)∆H<0。
①向一绝热恒容密闭容器中,加入2molCO2和5molH2发生上述反应,能够说明该反应达到平衡状态的是___ (填字母)
a.2v正(CO2)=v逆(CH3OCH3) b.容器内气体密度保持不变
c.容器内温度保持不变 d.容器内 比值保持不变
比值保持不变
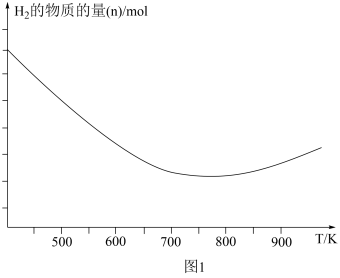
②在催化剂存在的恒容密闭容器里,保持CO2、H2初始加入量不变,测得在不同温度下,反应相同的时间,容器内H2的物质的量与温度的关系如图1所示,氢气的物质的量在温度高于800K后增大的可能原因是___ 、___ 。
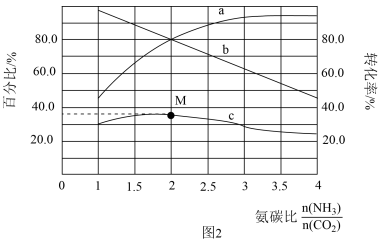
(3)一定条件下,CO2与NH3可合成尿素[CO(NH)2]2:2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(g)。某温度下,在容积为1L的恒容密闭容器中,按不同氨碳比加入总量为3mol的CO2和NH3混合气体发生反应。反应达到平衡时有关量随氨碳比的变化曲线如图2所示。其中,c表示尿素在平衡体系中的体积百分比。
CO(NH2)2(g)+H2O(g)。某温度下,在容积为1L的恒容密闭容器中,按不同氨碳比加入总量为3mol的CO2和NH3混合气体发生反应。反应达到平衡时有关量随氨碳比的变化曲线如图2所示。其中,c表示尿素在平衡体系中的体积百分比。
①表示NH3转化率的曲线是___ (填“a”或“b”);
②M点对应的百分比y=___ (保留三位有效数字)。
(4)科研人员通过电解酸化的CO2制备CH3OCH3,装置如图所示。
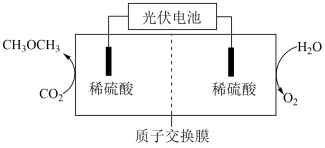
电解过程中,阴极的电极反应式为___ ,产生lmolO2时,通过质子交换膜的质子的物质的量为___ 。
(1)科学家研究利用回收的CO2制取甲醛(HCHO),已知:
①HCHO(g)+O2(g)=CO2(g)+H2O(g)∆H1=-480kJ/mol
②2H2(g)+O2(g)=2H2O(g)∆H2=-486kJ/mol
则由CO2和H2合成甲醛的热化学方程式为:
(2)工业上用CO2和H2反应合成甲醚:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)∆H<0。
CH3OCH3(g)+3H2O(g)∆H<0。①向一绝热恒容密闭容器中,加入2molCO2和5molH2发生上述反应,能够说明该反应达到平衡状态的是
a.2v正(CO2)=v逆(CH3OCH3) b.容器内气体密度保持不变
c.容器内温度保持不变 d.容器内
 比值保持不变
比值保持不变②在催化剂存在的恒容密闭容器里,保持CO2、H2初始加入量不变,测得在不同温度下,反应相同的时间,容器内H2的物质的量与温度的关系如图1所示,氢气的物质的量在温度高于800K后增大的可能原因是


(3)一定条件下,CO2与NH3可合成尿素[CO(NH)2]2:2NH3(g)+CO2(g)
 CO(NH2)2(g)+H2O(g)。某温度下,在容积为1L的恒容密闭容器中,按不同氨碳比加入总量为3mol的CO2和NH3混合气体发生反应。反应达到平衡时有关量随氨碳比的变化曲线如图2所示。其中,c表示尿素在平衡体系中的体积百分比。
CO(NH2)2(g)+H2O(g)。某温度下,在容积为1L的恒容密闭容器中,按不同氨碳比加入总量为3mol的CO2和NH3混合气体发生反应。反应达到平衡时有关量随氨碳比的变化曲线如图2所示。其中,c表示尿素在平衡体系中的体积百分比。①表示NH3转化率的曲线是
②M点对应的百分比y=
(4)科研人员通过电解酸化的CO2制备CH3OCH3,装置如图所示。

电解过程中,阴极的电极反应式为
您最近一年使用:0次
7 . 回答下列问题:
I.铅蓄电池是最常用的二次电池,电池总反应式为: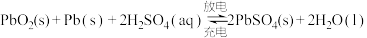
(1)放电时,铅蓄电池的负极反应式是_______ 。
(2)充电时,PbSO4(s)_______ (填序号)。
A.在阳极生成 B.在阴极生成 C.在两个电极上除去 D.在两个电极上生成
(3)用铅蓄电池作电源,以惰性电极电解浓的Na2SO4溶液制备烧碱和硫酸,装置如图所示,其中a、b为离子交换膜。
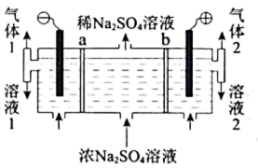
①a为_______ 离子交换膜(填“阴”或“阳”)。
②溶液1是_______ 。
③当铅蓄电池内消耗2 mol H2SO4时,理论上产生气体2的体积是_______ L(标准状况)。
II.一定温度下,在体积为1L的密闭容器中,充入1 mol CO2和3 mol H2,发生反应: ,测得CO2和CH3OH的浓度随时间变化如下图。
,测得CO2和CH3OH的浓度随时间变化如下图。
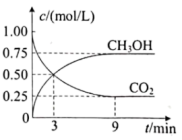
(4)反应从开始至达到平衡时,H2的平均反应速率是_______ 。
(5)平衡时CO2的转化率为_______ 。
(6)第9分钟时v逆(CH3OH)_______ (填“>”“<"或“=”)第3分钟时v正(CH3OH)。
(7)能说明上述反应达到平衡状态的是_______ (填编号)。
A.CO2与CH3OH的物质的量浓度相等
B.混合气体的密度不随时间的变化而变化
C.CO2在混合气体中的体积分数保持不变
D.单位时间内消耗3mol H2,同时生成1mol H2O
(8)为加快该反应速率,可采取的措施是_______ (填编号)。
A.恒容时充入Ne B.适当升高温度 C.增大容器的体积 D.选择高效催化剂
I.铅蓄电池是最常用的二次电池,电池总反应式为:
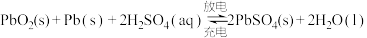
(1)放电时,铅蓄电池的负极反应式是
(2)充电时,PbSO4(s)
A.在阳极生成 B.在阴极生成 C.在两个电极上除去 D.在两个电极上生成
(3)用铅蓄电池作电源,以惰性电极电解浓的Na2SO4溶液制备烧碱和硫酸,装置如图所示,其中a、b为离子交换膜。

①a为
②溶液1是
③当铅蓄电池内消耗2 mol H2SO4时,理论上产生气体2的体积是
II.一定温度下,在体积为1L的密闭容器中,充入1 mol CO2和3 mol H2,发生反应:
 ,测得CO2和CH3OH的浓度随时间变化如下图。
,测得CO2和CH3OH的浓度随时间变化如下图。
(4)反应从开始至达到平衡时,H2的平均反应速率是
(5)平衡时CO2的转化率为
(6)第9分钟时v逆(CH3OH)
(7)能说明上述反应达到平衡状态的是
A.CO2与CH3OH的物质的量浓度相等
B.混合气体的密度不随时间的变化而变化
C.CO2在混合气体中的体积分数保持不变
D.单位时间内消耗3mol H2,同时生成1mol H2O
(8)为加快该反应速率,可采取的措施是
A.恒容时充入Ne B.适当升高温度 C.增大容器的体积 D.选择高效催化剂
您最近一年使用:0次



