名校
1 . 下列叙述中,不能用平衡移动原理解释的是
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B.高压比常压有利于合成SO3的反应 |
| C.工业合成氨时采用500℃的高温(已知该反应ΔH<0) |
| D.Fe(SCN)3溶液中加入铁粉后颜色变浅 |
您最近一年使用:0次
解题方法
2 . 在一定温度下的密闭容器中发生反应: ,平衡时测得A的浓度为
,平衡时测得A的浓度为 ,保持温度不变,将容器的容积缩小到原来的一半,再达到平衡时,测得A的浓度为
,保持温度不变,将容器的容积缩小到原来的一半,再达到平衡时,测得A的浓度为 。下列判断正确的是
。下列判断正确的是
 ,平衡时测得A的浓度为
,平衡时测得A的浓度为 ,保持温度不变,将容器的容积缩小到原来的一半,再达到平衡时,测得A的浓度为
,保持温度不变,将容器的容积缩小到原来的一半,再达到平衡时,测得A的浓度为 。下列判断正确的是
。下列判断正确的是A.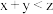 | B.平衡向逆反应方向移动 |
| C.B的转化率降低 | D.C的物质的量分数增大 |
您最近一年使用:0次
名校
3 . 下列叙述及解释正确的是
A. ,在达到平衡后,保持压强不变,充入O2,平衡向左移动 ,在达到平衡后,保持压强不变,充入O2,平衡向左移动 |
B. ,在达到平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 ,在达到平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 |
C. ,在达到平衡后,加入碳,平衡向正反应方向移动 ,在达到平衡后,加入碳,平衡向正反应方向移动 |
D. ∆H<0,在达到平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 ∆H<0,在达到平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 |
您最近一年使用:0次
2023-08-25更新
|
439次组卷
|
2卷引用:贵州省黔西南布依族苗族自治州兴义第一中学2022-2023学年高一下学期第三次月考化学试题
4 . 将少量 固体溶于浓盐酸中,然后加水至溶液呈黄绿色,溶液中存在平衡:
固体溶于浓盐酸中,然后加水至溶液呈黄绿色,溶液中存在平衡: (蓝色)
(蓝色)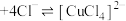 (黄色)
(黄色)
 ,下列说法正确的是
,下列说法正确的是
 固体溶于浓盐酸中,然后加水至溶液呈黄绿色,溶液中存在平衡:
固体溶于浓盐酸中,然后加水至溶液呈黄绿色,溶液中存在平衡: (蓝色)
(蓝色)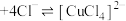 (黄色)
(黄色)
 ,下列说法正确的是
,下列说法正确的是A.向该溶液中加入足量 固体,溶液变为蓝色,且有白色沉淀生成 固体,溶液变为蓝色,且有白色沉淀生成 |
| B.向该溶液中加入足量NaCl固体,溶液变为蓝色 |
| C.向该溶液中再加入适量蒸馏水,溶液变为黄色 |
| D.若对该溶液适当升高温度,则溶液变为蓝色 |
您最近一年使用:0次
名校
5 . 现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_______ 热反应,且m+n ______ p (填“>”、“<”或“=”)。
(2)减压时,A 的质量分数_______ (填“增大”、“减小”或“不变”,下同)。
(3)若加入 B(体积不变),则A的转化率__________ 。
(4)若升高温度,则平衡时B、C的浓度之比[B]/[C]将_______ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量_______ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应的逆反应为
(2)减压时,A 的质量分数
(3)若加入 B(体积不变),则A的转化率
(4)若升高温度,则平衡时B、C的浓度之比[B]/[C]将
(5)若加入催化剂,平衡时气体混合物的总物质的量
您最近一年使用:0次
2023-02-07更新
|
247次组卷
|
7卷引用:贵州省贵阳市清镇养正学校2019-2020学年高二上学期期中考试化学试题
解题方法
6 . 碳捕集与碳封存技术有望成为碳减排的关键,其中碳捕集技术是指从空气中捕获二氧化碳的各种科学技术的统称。
(1)工业上用 捕碳可合成
捕碳可合成 :
:
已知:①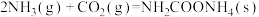
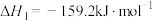
②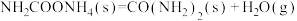
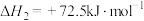 。
。
则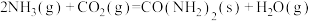

_______  。
。
(2)现将0.08mol纯净的氨基甲酸铵置于2L恒容密闭容器中,分别在不同温度下进行反应: 。实验测得的有关数据见下表(
。实验测得的有关数据见下表(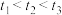 )
)
氨基甲酸铵分解反应是_______ (填“放热”或“吸热”)反应,15℃达平衡时,氨基甲酸铵的转化率为_______ ,化学平衡常数
_______ 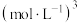 。
。
(3)用 捕碳的反应为:
捕碳的反应为: 。为研究温度对
。为研究温度对 捕获
捕获 效率的影响,将一定量的
效率的影响,将一定量的 溶液置于密闭容器中,并充入一定量的
溶液置于密闭容器中,并充入一定量的 气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得
气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得 气体浓度,得到趋势图:
气体浓度,得到趋势图:

①b、c、d三点的平衡常数 、
、 、
、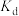 从大到小的顺序为
从大到小的顺序为_______ 。
②在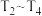 温度区间,容器内
温度区间,容器内 气体浓度呈现先减小后增大的变化趋势,其原因是
气体浓度呈现先减小后增大的变化趋势,其原因是_______ 。
(1)工业上用
 捕碳可合成
捕碳可合成 :
:已知:①
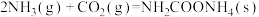
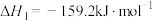
②
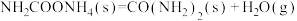
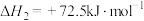 。
。则
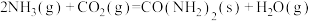

 。
。(2)现将0.08mol纯净的氨基甲酸铵置于2L恒容密闭容器中,分别在不同温度下进行反应:
 。实验测得的有关数据见下表(
。实验测得的有关数据见下表(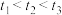 )
)温度/℃ 气体总浓度/ 时间/min | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
 | 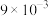 | 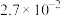 | 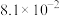 |
 | 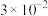 |  |  |
 | 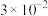 |  |  |

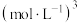 。
。(3)用
 捕碳的反应为:
捕碳的反应为: 。为研究温度对
。为研究温度对 捕获
捕获 效率的影响,将一定量的
效率的影响,将一定量的 溶液置于密闭容器中,并充入一定量的
溶液置于密闭容器中,并充入一定量的 气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得
气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得 气体浓度,得到趋势图:
气体浓度,得到趋势图:
①b、c、d三点的平衡常数
 、
、 、
、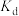 从大到小的顺序为
从大到小的顺序为②在
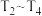 温度区间,容器内
温度区间,容器内 气体浓度呈现先减小后增大的变化趋势,其原因是
气体浓度呈现先减小后增大的变化趋势,其原因是
您最近一年使用:0次
解题方法
7 . 在一定条件下,反应x A+yB zC达到平衡:
zC达到平衡:
(1)若A、B、C均为气体,减压后平衡向逆反应方向移动,则x、y、z间的关系是_______ ;
(2)若已知C是气体,且x+y=z。在增大压强时,若平衡发生移动,则一定向______ (填“正”或“逆”)反应方向移动;
(3)已知B、C是气体,当其他条件不变时,增大A的物质的量,平衡不移动,则A为____ 态;
(4)加热后C的质量分数减少,则正反应是________ (填“放热”或“吸热”)反应。升高温度达到新的平衡后,该反应的平衡常数将变___ (填“大”或“小”)。
 zC达到平衡:
zC达到平衡:(1)若A、B、C均为气体,减压后平衡向逆反应方向移动,则x、y、z间的关系是
(2)若已知C是气体,且x+y=z。在增大压强时,若平衡发生移动,则一定向
(3)已知B、C是气体,当其他条件不变时,增大A的物质的量,平衡不移动,则A为
(4)加热后C的质量分数减少,则正反应是
您最近一年使用:0次
2022-12-05更新
|
48次组卷
|
2卷引用:贵州省金沙县精诚中学2021-2022学年高二上学期期中理综化学试题
解题方法
8 . 在密闭容器中发生如下反应: 。反应达平㣏后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的浓度为原平衡时的1.8倍。下列叙述正确的是
。反应达平㣏后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的浓度为原平衡时的1.8倍。下列叙述正确的是
 。反应达平㣏后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的浓度为原平衡时的1.8倍。下列叙述正确的是
。反应达平㣏后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的浓度为原平衡时的1.8倍。下列叙述正确的是A. | B.W的体积分数增大 |
| C.平衡向正反应方向移动 | D.Y的转化率下降 |
您最近一年使用:0次
2022-11-27更新
|
201次组卷
|
3卷引用:贵州省部分学校2022-2023学年高二上学期10月联考化学试题
解题方法
9 . 下列事实中,能用勒夏特列原理解释的是
| A.夏天,打开啤酒瓶时会从瓶口逸出气体 |
| B.制取氢气时,用粗锌产生气泡的速率比用纯锌快 |
| C.压缩氢气与碘蒸气的平衡混合体系,气体颜色变深 |
D.减小压强有利于 和 和 反应生成 反应生成 |
您最近一年使用:0次
2022-11-27更新
|
98次组卷
|
2卷引用:贵州省部分学校2022-2023学年高二上学期10月联考化学试题
名校
10 . 在一定条件下,反应 达到平衡后,改变条件,正、逆反应速率随时间的变化如图,下列说法正确的是
达到平衡后,改变条件,正、逆反应速率随时间的变化如图,下列说法正确的是
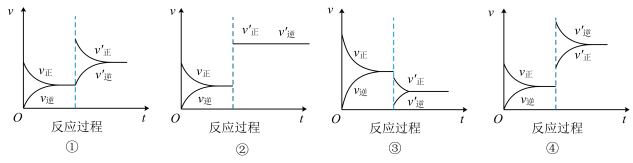
 达到平衡后,改变条件,正、逆反应速率随时间的变化如图,下列说法正确的是
达到平衡后,改变条件,正、逆反应速率随时间的变化如图,下列说法正确的是
| A.图①改变的条件可能是增大A的浓度,达到新平衡后A的转化率增大 |
| B.图②改变的条件是加压,达到新平衡后A的转化率不变 |
| C.图③改变的条件可能是减小A的浓度,达到新平衡后A的转化率减小 |
| D.图④改变的条件是升温,达到新平衡后A的转化率减小 |
您最近一年使用:0次
2022-11-13更新
|
430次组卷
|
4卷引用:贵州省部分学校2022-2023学年高二上学期期中联合考试化学试题
贵州省部分学校2022-2023学年高二上学期期中联合考试化学试题新疆维吾尔自治区新疆生产建设兵团部分名校2022-2023学年高二上学期期中联考化学试题安徽省合肥庐巢八校2022-2023学年高二上学期12月联考化学试题(已下线)第06讲 化学反应速率与化学平衡的图像-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)




