名校
解题方法
1 . 在恒容绝热的容器中进行反应:2X(g)+Y(g) 3Z(g)+Q(s) ΔH<0,下列说法正确的是
3Z(g)+Q(s) ΔH<0,下列说法正确的是
 3Z(g)+Q(s) ΔH<0,下列说法正确的是
3Z(g)+Q(s) ΔH<0,下列说法正确的是| A.容器中压强不变,表明反应达到平衡状态 |
| B.反应过程中X、Y的转化率一定不同 |
| C.增大X的浓度,平衡时Y的体积分数增大 |
| D.容器中温度不变,表明反应达到平衡状态 |
您最近一年使用:0次
2023-01-03更新
|
139次组卷
|
2卷引用:内蒙古乌兰浩特市第四中学2022-2023学年高二上学期第三次月考化学试题
2 . 下列说法错误的是
| A.化学平衡常数改变,化学平衡一定发生移动 |
B.恒温恒容条件下,反应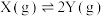 达平衡后再充入 达平衡后再充入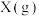 ,平衡向正反应方向移动 ,平衡向正反应方向移动 |
C.25℃时某容器中发生: ,当各组分物质的量不再变化时,达到化学平衡状态 ,当各组分物质的量不再变化时,达到化学平衡状态 |
D.实际生产中,反应 的条件为400~500℃、常压、合适的催化剂 的条件为400~500℃、常压、合适的催化剂 |
您最近一年使用:0次
名校
解题方法
3 . 由合成气(CO和H2)通过如下反应可制得甲醇:2H2(g)+CO(g) CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
 CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是| A.反应的ΔS>0 |
| B.当容器中气体密度不再发生变化时,反应达到平衡 |
| C.温度为400K时,反应的平衡常数K=2500 |
| D.其他条件不变,若起始时向容器中充入0.008molH2、0.004molCO和0.016molCH3OH,此时v(正)>v(逆) |
您最近一年使用:0次
2022-09-23更新
|
297次组卷
|
2卷引用:江苏省如皋中学2022-2023学年高三上学期8月综合测试化学试题
解题方法
4 . 下列实验操作、现象及结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下,用pH试纸分别测定浓度均为0.1mol·L-1CH3COONa和NaClO溶液的pH | 测得CH3COONa和NaClO溶液的pH分别为9和11 | 酸性:CH3COOH>HClO |
| B | 常温下,向0.1mol·L-1的Na2C2O4溶液中滴加等体积的0.1mol·L-1HCl的溶液 | 测得pH约为5.5 | c(C2O )>c(H2C2O4) )>c(H2C2O4) |
| C | 向FeCl3和KSCN混合溶液中,加入少量的KCl固体 | 溶液颜色变浅 | FeCl3+KSCN KCl+Fe(SCN)3平衡向逆反应方向移动 KCl+Fe(SCN)3平衡向逆反应方向移动 |
| D | 向2mL0.1mol·L-1MgCl2溶液中滴入3滴2mol·L-1的NaOH溶液,再滴入4滴0.1mol·L-1FeCl3溶液 | 先产生白色沉淀后,后产生红褐色沉淀 | 同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 湿法烟气脱氮工艺中常用到尿素,其反应原理为 ,反应达到平衡后仅改变某一条件,反应速率v与时间t的关系如图所示,下列说法错误的是
,反应达到平衡后仅改变某一条件,反应速率v与时间t的关系如图所示,下列说法错误的是

 ,反应达到平衡后仅改变某一条件,反应速率v与时间t的关系如图所示,下列说法错误的是
,反应达到平衡后仅改变某一条件,反应速率v与时间t的关系如图所示,下列说法错误的是
| A.t2时刻,改变的某一条件可能是充入少量的N2 |
| B.t4时刻,改变的某一条件可能是增大压强 |
| C.t6时刻,改变的某一条件可能是加入合适的催化剂 |
D.反应达到平衡的各时间段内, 时间段内 时间段内 的含量最低 的含量最低 |
您最近一年使用:0次
2021-11-21更新
|
249次组卷
|
3卷引用:湖南省株洲南方中学2022-2023学年高二上学期期中考试化学试题
名校
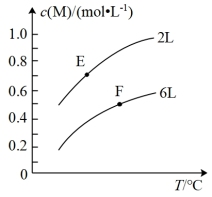
6 . 在一定条件下,取一定量的A和B在恒容密闭容器中发生反应:aA(g)+bB(s) mM(g)+nN(g) △H=QkJ·mol-1,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断一定正确的是
mM(g)+nN(g) △H=QkJ·mol-1,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断一定正确的是
 mM(g)+nN(g) △H=QkJ·mol-1,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断一定正确的是
mM(g)+nN(g) △H=QkJ·mol-1,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断一定正确的是
| A.a>m+n | B.达到平衡后,增大B的量将会提高A的转化率 |
| C.E点的平衡常数小于F点的平衡常数 | D.Q>0 |
您最近一年使用:0次
2021-09-27更新
|
994次组卷
|
8卷引用:押新高考卷09题 速率和平衡-备战2022年高考化学临考题号押题(新高考通版)
名校
7 . 下列事实中,能用勒夏特列原理解释的是
| A.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
| B.对于平衡体系2HI(g)⇌H2(g)+I2(g),增大压强(缩小容积)可使颜色变深 |
| C.反应CO(g)+NO2(g)⇌CO2(g)+NO(g) ΔH<0,达平衡后,升高温度体系颜色变深 |
| D.反应2SO2(g)+O2(g)⇌2SO3(g) △H<0中采取高温高压措施可提高SO3的产量 |
您最近一年使用:0次
2020-12-30更新
|
219次组卷
|
2卷引用:江西省景德镇一中2022-2023学年高二上学期期中考试化学试题(19班)
8 . 在①、②、③容积不等的恒容密闭容器中,均充入0.lmolCO和0.2molH2,在催化剂的作用下发生反应:CO(g)+2H2(g)  CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
下列说法正确的是
 CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示: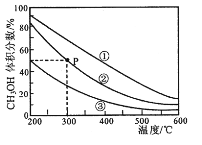
下列说法正确的是
| A.该反应的正反应为放热反应 |
| B.三个容器容积:①>②>③ |
| C.在P点,CO转化率为75% |
| D.在P点,向容器②中再充入CO、H2 及 CH3OH 各 0.025mol,此时 v(CO)正<v (CO)逆 |
您最近一年使用:0次
2017-03-22更新
|
684次组卷
|
5卷引用:湖南省常德市临澧县第一中学2021-2022学年高三第九次阶段性考试化学试题



