名校
解题方法
1 . 汽车尾气是否为导致空气质量问题的主要原因,由此引发的“汽车限行”争议,是当前备受关注的社会性科学议题。
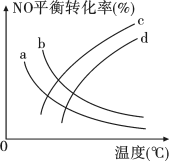
(1)用CO可将汽车尾气中的NO还原为 。探究温度、压强(2MPa、5MPa)对反应
。探究温度、压强(2MPa、5MPa)对反应
 的影响,如图所示,表示2MPa的是反应
的影响,如图所示,表示2MPa的是反应___________ (填字母)。
(2)一定温度下向容积为 的密闭容器中加入
的密闭容器中加入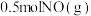 、
、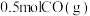 ,此时容器总压为
,此时容器总压为 ,发生反应
,发生反应 ,
, 时反应达到平衡,此时测得
时反应达到平衡,此时测得 的物质的量为
的物质的量为 ,则
,则 内
内
___________ mol∙L-1∙min-1;该反应的 为
为___________ 。[标准平衡常数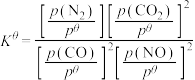 ,其中
,其中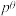 为标准压强(
为标准压强( ),
), 、
、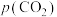 、
、 和
和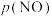 为各组分的平衡分压[已知
为各组分的平衡分压[已知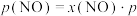 ,其中
,其中 为平衡总压,
为平衡总压, 为平衡系统中
为平衡系统中 的物质的量分数]
的物质的量分数]
(3)用 可催化消除
可催化消除 污染:
污染: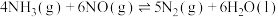
 。该反应速率
。该反应速率 ,
,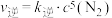 ,该反应的平衡常数
,该反应的平衡常数
___________ (用含 、
、 的式子表示)若将
的式子表示)若将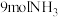 和
和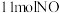 投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下
投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下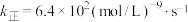 ,平衡时
,平衡时 的转化率为
的转化率为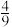 ,
,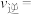
___________  。
。
(4)在恒容、 和
和 的起始浓度一定的条件下,分别以VWTi/AC0、VWTi/AC10、VWTi/AC50、VWTi/AC70为催化剂,发生反应:
的起始浓度一定的条件下,分别以VWTi/AC0、VWTi/AC10、VWTi/AC50、VWTi/AC70为催化剂,发生反应:
 ,相同时间内测得不同温度下
,相同时间内测得不同温度下 转化为
转化为 的转化率如图a所示,温度升高有副产物
的转化率如图a所示,温度升高有副产物 生成,测得不同温度
生成,测得不同温度 的生成量如图b所示。
的生成量如图b所示。
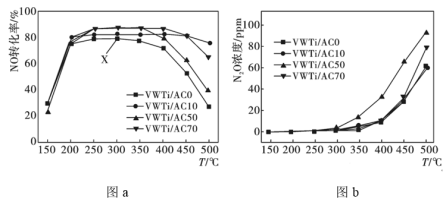
①结合图b分析,VWTi/AC50在 之后NO转化率降低的可能原因是
之后NO转化率降低的可能原因是___________ 。
②图中X点所示条件下,反应向___________ (填“正反应”或“逆反应”)方向移动。
③250℃时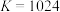 ,若起始时充入
,若起始时充入 ,
,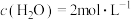 ,则
,则
___________ (填“>”、“<”或“=”) 。
。
(1)用CO可将汽车尾气中的NO还原为
 。探究温度、压强(2MPa、5MPa)对反应
。探究温度、压强(2MPa、5MPa)对反应
 的影响,如图所示,表示2MPa的是反应
的影响,如图所示,表示2MPa的是反应
(2)一定温度下向容积为
 的密闭容器中加入
的密闭容器中加入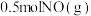 、
、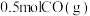 ,此时容器总压为
,此时容器总压为 ,发生反应
,发生反应 ,
, 时反应达到平衡,此时测得
时反应达到平衡,此时测得 的物质的量为
的物质的量为 ,则
,则 内
内
 为
为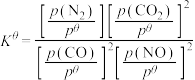 ,其中
,其中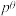 为标准压强(
为标准压强( ),
), 、
、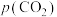 、
、 和
和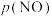 为各组分的平衡分压[已知
为各组分的平衡分压[已知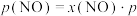 ,其中
,其中 为平衡总压,
为平衡总压, 为平衡系统中
为平衡系统中 的物质的量分数]
的物质的量分数](3)用
 可催化消除
可催化消除 污染:
污染: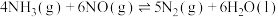
 。该反应速率
。该反应速率 ,
,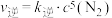 ,该反应的平衡常数
,该反应的平衡常数
 、
、 的式子表示)若将
的式子表示)若将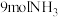 和
和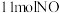 投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下
投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下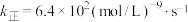 ,平衡时
,平衡时 的转化率为
的转化率为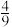 ,
,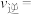
 。
。(4)在恒容、
 和
和 的起始浓度一定的条件下,分别以VWTi/AC0、VWTi/AC10、VWTi/AC50、VWTi/AC70为催化剂,发生反应:
的起始浓度一定的条件下,分别以VWTi/AC0、VWTi/AC10、VWTi/AC50、VWTi/AC70为催化剂,发生反应:
 ,相同时间内测得不同温度下
,相同时间内测得不同温度下 转化为
转化为 的转化率如图a所示,温度升高有副产物
的转化率如图a所示,温度升高有副产物 生成,测得不同温度
生成,测得不同温度 的生成量如图b所示。
的生成量如图b所示。
①结合图b分析,VWTi/AC50在
 之后NO转化率降低的可能原因是
之后NO转化率降低的可能原因是②图中X点所示条件下,反应向
③250℃时
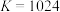 ,若起始时充入
,若起始时充入 ,
,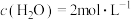 ,则
,则
 。
。
您最近一年使用:0次
名校
解题方法
2 . 在煤化工领域主要涉及碳一化学,即研究以含有一个碳原子的物质(CO、 、
、 、
、 等)为原料合成化工产品或液体燃料。回答下列问题:
等)为原料合成化工产品或液体燃料。回答下列问题:
(1)已知物质之间转化能量关系如图所示: 和
和 生成
生成 和
和 的热化学方程式
的热化学方程式___________ 。
(2)煤化工业上主要利用CO和 反应制备甲醇(
反应制备甲醇( ),反应热化学方程式为
),反应热化学方程式为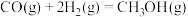
 。已知CO的平衡转化率与温度的关系如图所示:
。已知CO的平衡转化率与温度的关系如图所示:
___________ (填“>”“<”或“=”)0。
②A、B、C三点平衡常数 、
、 、
、 的大小关系为
的大小关系为___________ 。压强
___________ (填“>”“<”或“=”,下同) ,在
,在 和
和 条件下,由D点到B点过程中,正、逆反应速率之间的关系:
条件下,由D点到B点过程中,正、逆反应速率之间的关系:
___________  。
。
③若容器容积不变,则下列措施可提高CO平衡转化率的是___________ (填字母)。
a.充入CO,使体系总压强增大 b.将 从体系中分离
从体系中分离
c.充入He,使体系总压强增大 d.使用高效催化剂
④在2L恒容密闭容器中充入2molCO和 ,在
,在 和
和 条件下经10min达到平衡状态。在该条件下,
条件下经10min达到平衡状态。在该条件下,
___________  ;平衡常数
;平衡常数
___________ (填数值)。
(3)用 还原
还原 可以合成
可以合成 :
:
 。恒压下,
。恒压下, 和
和 的起始物质的量之比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜(能选择性分离出
的起始物质的量之比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜(能选择性分离出 )时甲醇的产率随温度的变化如图所示。P点甲醇产率高于T点的原因为
)时甲醇的产率随温度的变化如图所示。P点甲醇产率高于T点的原因为___________ 。
 、
、 、
、 等)为原料合成化工产品或液体燃料。回答下列问题:
等)为原料合成化工产品或液体燃料。回答下列问题:(1)已知物质之间转化能量关系如图所示:

 和
和 生成
生成 和
和 的热化学方程式
的热化学方程式(2)煤化工业上主要利用CO和
 反应制备甲醇(
反应制备甲醇( ),反应热化学方程式为
),反应热化学方程式为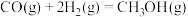
 。已知CO的平衡转化率与温度的关系如图所示:
。已知CO的平衡转化率与温度的关系如图所示: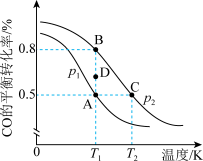

②A、B、C三点平衡常数
 、
、 、
、 的大小关系为
的大小关系为
 ,在
,在 和
和 条件下,由D点到B点过程中,正、逆反应速率之间的关系:
条件下,由D点到B点过程中,正、逆反应速率之间的关系:
 。
。③若容器容积不变,则下列措施可提高CO平衡转化率的是
a.充入CO,使体系总压强增大 b.将
 从体系中分离
从体系中分离c.充入He,使体系总压强增大 d.使用高效催化剂
④在2L恒容密闭容器中充入2molCO和
 ,在
,在 和
和 条件下经10min达到平衡状态。在该条件下,
条件下经10min达到平衡状态。在该条件下,
 ;平衡常数
;平衡常数
(3)用
 还原
还原 可以合成
可以合成 :
:
 。恒压下,
。恒压下, 和
和 的起始物质的量之比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜(能选择性分离出
的起始物质的量之比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜(能选择性分离出 )时甲醇的产率随温度的变化如图所示。P点甲醇产率高于T点的原因为
)时甲醇的产率随温度的变化如图所示。P点甲醇产率高于T点的原因为
您最近一年使用:0次
2024-01-12更新
|
251次组卷
|
2卷引用:安徽省芜湖市第一中学2022-2023学年高二上学期10月月考化学试卷
名校
解题方法
3 . 实验小组制备硫代硫酸钠(Na2S2O3)并探究其性质。
资料:ⅰ.S2O +2H+=S↓+SO2↑+H2O
+2H+=S↓+SO2↑+H2O
ⅱ.Fe3++3S2O
 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)
ⅲ.Ag2S2O3是难溶于水、可溶于Na2S2O3溶液的白色固体。
(1)实验室可利用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制备Na2S2O3,装置如下图。

①用化学用语解释Na2S和Na2CO3的混合溶液呈碱性的原因:S2-+H2O HS-+OH-、
HS-+OH-、___________ 。
②为了保证Na2S2O3的产量,实验中通入的SO2不能过量。要控制SO2的生成速率,可以采取的措施有:___________ (写出一条)。
(2)探究Na2S2O3溶液与不同金属的硫酸盐溶液间反应的多样性。
①Ⅰ中产生白色沉淀的离子方程式为___________ 。
②经检验,现象Ⅱ中的沉淀有Al(OH)3和S,用平衡移动原理解释Ⅱ中的现象:___________ 。
③经检验,现象中的无色溶液中含有Fe2+。从化学反应速率和限度的角度解释Ⅲ中Fe3+与S2O 反应的实验现象:
反应的实验现象:___________ 。
以上实验说明:Na2S2O3溶液与金属阳离子反应的多样性和阳离子的性质有关。
资料:ⅰ.S2O
 +2H+=S↓+SO2↑+H2O
+2H+=S↓+SO2↑+H2O ⅱ.Fe3++3S2O

 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)ⅲ.Ag2S2O3是难溶于水、可溶于Na2S2O3溶液的白色固体。
(1)实验室可利用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制备Na2S2O3,装置如下图。

①用化学用语解释Na2S和Na2CO3的混合溶液呈碱性的原因:S2-+H2O
 HS-+OH-、
HS-+OH-、②为了保证Na2S2O3的产量,实验中通入的SO2不能过量。要控制SO2的生成速率,可以采取的措施有:
(2)探究Na2S2O3溶液与不同金属的硫酸盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 | |
 | 试管 | 滴管 | |
| 2mL0.1mol/LNa2S2O3溶液 | Ag2SO4溶液(浓度约为0.03mol/L) | Ⅰ.局部生成白色沉淀,振荡后沉淀溶解,得到无色溶液 | |
| 0.03mol/LAl2(SO4)3溶液 | Ⅱ.一段时间后,生成沉淀 | ||
| 0.03mol/LFe2(SO4)3溶液 | Ⅲ.混合后溶液先变成紫黑色,30s时溶液几乎变为无色 | ||
②经检验,现象Ⅱ中的沉淀有Al(OH)3和S,用平衡移动原理解释Ⅱ中的现象:
③经检验,现象中的无色溶液中含有Fe2+。从化学反应速率和限度的角度解释Ⅲ中Fe3+与S2O
 反应的实验现象:
反应的实验现象:以上实验说明:Na2S2O3溶液与金属阳离子反应的多样性和阳离子的性质有关。
您最近一年使用:0次
2023-12-27更新
|
51次组卷
|
2卷引用:北京市第八中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
4 . 二甲醚(CH3OCH3)是一种极具发展潜力的有机化工产品和洁净燃料。由合成气制备二甲醚的主要反应原理如下:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ/molK1
CH3OH(g) △H1=-90.7kJ/molK1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ/molK2
CH3OCH3(g)+H2O(g) △H2=-23.5kJ/molK2
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ/molK3
CO2(g)+H2(g) △H3=-41.2kJ/molK3
回答下列问题:
(1)反应3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的△H=
CH3OCH3(g)+CO2(g)的△H=___________ kJ/mol;该反应的平衡常数K=___________ (用K1、K2、K3表示)。
(2)下列措施中,能提高(1)中CH3OCH3产率的有___________ 。
A.使用过量的CO B.升高温度 C.增大压强
(3)600℃时,将0.4molCO和0.2molH2O(g)通入2L恒容密闭容器中,发生反应③,5min后达到化学平衡,平衡后测得H2的体积分数为0.2.则0~5min内v(H2O)=___________ ,CO的转化率α(CO)=___________ 。
(4)在600℃时发生反应③,某一时刻测得容器内各物质的浓度分别为c(CO)=0.2mol/L,c(H2O)=0.15mol/L,c(CO2)=0.1mol/L,c(H2)=0.2mol/L,则下一时刻,反应___________ (填“正向进行”、“逆向进行”或“不移动”)。
①CO(g)+2H2(g)
 CH3OH(g) △H1=-90.7kJ/molK1
CH3OH(g) △H1=-90.7kJ/molK1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-23.5kJ/molK2
CH3OCH3(g)+H2O(g) △H2=-23.5kJ/molK2③CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-41.2kJ/molK3
CO2(g)+H2(g) △H3=-41.2kJ/molK3回答下列问题:
(1)反应3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g)的△H=
CH3OCH3(g)+CO2(g)的△H=(2)下列措施中,能提高(1)中CH3OCH3产率的有
A.使用过量的CO B.升高温度 C.增大压强
(3)600℃时,将0.4molCO和0.2molH2O(g)通入2L恒容密闭容器中,发生反应③,5min后达到化学平衡,平衡后测得H2的体积分数为0.2.则0~5min内v(H2O)=
(4)在600℃时发生反应③,某一时刻测得容器内各物质的浓度分别为c(CO)=0.2mol/L,c(H2O)=0.15mol/L,c(CO2)=0.1mol/L,c(H2)=0.2mol/L,则下一时刻,反应
您最近一年使用:0次
解题方法
5 . 合成氨是人类科技发展史上的一项重大突破。
(1)在一定条件下, 和
和 反应生成
反应生成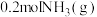 ,放出
,放出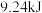 的热量,写出该可逆反应的热化学方程式:
的热量,写出该可逆反应的热化学方程式:_____ 。
(2)将 和
和 通入体积为
通入体积为 的恒温恒容密闭容器中,
的恒温恒容密闭容器中, 后达到化学平衡,测得
后达到化学平衡,测得 的浓度为
的浓度为 ,这段时间内用
,这段时间内用 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为_____ 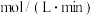 。
。
(3)理论上,为了增大平衡时 的转化率,可采取的措施是
的转化率,可采取的措施是_____ (写出一条)。
(4)下图是某压强下 和
和 按物质的量之比
按物质的量之比 投料进行反应,反应混合物中
投料进行反应,反应混合物中 的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是_____ 。

A.图中a点,容器内
B.图中 点,
点,
C.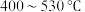 ,Ⅱ中
,Ⅱ中 的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
(1)在一定条件下,
 和
和 反应生成
反应生成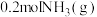 ,放出
,放出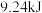 的热量,写出该可逆反应的热化学方程式:
的热量,写出该可逆反应的热化学方程式:(2)将
 和
和 通入体积为
通入体积为 的恒温恒容密闭容器中,
的恒温恒容密闭容器中, 后达到化学平衡,测得
后达到化学平衡,测得 的浓度为
的浓度为 ,这段时间内用
,这段时间内用 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为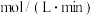 。
。(3)理论上,为了增大平衡时
 的转化率,可采取的措施是
的转化率,可采取的措施是(4)下图是某压强下
 和
和 按物质的量之比
按物质的量之比 投料进行反应,反应混合物中
投料进行反应,反应混合物中 的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
A.图中a点,容器内

B.图中
 点,
点,
C.
 ,Ⅱ中
,Ⅱ中 的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
您最近一年使用:0次
名校
解题方法
6 . 我国提出2060年达“碳中和”目标,通过反应CO2+H2 HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
(1)向恒容密闭容器中充入1molCO2和lmolH2,发生反应:CO2(g)+H2(g) HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
①该反应的△H_______ 0(填“>”或“<”)。已知:2H2(g)+O2(g)=2H2O(g)△H1,则反应2CO2(g)+2H2O(g)  2HCOOH(g)+O2(g)的△H2
2HCOOH(g)+O2(g)的△H2_______ (用△H和△H1表示)。
②下列有利于提高CO2的平衡转化率的措施有_______ (填标号)。
A.增大反应体系的压强 B.增大 C.降低反应温度 D.移出HCOOH
C.降低反应温度 D.移出HCOOH
③373K下,平衡时压强为P,用各物质的平衡分压(分压=总压×物质的量分数)表示该反应的平衡常数Kp=_________ (用含α和P的代数式表示)。
(2)浙江大学某国家实验室用水热法还原CO2转化为HCOOH,探究了不同条件下CO2的转化率,数据如图所示:
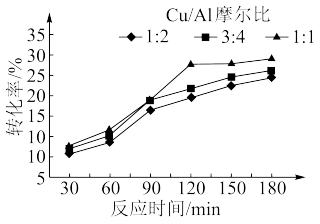
依据以上数据,最佳的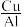 摩尔比和反应时间是
摩尔比和反应时间是______ 。
(3)中国科学院大学以Bi为电极材料,利用电化学催化还原法制备HCOOH。用计算机模拟CO2在电极材料表面发生还原反应的历程如图(*表示微粒与Bi的接触位点):
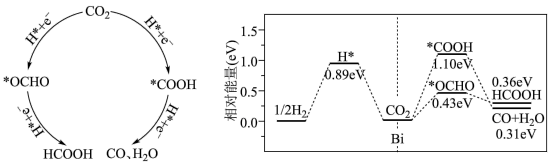
①HCOOH是________ (填“阴极”或“阳极”)产物,若在该电极消耗22gCO2,则转移电子数目为________ 。
②依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性______ (填“高于”或“低于”)生成CO的选择性,原因是________ 。
 HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:(1)向恒容密闭容器中充入1molCO2和lmolH2,发生反应:CO2(g)+H2(g)
 HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:| T/K | 373 | 473 | 573 | 673 |
| 平衡转化率 | α | 8.4α | 24.3α | 37.5α |
 2HCOOH(g)+O2(g)的△H2
2HCOOH(g)+O2(g)的△H2②下列有利于提高CO2的平衡转化率的措施有
A.增大反应体系的压强 B.增大
 C.降低反应温度 D.移出HCOOH
C.降低反应温度 D.移出HCOOH③373K下,平衡时压强为P,用各物质的平衡分压(分压=总压×物质的量分数)表示该反应的平衡常数Kp=
(2)浙江大学某国家实验室用水热法还原CO2转化为HCOOH,探究了不同条件下CO2的转化率,数据如图所示:

依据以上数据,最佳的
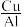 摩尔比和反应时间是
摩尔比和反应时间是(3)中国科学院大学以Bi为电极材料,利用电化学催化还原法制备HCOOH。用计算机模拟CO2在电极材料表面发生还原反应的历程如图(*表示微粒与Bi的接触位点):

①HCOOH是
②依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性
您最近一年使用:0次
名校
解题方法
7 . 氟铈矿(含CeFCO3、BaO、SiO2等)是稀土元素最主要的来源,其中不仅含有丰富的稀土元素Ce(31.51%,以CeO2计),还含有大量的F资源(8.92%)和其他稀土资源(30.71%,用RE表示),其分离工艺流程如下:

已知:①氧化焙烧时,Ce元素转化成CeO2;
②酸浸后,Ce元素主要以Ce4+形式存在,其他稀土RE主要以RE3+形式存在;
③Ce4+能与F-结合成[CeF2]2+,Al3+能与F-结合成[AlFx]3-x,均易溶于水,难溶于有机溶剂,不能被P204萃取剂萃取。
回答下列问题:
(1)为了提高生产效率,焙烧时可以采取的操作___________ 。
(2)废渣的主要成分是___________ 。
(3)氧化焙烧时及萃取之前,均加入铝盐,其目的是___________ 。
(4)萃取Ce4+时,选用经典的酸性有机萃取剂P204(可用HA表示),萃取的过程可以表示成 ,通过将萃取后的有机相pH值调
,通过将萃取后的有机相pH值调___________ (填“高”或“低”)来将Ce4+从萃取剂中分离出来。
(5)将上述过程中获得Ce4+还原成Ce3+,再加入NH4HCO3溶液,即可获得稀土发光材料Ce2(CO3)3,但实际操作中,通常固体产品中含有少量Ce(OH)3,则当溶液Ce3+恰好完全沉淀时,即 ,
,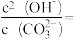
___________ ,为了使该条件下获得的固体产品中不含Ce(OH)3,应控制pH不超过___________ 。(已知常温下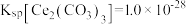 ,
,
(6)水相2中,n(Al):n(F)=1:4,请写出生成Na3AlF6沉淀的离子方程式___________ 。

已知:①氧化焙烧时,Ce元素转化成CeO2;
②酸浸后,Ce元素主要以Ce4+形式存在,其他稀土RE主要以RE3+形式存在;
③Ce4+能与F-结合成[CeF2]2+,Al3+能与F-结合成[AlFx]3-x,均易溶于水,难溶于有机溶剂,不能被P204萃取剂萃取。
回答下列问题:
(1)为了提高生产效率,焙烧时可以采取的操作
(2)废渣的主要成分是
(3)氧化焙烧时及萃取之前,均加入铝盐,其目的是
(4)萃取Ce4+时,选用经典的酸性有机萃取剂P204(可用HA表示),萃取的过程可以表示成
 ,通过将萃取后的有机相pH值调
,通过将萃取后的有机相pH值调(5)将上述过程中获得Ce4+还原成Ce3+,再加入NH4HCO3溶液,即可获得稀土发光材料Ce2(CO3)3,但实际操作中,通常固体产品中含有少量Ce(OH)3,则当溶液Ce3+恰好完全沉淀时,即
 ,
,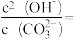
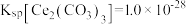 ,
,
(6)水相2中,n(Al):n(F)=1:4,请写出生成Na3AlF6沉淀的离子方程式
您最近一年使用:0次
名校
解题方法
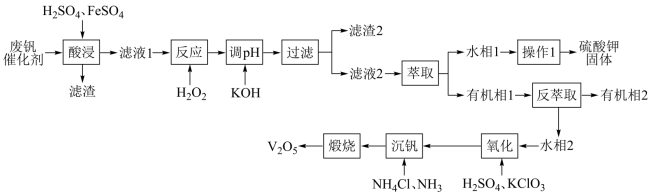
8 . 五氧化二钒广泛用于冶金、化工等行业,用作合金添加剂、生产硫酸或石油精炼用的催化剂等。从废钒催化剂中(含有K2SO4、V2O5、V2O4、SiO2、Fe2O3、Al2O3等)回收钒,既能避免对环境的污染,又能节约宝贵的资源。回收工艺流程如图:
“酸浸”时V2O5和V2O4先与稀硫酸反应分别生成VO 和VO2+。
和VO2+。
②有机萃取剂萃取VO2+的能力比萃取VO 的能力强。
的能力强。
③溶液中VO 与VO
与VO 可相互转化:VO
可相互转化:VO +H2O
+H2O VO
VO +2H+且NH4VO3为沉淀
+2H+且NH4VO3为沉淀
(1)“酸浸”时,FeSO4参与反应的离子方程式为_______ 。
(2)“萃取”和“反萃取”时,将发生R2(SO4)n(水层)+2nHA(有机层) 2RAn(有机层)+nH2SO4(水层)(R表示VO2+,HA表示有机萃取剂),“反萃取”加入试剂
2RAn(有机层)+nH2SO4(水层)(R表示VO2+,HA表示有机萃取剂),“反萃取”加入试剂_______ 。(填化学式)
(3)“氧化”过程中发生反应的离子方程式为_______ 。
(4)“沉钒”时,通入氨气的作用是_______ ,以沉钒率(NH4VO3沉淀中V的质量和废催化剂V的质量之比)表示该步反应钒的回收率。请解释如图温度超过80℃以后,沉钒率下降的可能原因是_______ 。
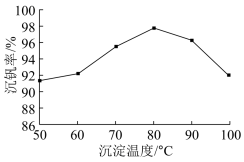
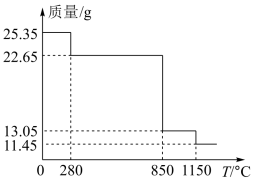
(5)25.35gMnSO4•H2O样品受热分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。1150℃时,反应的化学方程式为_______ 。
“酸浸”时V2O5和V2O4先与稀硫酸反应分别生成VO
 和VO2+。
和VO2+。②有机萃取剂萃取VO2+的能力比萃取VO
 的能力强。
的能力强。③溶液中VO
 与VO
与VO 可相互转化:VO
可相互转化:VO +H2O
+H2O VO
VO +2H+且NH4VO3为沉淀
+2H+且NH4VO3为沉淀(1)“酸浸”时,FeSO4参与反应的离子方程式为
(2)“萃取”和“反萃取”时,将发生R2(SO4)n(水层)+2nHA(有机层)
 2RAn(有机层)+nH2SO4(水层)(R表示VO2+,HA表示有机萃取剂),“反萃取”加入试剂
2RAn(有机层)+nH2SO4(水层)(R表示VO2+,HA表示有机萃取剂),“反萃取”加入试剂(3)“氧化”过程中发生反应的离子方程式为
(4)“沉钒”时,通入氨气的作用是

(5)25.35gMnSO4•H2O样品受热分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。1150℃时,反应的化学方程式为

您最近一年使用:0次
解题方法
9 . 草酸亚铁晶体( FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.采用如下装置(可重复选用)进行实验探究纯净草酸亚铁晶体受热分解的产物。

(1)装置D的名称为___________ ,作用是_________________________________ 。
(2)按照气流从左到右的方向,上述装置的连接顺序为a→_____________ →d→e→b→c→尾气处理装置(填仪器接口的小字母编号)。
(3)能证明分解产物中存在CO的现象是_____________________ 。
II.将54.0g草酸亚铁晶体在氮气的氛围中加热分解,得到分解产物的热重曲线(样品质量随温度的变化情况)如图所示:

(4)B点时,固体只含有一种铁的氧化物,则所得固体的化学式为__________ 。
Ⅲ.文献表明:相同条件下,草酸根(C2O )的还原性强于Fe2+。为检验这一结论进行以下实验。
)的还原性强于Fe2+。为检验这一结论进行以下实验。
资料:ⅰ.草酸(H2C2O4)为二元弱酸。
ⅱ.三水三草酸合铁酸钾K3[Fe(C2O4)3]·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3] 3− Fe3++ 3C2O
Fe3++ 3C2O K=6.3×10−21
K=6.3×10−21
通过Fe3+和C2O 在溶液中的反应比较Fe2+和C2O
在溶液中的反应比较Fe2+和C2O 的还原性强弱
的还原性强弱
(5)取实验中的少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红。加硫酸后溶液变红的原因是__________________________________ 。
(6)经检验,翠绿色晶体为K3[Fe(C2O4)3]·3H2O。请设计实验,确认实验中没有发生氧化还原反应的操作和现象是_____________ 。
I.采用如下装置(可重复选用)进行实验探究纯净草酸亚铁晶体受热分解的产物。

(1)装置D的名称为
(2)按照气流从左到右的方向,上述装置的连接顺序为a→
(3)能证明分解产物中存在CO的现象是
II.将54.0g草酸亚铁晶体在氮气的氛围中加热分解,得到分解产物的热重曲线(样品质量随温度的变化情况)如图所示:

(4)B点时,固体只含有一种铁的氧化物,则所得固体的化学式为
Ⅲ.文献表明:相同条件下,草酸根(C2O
 )的还原性强于Fe2+。为检验这一结论进行以下实验。
)的还原性强于Fe2+。为检验这一结论进行以下实验。资料:ⅰ.草酸(H2C2O4)为二元弱酸。
ⅱ.三水三草酸合铁酸钾K3[Fe(C2O4)3]·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3] 3−
 Fe3++ 3C2O
Fe3++ 3C2O K=6.3×10−21
K=6.3×10−21通过Fe3+和C2O
 在溶液中的反应比较Fe2+和C2O
在溶液中的反应比较Fe2+和C2O 的还原性强弱
的还原性强弱| 操作 | 现象 |
| 在避光处,向10mL0.5mol∙L-1FeCl3溶液中缓慢加入0.5mol∙L-1K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤 | 得到翠绿色溶液和翠绿色晶体 |
(6)经检验,翠绿色晶体为K3[Fe(C2O4)3]·3H2O。请设计实验,确认实验中没有发生氧化还原反应的操作和现象是
您最近一年使用:0次
解题方法
10 . 硒是人体必需微量元素之一,可用作光敏材料、电解锰行业催化剂、动物体必需的营养元素和植物有益的营养元素等。粗硒经过下列流程可获得亚硒酸钠( )。
)。
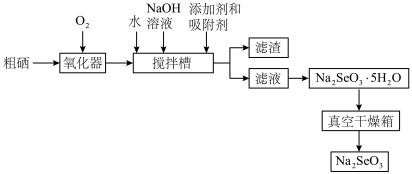
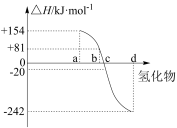
(1)298K、 ,
, 、S、Se、Te分别与
、S、Se、Te分别与 化合的反应热数据如下图所示。写出Se与
化合的反应热数据如下图所示。写出Se与 化合的热化学反应方程式:
化合的热化学反应方程式:___________ 。
(2)硒与硫是同主族的相邻元素,硒的原子序数为___________ 。
(3)已知在氧化器中粗硒转化为 ,在搅拌槽中与NaOH发生反应的离子方程式为
,在搅拌槽中与NaOH发生反应的离子方程式为______ 。
(4)由滤液获取 晶体的操作为
晶体的操作为___________ 、过滤、洗涤。
(5) 转化为
转化为 的过程中存在平衡
的过程中存在平衡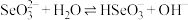 ,下列粒子中不会影响该平衡的是___________(填字母)。
,下列粒子中不会影响该平衡的是___________(填字母)。
(6)常温下,向 溶液中逐滴加入NaOH溶液,混合溶液中
溶液中逐滴加入NaOH溶液,混合溶液中 [X为
[X为 或
或 ]与pH的变化关系如图所示。
]与pH的变化关系如图所示。
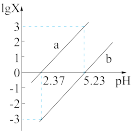
①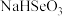 溶液呈
溶液呈___________ 性(填“酸”“碱”或“中”)。
② 时,溶液中
时,溶液中
___________ 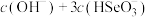 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 )。
)。
(1)298K、
 ,
, 、S、Se、Te分别与
、S、Se、Te分别与 化合的反应热数据如下图所示。写出Se与
化合的反应热数据如下图所示。写出Se与 化合的热化学反应方程式:
化合的热化学反应方程式:
(2)硒与硫是同主族的相邻元素,硒的原子序数为
(3)已知在氧化器中粗硒转化为
 ,在搅拌槽中与NaOH发生反应的离子方程式为
,在搅拌槽中与NaOH发生反应的离子方程式为(4)由滤液获取
 晶体的操作为
晶体的操作为(5)
 转化为
转化为 的过程中存在平衡
的过程中存在平衡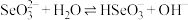 ,下列粒子中不会影响该平衡的是___________(填字母)。
,下列粒子中不会影响该平衡的是___________(填字母)。A. | B. | C. | D.O=C=O |
 溶液中逐滴加入NaOH溶液,混合溶液中
溶液中逐滴加入NaOH溶液,混合溶液中 [X为
[X为 或
或 ]与pH的变化关系如图所示。
]与pH的变化关系如图所示。
①
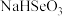 溶液呈
溶液呈②
 时,溶液中
时,溶液中
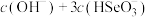 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次



