名校
解题方法
1 . 在煤化工领域主要涉及碳一化学,即研究以含有一个碳原子的物质(CO、 、
、 、
、 等)为原料合成化工产品或液体燃料。回答下列问题:
等)为原料合成化工产品或液体燃料。回答下列问题:
(1)已知物质之间转化能量关系如图所示: 和
和 生成
生成 和
和 的热化学方程式
的热化学方程式___________ 。
(2)煤化工业上主要利用CO和 反应制备甲醇(
反应制备甲醇( ),反应热化学方程式为
),反应热化学方程式为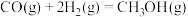
 。已知CO的平衡转化率与温度的关系如图所示:
。已知CO的平衡转化率与温度的关系如图所示:
___________ (填“>”“<”或“=”)0。
②A、B、C三点平衡常数 、
、 、
、 的大小关系为
的大小关系为___________ 。压强
___________ (填“>”“<”或“=”,下同) ,在
,在 和
和 条件下,由D点到B点过程中,正、逆反应速率之间的关系:
条件下,由D点到B点过程中,正、逆反应速率之间的关系:
___________  。
。
③若容器容积不变,则下列措施可提高CO平衡转化率的是___________ (填字母)。
a.充入CO,使体系总压强增大 b.将 从体系中分离
从体系中分离
c.充入He,使体系总压强增大 d.使用高效催化剂
④在2L恒容密闭容器中充入2molCO和 ,在
,在 和
和 条件下经10min达到平衡状态。在该条件下,
条件下经10min达到平衡状态。在该条件下,
___________  ;平衡常数
;平衡常数
___________ (填数值)。
(3)用 还原
还原 可以合成
可以合成 :
:
 。恒压下,
。恒压下, 和
和 的起始物质的量之比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜(能选择性分离出
的起始物质的量之比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜(能选择性分离出 )时甲醇的产率随温度的变化如图所示。P点甲醇产率高于T点的原因为
)时甲醇的产率随温度的变化如图所示。P点甲醇产率高于T点的原因为___________ 。
 、
、 、
、 等)为原料合成化工产品或液体燃料。回答下列问题:
等)为原料合成化工产品或液体燃料。回答下列问题:(1)已知物质之间转化能量关系如图所示:

 和
和 生成
生成 和
和 的热化学方程式
的热化学方程式(2)煤化工业上主要利用CO和
 反应制备甲醇(
反应制备甲醇( ),反应热化学方程式为
),反应热化学方程式为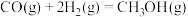
 。已知CO的平衡转化率与温度的关系如图所示:
。已知CO的平衡转化率与温度的关系如图所示: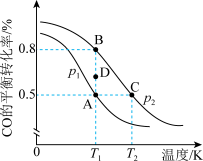

②A、B、C三点平衡常数
 、
、 、
、 的大小关系为
的大小关系为
 ,在
,在 和
和 条件下,由D点到B点过程中,正、逆反应速率之间的关系:
条件下,由D点到B点过程中,正、逆反应速率之间的关系:
 。
。③若容器容积不变,则下列措施可提高CO平衡转化率的是
a.充入CO,使体系总压强增大 b.将
 从体系中分离
从体系中分离c.充入He,使体系总压强增大 d.使用高效催化剂
④在2L恒容密闭容器中充入2molCO和
 ,在
,在 和
和 条件下经10min达到平衡状态。在该条件下,
条件下经10min达到平衡状态。在该条件下,
 ;平衡常数
;平衡常数
(3)用
 还原
还原 可以合成
可以合成 :
:
 。恒压下,
。恒压下, 和
和 的起始物质的量之比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜(能选择性分离出
的起始物质的量之比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜(能选择性分离出 )时甲醇的产率随温度的变化如图所示。P点甲醇产率高于T点的原因为
)时甲醇的产率随温度的变化如图所示。P点甲醇产率高于T点的原因为
您最近一年使用:0次
2024-01-12更新
|
251次组卷
|
2卷引用:安徽省芜湖市第一中学2022-2023学年高二上学期10月月考化学试卷
名校
解题方法
2 . 二甲醚(CH3OCH3)是一种极具发展潜力的有机化工产品和洁净燃料。由合成气制备二甲醚的主要反应原理如下:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ/molK1
CH3OH(g) △H1=-90.7kJ/molK1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ/molK2
CH3OCH3(g)+H2O(g) △H2=-23.5kJ/molK2
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ/molK3
CO2(g)+H2(g) △H3=-41.2kJ/molK3
回答下列问题:
(1)反应3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的△H=
CH3OCH3(g)+CO2(g)的△H=___________ kJ/mol;该反应的平衡常数K=___________ (用K1、K2、K3表示)。
(2)下列措施中,能提高(1)中CH3OCH3产率的有___________ 。
A.使用过量的CO B.升高温度 C.增大压强
(3)600℃时,将0.4molCO和0.2molH2O(g)通入2L恒容密闭容器中,发生反应③,5min后达到化学平衡,平衡后测得H2的体积分数为0.2.则0~5min内v(H2O)=___________ ,CO的转化率α(CO)=___________ 。
(4)在600℃时发生反应③,某一时刻测得容器内各物质的浓度分别为c(CO)=0.2mol/L,c(H2O)=0.15mol/L,c(CO2)=0.1mol/L,c(H2)=0.2mol/L,则下一时刻,反应___________ (填“正向进行”、“逆向进行”或“不移动”)。
①CO(g)+2H2(g)
 CH3OH(g) △H1=-90.7kJ/molK1
CH3OH(g) △H1=-90.7kJ/molK1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-23.5kJ/molK2
CH3OCH3(g)+H2O(g) △H2=-23.5kJ/molK2③CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-41.2kJ/molK3
CO2(g)+H2(g) △H3=-41.2kJ/molK3回答下列问题:
(1)反应3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g)的△H=
CH3OCH3(g)+CO2(g)的△H=(2)下列措施中,能提高(1)中CH3OCH3产率的有
A.使用过量的CO B.升高温度 C.增大压强
(3)600℃时,将0.4molCO和0.2molH2O(g)通入2L恒容密闭容器中,发生反应③,5min后达到化学平衡,平衡后测得H2的体积分数为0.2.则0~5min内v(H2O)=
(4)在600℃时发生反应③,某一时刻测得容器内各物质的浓度分别为c(CO)=0.2mol/L,c(H2O)=0.15mol/L,c(CO2)=0.1mol/L,c(H2)=0.2mol/L,则下一时刻,反应
您最近一年使用:0次
名校
解题方法
3 . 我国提出2060年达“碳中和”目标,通过反应CO2+H2 HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
(1)向恒容密闭容器中充入1molCO2和lmolH2,发生反应:CO2(g)+H2(g) HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
①该反应的△H_______ 0(填“>”或“<”)。已知:2H2(g)+O2(g)=2H2O(g)△H1,则反应2CO2(g)+2H2O(g)  2HCOOH(g)+O2(g)的△H2
2HCOOH(g)+O2(g)的△H2_______ (用△H和△H1表示)。
②下列有利于提高CO2的平衡转化率的措施有_______ (填标号)。
A.增大反应体系的压强 B.增大 C.降低反应温度 D.移出HCOOH
C.降低反应温度 D.移出HCOOH
③373K下,平衡时压强为P,用各物质的平衡分压(分压=总压×物质的量分数)表示该反应的平衡常数Kp=_________ (用含α和P的代数式表示)。
(2)浙江大学某国家实验室用水热法还原CO2转化为HCOOH,探究了不同条件下CO2的转化率,数据如图所示:
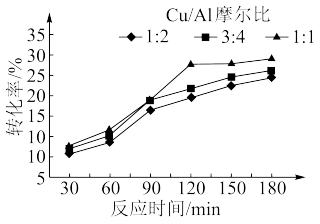
依据以上数据,最佳的 摩尔比和反应时间是
摩尔比和反应时间是______ 。
(3)中国科学院大学以Bi为电极材料,利用电化学催化还原法制备HCOOH。用计算机模拟CO2在电极材料表面发生还原反应的历程如图(*表示微粒与Bi的接触位点):
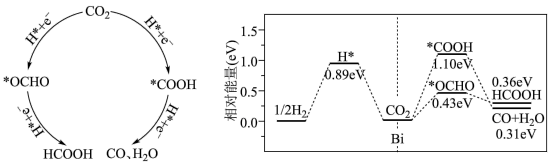
①HCOOH是________ (填“阴极”或“阳极”)产物,若在该电极消耗22gCO2,则转移电子数目为________ 。
②依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性______ (填“高于”或“低于”)生成CO的选择性,原因是________ 。
 HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:
HCOOH将CO2转化为高附加值产品HCOOH是实现该目标的一种方式。回答下列问题:(1)向恒容密闭容器中充入1molCO2和lmolH2,发生反应:CO2(g)+H2(g)
 HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:
HCOOH(g) △H。测定不同温度下CO2的平衡转化率数据如表所示:| T/K | 373 | 473 | 573 | 673 |
| 平衡转化率 | α | 8.4α | 24.3α | 37.5α |
 2HCOOH(g)+O2(g)的△H2
2HCOOH(g)+O2(g)的△H2②下列有利于提高CO2的平衡转化率的措施有
A.增大反应体系的压强 B.增大
 C.降低反应温度 D.移出HCOOH
C.降低反应温度 D.移出HCOOH③373K下,平衡时压强为P,用各物质的平衡分压(分压=总压×物质的量分数)表示该反应的平衡常数Kp=
(2)浙江大学某国家实验室用水热法还原CO2转化为HCOOH,探究了不同条件下CO2的转化率,数据如图所示:

依据以上数据,最佳的
 摩尔比和反应时间是
摩尔比和反应时间是(3)中国科学院大学以Bi为电极材料,利用电化学催化还原法制备HCOOH。用计算机模拟CO2在电极材料表面发生还原反应的历程如图(*表示微粒与Bi的接触位点):

①HCOOH是
②依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性
您最近一年使用:0次
解题方法
4 . 草酸亚铁晶体( FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.采用如下装置(可重复选用)进行实验探究纯净草酸亚铁晶体受热分解的产物。

(1)装置D的名称为___________ ,作用是_________________________________ 。
(2)按照气流从左到右的方向,上述装置的连接顺序为a→_____________ →d→e→b→c→尾气处理装置(填仪器接口的小字母编号)。
(3)能证明分解产物中存在CO的现象是_____________________ 。
II.将54.0g草酸亚铁晶体在氮气的氛围中加热分解,得到分解产物的热重曲线(样品质量随温度的变化情况)如图所示:

(4)B点时,固体只含有一种铁的氧化物,则所得固体的化学式为__________ 。
Ⅲ.文献表明:相同条件下,草酸根(C2O )的还原性强于Fe2+。为检验这一结论进行以下实验。
)的还原性强于Fe2+。为检验这一结论进行以下实验。
资料:ⅰ.草酸(H2C2O4)为二元弱酸。
ⅱ.三水三草酸合铁酸钾K3[Fe(C2O4)3]·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3] 3− Fe3++ 3C2O
Fe3++ 3C2O K=6.3×10−21
K=6.3×10−21
通过Fe3+和C2O 在溶液中的反应比较Fe2+和C2O
在溶液中的反应比较Fe2+和C2O 的还原性强弱
的还原性强弱
(5)取实验中的少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红。加硫酸后溶液变红的原因是__________________________________ 。
(6)经检验,翠绿色晶体为K3[Fe(C2O4)3]·3H2O。请设计实验,确认实验中没有发生氧化还原反应的操作和现象是_____________ 。
I.采用如下装置(可重复选用)进行实验探究纯净草酸亚铁晶体受热分解的产物。

(1)装置D的名称为
(2)按照气流从左到右的方向,上述装置的连接顺序为a→
(3)能证明分解产物中存在CO的现象是
II.将54.0g草酸亚铁晶体在氮气的氛围中加热分解,得到分解产物的热重曲线(样品质量随温度的变化情况)如图所示:

(4)B点时,固体只含有一种铁的氧化物,则所得固体的化学式为
Ⅲ.文献表明:相同条件下,草酸根(C2O
 )的还原性强于Fe2+。为检验这一结论进行以下实验。
)的还原性强于Fe2+。为检验这一结论进行以下实验。资料:ⅰ.草酸(H2C2O4)为二元弱酸。
ⅱ.三水三草酸合铁酸钾K3[Fe(C2O4)3]·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3] 3−
 Fe3++ 3C2O
Fe3++ 3C2O K=6.3×10−21
K=6.3×10−21通过Fe3+和C2O
 在溶液中的反应比较Fe2+和C2O
在溶液中的反应比较Fe2+和C2O 的还原性强弱
的还原性强弱| 操作 | 现象 |
| 在避光处,向10mL0.5mol∙L-1FeCl3溶液中缓慢加入0.5mol∙L-1K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤 | 得到翠绿色溶液和翠绿色晶体 |
(6)经检验,翠绿色晶体为K3[Fe(C2O4)3]·3H2O。请设计实验,确认实验中没有发生氧化还原反应的操作和现象是
您最近一年使用:0次
解题方法
5 . 亚硝酰氯(NOCl)是有机合成中的重要试剂。实验室中可用如下反应合成。
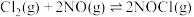

(1)已知 (忽略
(忽略 、
、 随温度的变化,T为开尔文温度)。上述反应的
随温度的变化,T为开尔文温度)。上述反应的 与温度的关系如下图(该反应的
与温度的关系如下图(该反应的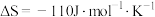 )。
)。

该反应在常温下________ (填“能”或“不能”)自发进行;该反应的
_______  。
。
(2)T°C下,向某真空恒容密闭容器中加入足量的 并充入一定量的NO(g),发生下列反应:
并充入一定量的NO(g),发生下列反应:
反应Ⅰ: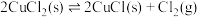

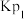
反应Ⅱ:

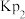
已知:反应Ⅰ、Ⅱ的平衡常数1gKp~T关系如下图:
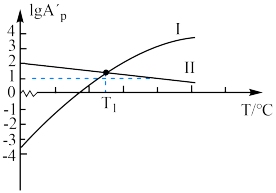
①由图可知,反应Ⅰ反应热
___________ (填“>”或“<”)0。
② °C下,测得起始压强为20kPa,平衡时压强为21kPa,则该温度下NO的平衡转化率为
°C下,测得起始压强为20kPa,平衡时压强为21kPa,则该温度下NO的平衡转化率为_____ %;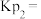
________ 。
(3)向体积均为1L的两恒容容器中分别充入2molNO和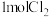 ,发生反应:
,发生反应: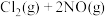
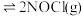 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。
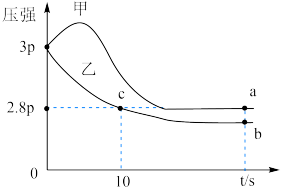
①甲容器中,开始压强变大的原因___________ 。
②乙容器中0~10s内平均反应速率v(NO)=___________ 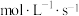 。
。
③a、b、c三点的正反应速率最小的是___________ 点。
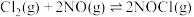

(1)已知
 (忽略
(忽略 、
、 随温度的变化,T为开尔文温度)。上述反应的
随温度的变化,T为开尔文温度)。上述反应的 与温度的关系如下图(该反应的
与温度的关系如下图(该反应的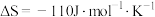 )。
)。
该反应在常温下

 。
。(2)T°C下,向某真空恒容密闭容器中加入足量的
 并充入一定量的NO(g),发生下列反应:
并充入一定量的NO(g),发生下列反应:反应Ⅰ:
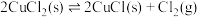

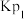
反应Ⅱ:


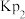
已知:反应Ⅰ、Ⅱ的平衡常数1gKp~T关系如下图:

①由图可知,反应Ⅰ反应热

②
 °C下,测得起始压强为20kPa,平衡时压强为21kPa,则该温度下NO的平衡转化率为
°C下,测得起始压强为20kPa,平衡时压强为21kPa,则该温度下NO的平衡转化率为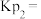
(3)向体积均为1L的两恒容容器中分别充入2molNO和
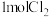 ,发生反应:
,发生反应: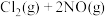
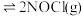 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。
①甲容器中,开始压强变大的原因
②乙容器中0~10s内平均反应速率v(NO)=
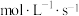 。
。③a、b、c三点的正反应速率最小的是
您最近一年使用:0次
名校
解题方法
6 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶液平衡均属于化学平衡
Ⅰ.已知H2A在水中存在以下平衡:H2A⇌H++HA-,HA-⇌H++A2-
(1)NaHA溶液的pH_______ (填大于、小于或等于) Na2A溶液的pH
(2)某温度下,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是_______
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s) ⇌Ca2+(aq)+A2-(aq) ∆H>0
①降低温度时,Ksp_______ (填“增大”、“减小”或“不变”)
②滴加少量浓盐酸,c(Ca2+)_______ (填“增大”、“减小”或“不变”)
Ⅱ.含有Cr2O 的废水毒性较大,某工厂废水中含5.00×10-3 mol•L-1的Cr2O
的废水毒性较大,某工厂废水中含5.00×10-3 mol•L-1的Cr2O 。为使废水能达标排放,作如下处理:
。为使废水能达标排放,作如下处理:
Cr2O
 Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
(4)该废水中加入绿矾(FeSO4•7H2O)和H+,发生反应的离子方程式为:_______
(5)欲使10L该废水中的Cr2O 完全转化为Cr3+,理论上需要加入
完全转化为Cr3+,理论上需要加入_______ g FeSO4•7H2O
(6)若处理后的废水中残留的c(Fe3+)=2×10-13mol•L-1,则残留的Cr3+的浓度为_______ (已知:Ksp[Fe(OH)3]=4.0×10-38 Ksp[Cr(OH)3]=6.0×10-31)
Ⅰ.已知H2A在水中存在以下平衡:H2A⇌H++HA-,HA-⇌H++A2-
(1)NaHA溶液的pH
(2)某温度下,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是_______
| A.c(H+)•c(OH-)=1×10-14 | B.c(Na+)+c(K+)=c(HA-)+2c(A2-) |
| C.c(Na+)>c(K+) | D.c(Na+)+c(K+)=0.05mol/L |
①降低温度时,Ksp
②滴加少量浓盐酸,c(Ca2+)
Ⅱ.含有Cr2O
 的废水毒性较大,某工厂废水中含5.00×10-3 mol•L-1的Cr2O
的废水毒性较大,某工厂废水中含5.00×10-3 mol•L-1的Cr2O 。为使废水能达标排放,作如下处理:
。为使废水能达标排放,作如下处理: Cr2O

 Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3(4)该废水中加入绿矾(FeSO4•7H2O)和H+,发生反应的离子方程式为:
(5)欲使10L该废水中的Cr2O
 完全转化为Cr3+,理论上需要加入
完全转化为Cr3+,理论上需要加入(6)若处理后的废水中残留的c(Fe3+)=2×10-13mol•L-1,则残留的Cr3+的浓度为
您最近一年使用:0次
21-22高二·浙江·期中
解题方法
7 . CH3COOH是食醋的主要成分,用化学反应原理可以研究其性质。
(1)气态CH3COOH中存在平衡2CH3COOH (CH3COOH)2 △H<0, 若要准确测定CH3COOH的相对分子质量,应选用的条件是___________。
(CH3COOH)2 △H<0, 若要准确测定CH3COOH的相对分子质量,应选用的条件是___________。
(2)用滴定法可以测定食醋中醋酸的含量,用酸式滴定管取10.00mL这种市售食醋,置于已知烧杯中称得其质量为12.50g,再稀释至100mL,滴定时每次取20.00 mL于锥形瓶中,选用的标准溶液是0.1125 mol/LNaOH溶液滴定至终点,平均每次消耗NaOH溶液20.00mL。
①该实验中的指示剂应选择___________ (填“酚酞”、“甲基橙”或“石蕊”),滴定终点的现象为___________ 。
②该食醋中CH3COOH的质量分数为___________ (CH3COOH的相对分子质量为60,结果保留三位有效数字)。
③滴定过程中下列操作会导致测定的CH3COOH的质量分数偏小的是(其它操作均正确)___________ 。
A.碱式滴定管在装液前未用待测NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分无气泡,在滴定终点读数时发现气泡
C.达到滴定终点时,俯视溶液凹液面最低点读数
D.滴定过程中,部分NaOH溶液滴到锥形瓶外
(1)气态CH3COOH中存在平衡2CH3COOH
 (CH3COOH)2 △H<0, 若要准确测定CH3COOH的相对分子质量,应选用的条件是___________。
(CH3COOH)2 △H<0, 若要准确测定CH3COOH的相对分子质量,应选用的条件是___________。| A.低温低压 | B.低温高压 | C.高温低压 | D.高温高压 |
①该实验中的指示剂应选择
②该食醋中CH3COOH的质量分数为
③滴定过程中下列操作会导致测定的CH3COOH的质量分数偏小的是(其它操作均正确)
A.碱式滴定管在装液前未用待测NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分无气泡,在滴定终点读数时发现气泡
C.达到滴定终点时,俯视溶液凹液面最低点读数
D.滴定过程中,部分NaOH溶液滴到锥形瓶外
您最近一年使用:0次
名校
解题方法
8 . 丙烯是一种重要的化工原料。可在一固定容积的密闭容器中由丙烷催化脱氢制备。
(1)已知:
①C3H8(g)=C3H6(g)+H2(g)
②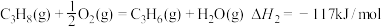
③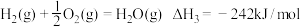
反应①的
________________ 。
(2)欲提高①反应中 的平衡转化率,可采取的措施有________________(填标号)。
的平衡转化率,可采取的措施有________________(填标号)。
(3)能表明该反应①达到平衡状态的是_______________(填字母)。
(4)某温度下,在体积不变的密闭容器内发生反应①,起始总压强为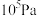 ,平衡时总压增加了20%。则达到平衡时,
,平衡时总压增加了20%。则达到平衡时, 的转化率为
的转化率为__________________ 。该反应的平衡常数
________________ Pa。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)反应④:
在不同催化剂作用下合成甲醇,相同时间内 的转化率随温度变化如图所示,
的转化率随温度变化如图所示,

其中活化能最高,反应速率最慢的所用的催化剂是______ (填“A”、“B”或“C”);请解释温度 之前催化剂不同转化率不同,高于
之前催化剂不同转化率不同,高于 后转化率相同且下降的原因
后转化率相同且下降的原因________________
(1)已知:
①C3H8(g)=C3H6(g)+H2(g)

②
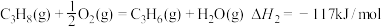
③
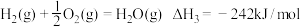
反应①的

(2)欲提高①反应中
 的平衡转化率,可采取的措施有________________(填标号)。
的平衡转化率,可采取的措施有________________(填标号)。A.增大 的浓度 的浓度 | B.提高温度 | C.恒容下通入惰性气体 | D.使用高效催化剂 |
| A.C3H8的转化率等于H2的产率 | B.混合气体的平均相对分子质量不变 |
C.v(C3H8)与 的比值不变 的比值不变 | D.混合气体的密度不变 |
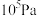 ,平衡时总压增加了20%。则达到平衡时,
,平衡时总压增加了20%。则达到平衡时, 的转化率为
的转化率为
(5)反应④:

在不同催化剂作用下合成甲醇,相同时间内
 的转化率随温度变化如图所示,
的转化率随温度变化如图所示,
其中活化能最高,反应速率最慢的所用的催化剂是
 之前催化剂不同转化率不同,高于
之前催化剂不同转化率不同,高于 后转化率相同且下降的原因
后转化率相同且下降的原因
您最近一年使用:0次
2023-02-22更新
|
202次组卷
|
2卷引用:广西桂林市第十八中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
9 . 电化学原理在探究物质性质和实际生产中应用广泛,据此回答下列问题。

(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜_______ (填“强”或“弱”);由装置乙知常温下铬在浓硝酸中出现_______ 现象(填化学专业名词)。
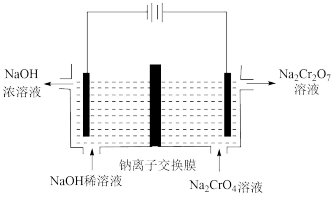
(2)已知存在反应:2 +2H+⇌
+2H+⇌ +H2O。用下图装置,以石墨作电极电解Na2CrO4溶液制备Na2Cr2O7的转化原理为
+H2O。用下图装置,以石墨作电极电解Na2CrO4溶液制备Na2Cr2O7的转化原理为_______ 。
(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(VI)转化为Cr(III)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为_______ 。阴极上 、H+、Fe3+都可能放电。若
、H+、Fe3+都可能放电。若 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为_______ ;若H+放电,则阴极区形成_______ 和Cr(OH)3沉淀。
②铁氧磁体法:在含Cr(VI)的废水中加入FeSO4,在pH<4时发生反应使Cr(VI)转化为Cr(III),调节溶液pH为6~8,使溶液中的Fe(II)、Fe(III)、Cr(III)析出组成相当于Fe(II)[Fe(III)x·Cr(III)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=_______ 。

(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜
(2)已知存在反应:2
 +2H+⇌
+2H+⇌ +H2O。用下图装置,以石墨作电极电解Na2CrO4溶液制备Na2Cr2O7的转化原理为
+H2O。用下图装置,以石墨作电极电解Na2CrO4溶液制备Na2Cr2O7的转化原理为
(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(VI)转化为Cr(III)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含
 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为 、H+、Fe3+都可能放电。若
、H+、Fe3+都可能放电。若 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为②铁氧磁体法:在含Cr(VI)的废水中加入FeSO4,在pH<4时发生反应使Cr(VI)转化为Cr(III),调节溶液pH为6~8,使溶液中的Fe(II)、Fe(III)、Cr(III)析出组成相当于Fe(II)[Fe(III)x·Cr(III)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=
您最近一年使用:0次
名校
解题方法
10 . 纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用。
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为_____ 、_____ 。
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

已知:几种盐的溶解度
(2)①写出装置I中反应的化学方程式_____ 。
②从平衡移动角度解释该反应发生的原因_____ 。
(3)写出装置II中发生反应的化学方程式_____ 。
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用_____ 。
(5)该流程中可循环利用的物质是_____ 。
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是_____ 。
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

已知:几种盐的溶解度
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
| 溶解度(20℃,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
②从平衡移动角度解释该反应发生的原因
(3)写出装置II中发生反应的化学方程式
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用
(5)该流程中可循环利用的物质是
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
您最近一年使用:0次



