1 . 下列实验方案不能达到相应实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 向盛有 溶液的试管中滴加2滴 溶液的试管中滴加2滴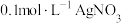 溶液,振荡试管,再向其中滴加4滴 溶液,振荡试管,再向其中滴加4滴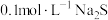 溶液,观察现象 溶液,观察现象 | 证明溶解度  |
| B | 向盛有 溶液的试管中滴加 溶液的试管中滴加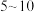 滴 滴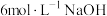 溶液,再继续滴加 溶液,再继续滴加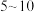 滴 滴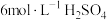 溶液,观察现象 溶液,观察现象 | 证明浓度对化学平衡的影响 |
| C | 向盛有少量蒸馏水的试管中滴加2滴 溶液,再滴加2滴硫氰化钾溶液,观察现象 溶液,再滴加2滴硫氰化钾溶液,观察现象 | 证明 的存在 的存在 |
| D | 室温下,向一定量饱和 溶液中通入足量 溶液中通入足量 气体,观察是否有晶体析出 气体,观察是否有晶体析出 | 证明室温下固体在水中的溶解度: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列有关实验装置、原理和操作正确,且能达到相应实验目的的是
|
|
|
|
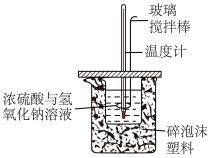
| A.测定Fe2+的浓度 | B.配制100mL一定物质的量浓度的硫酸溶液 | C.测定中和热 | D.探究温度对平衡移动的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 实验室模拟工业处理含铬废水,操作及现象如图1,反应过程中铬元素的化合价变化如图2,下列说法正确的是
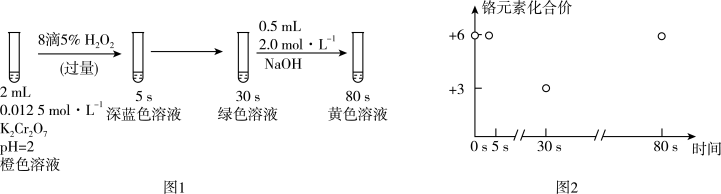
已知:深蓝色溶液中生成了CrO5

已知:深蓝色溶液中生成了CrO5
| A.实验开始至5s,铬元素被氧化 |
B.实验开始至30s,溶液中生成Cr3+的总反应离子方程式为: +3H2O2+8H+=2Cr3++7H2O+3O2↑ +3H2O2+8H+=2Cr3++7H2O+3O2↑ |
| C.30s至80s的过程,一定是氧气氧化了Cr3+ |
| D.80s时,溶液中又生成了Cr2O3,颜色相比于开始时浅,是水稀释所致 |
您最近一年使用:0次
4 . 设NA是阿伏加德罗常数的值。下列说法中正确的是
| A.标准状况下,22.4L3H2所含质子数为4NA |
| B.11.0gH2C2O4·2H2O晶体中含有的离子总数为0.3NA |
| C.100mL0.1mol/LK2Cr2O7酸性溶液中,含铬元素离子的数目为0.01NA |
| D.高温时,0.3mol铁粉与足量水蒸气完全反应时转移电子数为0.8NA |
您最近一年使用:0次
名校
5 . 下列有关实验反应、操作现象及实验结论,不正确的是
| 选项 | 实验反应 | 操作及现象 | 实验结论 |
| A |  | 向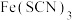 溶液中加入少量铁粉,溶液红色变浅 溶液中加入少量铁粉,溶液红色变浅 | 在其他条件不变时,减小反应物浓度,平衡向逆反应方向移动 |
| B | 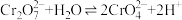 | 向K2Cr2O7溶液中加入少量浓NaOH溶液,溶液变为黄色 | 在其他条件不变时,减小生成物浓度,平衡向正反应方向移动 |
| C |  | 向 的HCOOH中加水稀释,溶液pH增大 的HCOOH中加水稀释,溶液pH增大 | HCOOH是弱酸 |
| D | 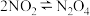 | 将装有NO2与N2O4混合气体的针管活塞外拉,针管内气体颜色先变浅又逐渐变深 | 对有气体参与的可逆反应,在其他条件不变时,减小压强,平衡向气体体积增大的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 下列实验探究方案不能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向 溶液滴加4滴 溶液滴加4滴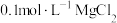 溶液,再滴加4滴 溶液,再滴加4滴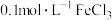 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 | 比较 和 和 的 的 |
| B | 向盛有 水溶液的试管中滴加几滴品红溶液,振荡,观察溶液颜色变化 水溶液的试管中滴加几滴品红溶液,振荡,观察溶液颜色变化 |  具有漂白性 具有漂白性 |
| C | 酸性 溶液中滴加乙醇至过量,观察溶液颜色变化 溶液中滴加乙醇至过量,观察溶液颜色变化 | 乙醇具有还原性 |
| D | 向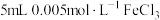 溶液中加入 溶液中加入 溶液,再滴加5滴 溶液,再滴加5滴 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 | 浓度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 下列实验对应的现象和结论都正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向某无色溶液中加入稀盐酸 | 生成的无色气体能使品红褪色 | 该无色溶液中一定存在 |
| B | 向食品脱氧剂样品(含还原铁粉)中加入硫酸后滴加酸性KMnO4溶液 | 紫红色褪去 | 食品脱氧剂样品中含Fe2+ |
| C | 一定温度下,向某容器中充入HI气体,一段时间后压缩容器体积为原来的一半 | 气体颜色变深 | 气体压强增大使平衡正向移动 |
| D | 将溴乙烷与氢氧化钠的醇溶液共热,产生的气体先通入蒸馏水后再通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液的紫红色褪去 | 溴乙烷发生消去反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 恒温密闭容器中发生反应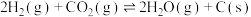 ,下列说法正确的是
,下列说法正确的是
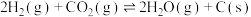 ,下列说法正确的是
,下列说法正确的是A.不同条件下,分别测得ν(H2)=1.5mol·L-1·s-1,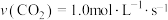 ,则前者反应速率较大 ,则前者反应速率较大 |
| B.向达到平衡后的容器中加入碳,可促使平衡向逆方向移动 |
| C.达到平衡后压缩容器体积,可促使平衡向正方向移动,逆反应速率减小 |
| D.恒容条件下达到平衡后充入水蒸气,该反应的平衡常数不变 |
您最近一年使用:0次
名校
9 . 在密闭容器中,反应
 ,达到如下图甲平衡,在仅改变某一条件后达到乙平衡,对改变的条件下列分析正确的是
,达到如下图甲平衡,在仅改变某一条件后达到乙平衡,对改变的条件下列分析正确的是
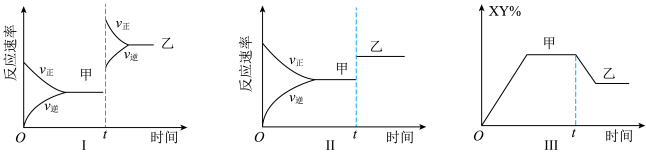

 ,达到如下图甲平衡,在仅改变某一条件后达到乙平衡,对改变的条件下列分析正确的是
,达到如下图甲平衡,在仅改变某一条件后达到乙平衡,对改变的条件下列分析正确的是
| A.图Ⅰ是增大反应物的浓度 |
| B.图Ⅱ一定是加入催化剂的变化情况 |
| C.图Ⅲ是增大压强 |
| D.图Ⅲ是升高温度 |
您最近一年使用:0次
2023-05-07更新
|
605次组卷
|
3卷引用:广西玉林市博白县中学2022-2023学年高二下学期期中段考化学试题
广西玉林市博白县中学2022-2023学年高二下学期期中段考化学试题广西武鸣高中、北流高中、容县高中、博白县中学、玉林一中、玉林实验中学等八校联考2022-2023学年高二下学期期中测试化学试题(已下线)实验03 探究外界条件对化学平衡移动的影响-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)
10 . 氨在国民经济中占有重要地位。
(1)NH3的电子式为_____ 。
(2)实验室中制取氨气的化学方程式为_____ ,生成的气体可以用蘸有浓盐酸的玻璃棒来检验,将产物溶于水,溶液呈酸性,用离子方程式表示原因_____ ;溶液中离子浓度由大到小的顺序为_____ 。
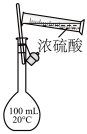
(3)欲快速制取氨气,可将浓氨水滴入固体氢氧化钠中,其装置如图,请结合化学用语从化学平衡的角度解释:_____ 。

(4)将SO2气体通入氯化钡溶液,未见有沉淀生成,继续通入NH3,则出现白色沉淀,请写出反应的离子方程式_____ ;若将SO2气体通入酸化的硝酸钡溶液,也产生白色沉淀,用离子方程式加以说明_____ 。
(5)氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。肼--空气燃料电池是一种碱性电池,该电池放电时,负极的反应式_____ 。
(6)氮氧化物的排放会对空气造成污染,利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3。写出氧化吸收法除去氮氧化物的化学方程式_____ 。
(1)NH3的电子式为
(2)实验室中制取氨气的化学方程式为
(3)欲快速制取氨气,可将浓氨水滴入固体氢氧化钠中,其装置如图,请结合化学用语从化学平衡的角度解释:

(4)将SO2气体通入氯化钡溶液,未见有沉淀生成,继续通入NH3,则出现白色沉淀,请写出反应的离子方程式
(5)氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。肼--空气燃料电池是一种碱性电池,该电池放电时,负极的反应式
(6)氮氧化物的排放会对空气造成污染,利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3。写出氧化吸收法除去氮氧化物的化学方程式
您最近一年使用:0次


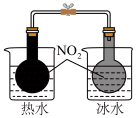 (热水浴气体颜色较深,冰水浴气体颜色较浅)
(热水浴气体颜色较深,冰水浴气体颜色较浅)

