名校
1 . 下列有关实验探究方案设计合理的是
| 选项 | 实验方案 | 实验目的 |
| A | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4和FeCl3溶液,观察气体产生的速率 | 比较Cu2+和Fe3+的催化效果 |
| B | 先将注射器充满NO2气体,然后将活塞往里推,压缩体积,观察注射器内气体颜色先变深后变浅 | 验证压强对平衡的影响 |
| C | 在锥形瓶内各盛有2g锌粒(颗粒大小基本相同),然后通过分液漏斗分别加入40mL1mol·L-1和40mL18mol·L-1的硫酸,比较两者收集10mL氢气所用的时间
| 探究硫酸浓度对反应速率的影响 |
| D | 在 平衡体系中加入KCl晶体,观察并比较实验现象 平衡体系中加入KCl晶体,观察并比较实验现象 | 探究离子浓度对平衡移动的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 在2L恒容密闭容器中充入2mol X和1mol Y发生反应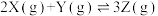
 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断错误的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断错误的是

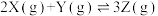
 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断错误的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断错误的是
| A.Q点时,Y的转化率最大 |
| B.W点X的正反应速率小于M点X的正反应速率 |
| C.升高温度,平衡向左移动,平衡常数减小 |
| D.平衡时充入Y,达到新平衡时Y的转化率比原平衡时大 |
您最近半年使用:0次
3 . 下列事实不能 用勒夏特列原理来解释的是
| A.实验室中常用排饱和食盐水的方法收集Cl2 |
| B.鼓入过量空气有利于SO2转化为SO3 |
| C.开启啤酒瓶后,压强变小,瓶中立刻泛起大量泡沫 |
| D.煅烧硫铁矿时先将矿石粉碎 |
您最近半年使用:0次
名校
4 . 下述反应可制备特种陶瓷的原料MgO:MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
 MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是| A.恒温时,增大压强平衡逆向移动,平衡常数减小 |
| B.容积不变时,升高温度,混合气体的平均相对分子质量减小 |
| C.恒温恒容时,分离出部分CO2气体可提高MgSO4的转化率 |
D.恒温恒容时,冲入CO气体,达到新平衡时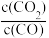 增大 增大 |
您最近半年使用:0次
5 . 下列说法正确的是
A. 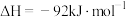 ,升温加快反应速率,平衡往正向移动 ,升温加快反应速率,平衡往正向移动 |
B. ,平衡体系加压后颜色变深 ,平衡体系加压后颜色变深 |
C.恒温恒压下,向 平衡体系中充入氦气,平衡往正向移动 平衡体系中充入氦气,平衡往正向移动 |
D. ,平衡体系中水加稀释,平衡往正向移动 ,平衡体系中水加稀释,平衡往正向移动 |
您最近半年使用:0次
名校
6 . 在常温常压下,向 溶液中滴入
溶液中滴入 的
的 溶液,发生如下反应:
溶液,发生如下反应: 所得溶液显红色,改变下列条件,能使溶液颜色变浅的是
所得溶液显红色,改变下列条件,能使溶液颜色变浅的是
 溶液中滴入
溶液中滴入 的
的 溶液,发生如下反应:
溶液,发生如下反应: 所得溶液显红色,改变下列条件,能使溶液颜色变浅的是
所得溶液显红色,改变下列条件,能使溶液颜色变浅的是A.向溶液中加入少量的 晶体 晶体 | B.向溶液中加入少量的水 |
| C.设法移走溶液中的部分水 | D.向溶液中滴加2滴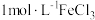 溶液 溶液 |
您最近半年使用:0次
2024-03-02更新
|
60次组卷
|
2卷引用:福建省福州第一中学2023-2024学年高二上学期第二学段考试(期末)化学试题
7 . 侯氏制碱法中,下列操作与回收母液中 无关的是
无关的是
 无关的是
无关的是A.通入 | B.通入 | C.降低温度 | D.添加 |
您最近半年使用:0次
8 . 化学与生活密切相关,下列说法正确的是
A.一氧化碳与血红蛋白 存在反应: 存在反应: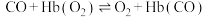 ,当 ,当 中毒时,平衡向右移动,使人体组织局部氧气浓度过高而中毒 中毒时,平衡向右移动,使人体组织局部氧气浓度过高而中毒 |
| B.海轮的外壳附上一些锌块,是利用了电解原理的牺牲阳极的阴极保护法 |
C.汽车尾气治理原理为: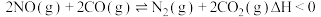 ,由于需要借助催化转化器,因此推断该反应在常温下不能自发反应 ,由于需要借助催化转化器,因此推断该反应在常温下不能自发反应 |
| D.比色分析法可用于某些化学反应速率测定,是利用有色物质浓度与溶液颜色的关系 |
您最近半年使用:0次
名校
9 . 下列事实能用勒夏特列原理来解释的是
A. 被氧化为 被氧化为 ,往往需要使用催化剂: ,往往需要使用催化剂: |
B.500℃温度比室温更有利于合成氨反应:  |
C. 、 、 、 、 平衡混合气体加压后颜色加深: 平衡混合气体加压后颜色加深: |
D.实验室采用排饱和食盐水的方法收集氯气: |
您最近半年使用:0次
名校
10 . 下列实验方法、操作均正确,且能达到实验目的的是
| 选项 | 实验目的 | 实验方法或操作 |
| A | 测定中和反应反应热 | 用简易量热器测量浓硫酸与NaOH溶液反应前后的温度 |
| B | 探究温度对化学平衡的影响 | 将NO2球分别浸泡在冷水和热水中,观察溶液颜色变化 |
| C | 探究压强对化学反应平衡移动的影响 | 容器中反应H2(g) + I2(g)  2HI(g)达平衡时,将容器压缩为原体积的 2HI(g)达平衡时,将容器压缩为原体积的 ,观察颜色变化 ,观察颜色变化 |
| D | 探究浓度对化学反应速率的影响 | 量取同体积不同浓度的盐酸,分别加入等体积、等浓度的NaOH溶液,对比现象 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-12-29更新
|
96次组卷
|
2卷引用:福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题




