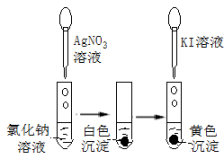
下列有关实验探究方案设计合理的是
| 选项 | 实验方案 | 实验目的 |
| A | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4和FeCl3溶液,观察气体产生的速率 | 比较Cu2+和Fe3+的催化效果 |
| B | 先将注射器充满NO2气体,然后将活塞往里推,压缩体积,观察注射器内气体颜色先变深后变浅 | 验证压强对平衡的影响 |
| C | 在锥形瓶内各盛有2g锌粒(颗粒大小基本相同),然后通过分液漏斗分别加入40mL1mol·L-1和40mL18mol·L-1的硫酸,比较两者收集10mL氢气所用的时间
| 探究硫酸浓度对反应速率的影响 |
| D | 在 平衡体系中加入KCl晶体,观察并比较实验现象 平衡体系中加入KCl晶体,观察并比较实验现象 | 探究离子浓度对平衡移动的影响 |
| A.A | B.B | C.C | D.D |
更新时间:2024-04-22 10:01:34
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】将纯净的A置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:A(s) 2B(g)+C(g)+D(g)。下列说法正确的是
2B(g)+C(g)+D(g)。下列说法正确的是
 2B(g)+C(g)+D(g)。下列说法正确的是
2B(g)+C(g)+D(g)。下列说法正确的是| A.2v(B)=v(C) |
| B.增大A的物质的量,化学反应速率加快 |
| C.若B的质量分数不变,则反应达平衡 |
| D.平衡后移除C,A的转化率增大 |
您最近半年使用:0次
【推荐2】下列实验方案中,设计正确的是
| A.用蒸馏的方法分离汽油和水的混合物 |
B.用焰色反应鉴别KCl和 溶液 溶液 |
C.用NaOH溶液和蓝色石蕊试纸检验溶液中是否存在 |
D.其他条件相同时,分别向等体积的不同浓度的 溶液中加入等量 溶液中加入等量 ,探究浓度对 ,探究浓度对 分解快慢的影响 分解快慢的影响 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 证明Mg(OH)2沉淀可以转化为Fe(OH)3 | 向2mL1mol·L-1NaOH溶液中先加入3滴1mol·L-1 MgCl2溶液,再加入3滴1mol·L-1FeCl3溶液 |
| B | 探究浓度对反应速率的影响 | 相同条件下,向2支各盛有4mL0.01mol·L-1酸性KMnO4溶液的试管中,分别加入2mL0.1mol·L-1H2C2O4溶液和2mL 0.2mol·L-1 H2C2O4溶液,记录溶液褪色所需的时间 |
| C | 测定未知浓度的NaOH溶液 | 用标准盐酸溶液滴定NaOH溶液,用甲基橙作指示剂,当溶液颜色由黄色变为红色即为滴定终点 |
| D | 比较HClO和H2CO3的酸性强弱 | 常温下,用pH试纸分别测定浓度均为0.1 mol·L-1的NaClO溶液和NaHCO3溶液的pH |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确且能用勒夏特列原理解释的是
A.对于反应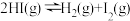 ,达到平衡后,缩小容器的体积可使体系颜色变深 ,达到平衡后,缩小容器的体积可使体系颜色变深 |
B.向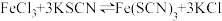 平衡体系中加入少量 平衡体系中加入少量 固体,平衡逆向移动,溶液红色颜色变浅 固体,平衡逆向移动,溶液红色颜色变浅 |
C.重铬酸钾溶液中滴加 溶液,溶液由橙色变黄色【重铬酸钾溶液中存在: 溶液,溶液由橙色变黄色【重铬酸钾溶液中存在: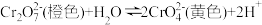 】 】 |
D.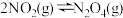 平衡体系,压缩容器的体积,平衡正向移动,最终体系颜色变浅 平衡体系,压缩容器的体积,平衡正向移动,最终体系颜色变浅 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某实验小组同学做电解CuCl2溶液实验,发现电解后 (电极未从溶液中取出)阴极上析出的铜会消失。为探究铜“消失”的原因,该小组同学用不同电解质溶液(足量)、在相同时间内进行如下实验。
已知:① ②
② (无色)③
(无色)③ ;黄色
;黄色
下列分析不正确 的是
| 装置 |
| |
| 序号 | 电解质溶液 | 实验现象(电解后) |
| I |  溶液 溶液 | 溶液仍呈蓝色,附着的铜层无明显变化 |
| II | 稀 溶液 溶液 | 溶液由蓝色开始变为浅黄绿色,2min后溶液变浑浊 |
| III | 浓 溶液 溶液 | 溶液由绿色逐渐变为深黄绿色(略黑),附着的铜层变薄 |
 ②
② (无色)③
(无色)③ ;黄色
;黄色下列分析
A.电解后 溶液的 溶液的 减小,原因是 减小,原因是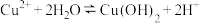 |
B.浓 溶液呈绿色原因是 溶液呈绿色原因是 增大, 增大,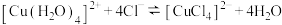 平衡正向移动 平衡正向移动 |
C.II中溶液变浑浊,推测难溶物为 |
D.III中溶液变为深黄绿色,推测原因是 ,溶液中 ,溶液中 增大 增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实与对应的方程式不相符的是
| A.已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH<0,灼热的铂丝与NH3、O2混合气接触,铂丝继续保持红热 |
B.已知:2NO2(g)(红棕色) N2O4(g)(无色) ΔH<0,将“NO2球”浸泡在冷水中,颜色变深 N2O4(g)(无色) ΔH<0,将“NO2球”浸泡在冷水中,颜色变深 |
| C.因H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,故向含0.1molHCl的盐酸中加入4.0gNaOH固体,放出的热量大于5.73kJ |
| D.甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3kJ·mol-1,则甲烷的燃烧热为890.3kJ·mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在恒压、NO和O2的起始浓度一定的条件下, 催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是


| A.反应2NO(g)+O2(g)⇌2NO2(g)的△H<0 |
| B.图中X点所示条件下,延长反应时间能提高NO转化率 |
| C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率 |
| D.实线部分先增大后减小的主要原因是:随着温度升高,平衡先向右移动,然后再向左移动 |
您最近半年使用:0次



 + D2O
+ D2O +2H+
+2H+  +H2O
+H2O