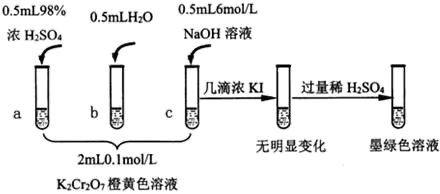
1 . 研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验:
已知:
资料1: (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+ ∆H=+13.8kJ/mol;
(黄色)+2H+ ∆H=+13.8kJ/mol;
资料2:+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
(1)试管c和b对比,推测试管c的现象是_______ 。
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?____ (填“是”或“否”),理由是____ 。
(3)对比试管a、b、c的实验现象,可知pH值减小时,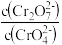
____ (填“增大”,“减小”,“不变”)。
(4)试管c继续滴加KI溶液、过量稀H2SO4,写出此过程中氧化还原反应的离子方程式____ 。

已知:
资料1:
 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+ ∆H=+13.8kJ/mol;
(黄色)+2H+ ∆H=+13.8kJ/mol;资料2:+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
(1)试管c和b对比,推测试管c的现象是
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?
(3)对比试管a、b、c的实验现象,可知pH值减小时,
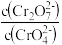
(4)试管c继续滴加KI溶液、过量稀H2SO4,写出此过程中氧化还原反应的离子方程式
您最近一年使用:0次
名校
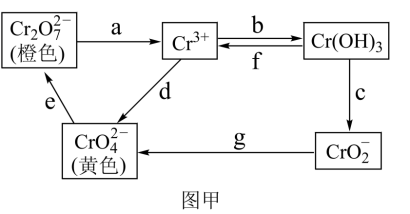
2 . 铬是不锈钢中一种重要的元素,铬的毒性与其存在的价态有关,低价铬对人体基本无害,六价铬比三价铬毒性高100倍,并易被人体吸收且在体内蓄积,有关含铬化合物的相互转化关系如图甲。
回答下列问题:
(1)从图甲中信息判断,Cr(OH)3是___________ 氢氧化物(填“酸性”、“碱性”或“两性”),相关反应的离子方程式为___________ 。
(2)图甲中所示转化过程中需要加入氧化剂的是___________ (填写表示转化过程的小写字母)。
(3)在水溶液中橙色的 与黄色的
与黄色的 有下列平衡关系:
有下列平衡关系: +H2O
+H2O 2
2 +2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是
+2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是___________ 。
(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率( )随温度的变化如图乙所示。
)随温度的变化如图乙所示。
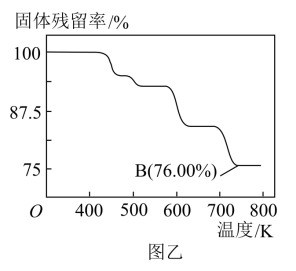
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是___________ 。
②图乙中B点所示固体的化学式是___________ 。

回答下列问题:
(1)从图甲中信息判断,Cr(OH)3是
(2)图甲中所示转化过程中需要加入氧化剂的是
(3)在水溶液中橙色的
 与黄色的
与黄色的 有下列平衡关系:
有下列平衡关系: +H2O
+H2O 2
2 +2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是
+2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率(
 )随温度的变化如图乙所示。
)随温度的变化如图乙所示。
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是
②图乙中B点所示固体的化学式是
您最近一年使用:0次
名校
3 . 某小组同学用乙醛进行银镜反应实验时,补充做了以下实验。已知: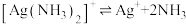
实验①: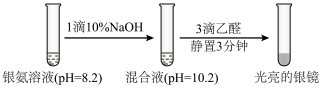
实验②: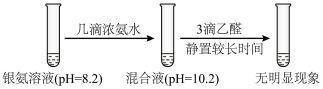
下列关于该实验的分析不正确的是
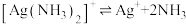
实验①:

实验②:

下列关于该实验的分析不正确的是
| A.实验①无需加热,说明碱性条件有利于银氨溶液与乙醛的反应 |
| B.实验①中加入NaOH后,溶液中c(NH3)增大 |
| C.实验表明,相同pH条件下,不同存在形式的Ag(I)的氧化性不一样 |
| D.对比实验①和②知,形成[Ag(NH3)2]+后Ag(I)氧化性降低 |
您最近一年使用:0次
名校
解题方法
4 . 研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如图实验: (aq)(橙色)+H2O(l)
(aq)(橙色)+H2O(l) 2CrO
2CrO (aq)(黄色)+2H+(aq)△H1=+13.8kJ•mol-1
(aq)(黄色)+2H+(aq)△H1=+13.8kJ•mol-1
②+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为墨绿色。
(1)对比试管c和b,推测试管c的现象是:__ 。
(2)对比试管a和b,发现a中溶液橙色比b的更深,请用平衡移动理论分析原因:____ 。
(3)对比试管a、b、c的实验现象,若pH增大,则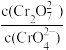
__ (选填“增大”,“减小”,“不变”);
(4)分析如图试管c中滴加KI溶液无明显现象、继续滴加过量稀H2SO4溶液变成墨绿色,由此实验现象,说明+6价铬盐氧化性强弱为Cr2O
____ CrO (填“大于”,“小于”,“不确定”);
(填“大于”,“小于”,“不确定”);
(5)电解法处理:工业上处理含Cr2O 离子的酸性废水,用石墨为电极进行电解,将Cr2O
离子的酸性废水,用石墨为电极进行电解,将Cr2O 离子还原为可溶性Cr3+。则Cr2O
离子还原为可溶性Cr3+。则Cr2O 离子在
离子在___ 极(填“阴”或“阳”)放电,写出Cr2O 放电的电极反应式
放电的电极反应式___ 。

 (aq)(橙色)+H2O(l)
(aq)(橙色)+H2O(l) 2CrO
2CrO (aq)(黄色)+2H+(aq)△H1=+13.8kJ•mol-1
(aq)(黄色)+2H+(aq)△H1=+13.8kJ•mol-1②+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为墨绿色。
(1)对比试管c和b,推测试管c的现象是:
(2)对比试管a和b,发现a中溶液橙色比b的更深,请用平衡移动理论分析原因:
(3)对比试管a、b、c的实验现象,若pH增大,则
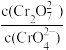
(4)分析如图试管c中滴加KI溶液无明显现象、继续滴加过量稀H2SO4溶液变成墨绿色,由此实验现象,说明+6价铬盐氧化性强弱为Cr2O

 (填“大于”,“小于”,“不确定”);
(填“大于”,“小于”,“不确定”);(5)电解法处理:工业上处理含Cr2O
 离子的酸性废水,用石墨为电极进行电解,将Cr2O
离子的酸性废水,用石墨为电极进行电解,将Cr2O 离子还原为可溶性Cr3+。则Cr2O
离子还原为可溶性Cr3+。则Cr2O 离子在
离子在 放电的电极反应式
放电的电极反应式
您最近一年使用:0次
2020-12-08更新
|
107次组卷
|
2卷引用:福建省宁德市高中同心顺联盟校2020-2021学年高二上学期期中考试化学试题
5 . 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+ O2 (g)  2SO3(g) △H< 0。查阅资料知:SO3熔点16.83℃,沸点44.8℃。
2SO3(g) △H< 0。查阅资料知:SO3熔点16.83℃,沸点44.8℃。
(1)600℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,反应过程中SO2,O2,SO3物质的量变化如图。

①据图判断,该反应处于平衡状态的时间是_______ 。
②计算600℃下,该反应的化学平衡常数 K=_______ 。
③据图判断,反应进行至20 min时,曲线发生变化的原因是________________ (用文字表达)。
(2)某化学研究学习小组用下图的装置组装设计了一个实验,以测定SO2转化为SO3的转化率,仪器的连接顺序是a→h→i→b→c→f→g→d→e。

①为提高SO2的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是____ 。
②在Ⅰ处用大火加热烧瓶时SO2的转化率会_______ 。(选填“增大”“不变”或“减小”)
③用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为_____________ 。
 2SO3(g) △H< 0。查阅资料知:SO3熔点16.83℃,沸点44.8℃。
2SO3(g) △H< 0。查阅资料知:SO3熔点16.83℃,沸点44.8℃。(1)600℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,反应过程中SO2,O2,SO3物质的量变化如图。

①据图判断,该反应处于平衡状态的时间是
②计算600℃下,该反应的化学平衡常数 K=
③据图判断,反应进行至20 min时,曲线发生变化的原因是
(2)某化学研究学习小组用下图的装置组装设计了一个实验,以测定SO2转化为SO3的转化率,仪器的连接顺序是a→h→i→b→c→f→g→d→e。

①为提高SO2的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是
②在Ⅰ处用大火加热烧瓶时SO2的转化率会
③用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为
您最近一年使用:0次
6 . 已知:重铬酸钾( )具有强氧化性,其还原产物
)具有强氧化性,其还原产物 在水溶液中呈绿色。在
在水溶液中呈绿色。在 溶液中存在下列平衡:
溶液中存在下列平衡: (橙色)
(橙色) (黄色)
(黄色) 。用
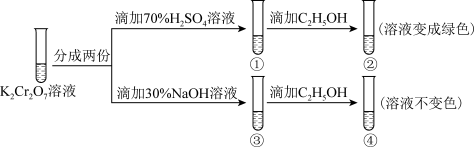
。用 溶液进行如图所示实验,下列说法不正确的是
溶液进行如图所示实验,下列说法不正确的是
 )具有强氧化性,其还原产物
)具有强氧化性,其还原产物 在水溶液中呈绿色。在
在水溶液中呈绿色。在 溶液中存在下列平衡:
溶液中存在下列平衡: (橙色)
(橙色) (黄色)
(黄色) 。用
。用 溶液进行如图所示实验,下列说法不正确的是
溶液进行如图所示实验,下列说法不正确的是
| A.①中溶液橙色加深,③中溶液变为黄色 |
B.②中 被 被 还原 还原 |
C.对比②和④可知, 酸性溶液氧化性强 酸性溶液氧化性强 |
D.若向④中加入70% 溶液至过量,溶液变为橙色 溶液至过量,溶液变为橙色 |
您最近一年使用:0次
2022-09-04更新
|
844次组卷
|
91卷引用:福建省福州市第八中学2016-2017学年高二下学期期中考试化学试题
福建省福州市第八中学2016-2017学年高二下学期期中考试化学试题福建省厦门市湖滨中学2019届高三上学期第一次阶段检测化学试题福建省莆田市仙游县枫亭中学2019-2020学年高二上学期期末考试化学试题2016年全国普通高等学校招生统一考试化学(北京卷精编版)2017届河北省沧州市第一中学高三上周测化学试卷2017届河南省开封市高三上学期10月定位考试化学试卷2017届江西省鹰潭市第一中学高三上学期第四次月考化学试卷2016-2017学年辽宁东北育才学校高二上阶段考二化学卷2017届宁夏固原一中高三上适应性训练四化学卷2017届河北省冀州中学高三(高复班)上学期一轮检测(二)化学试卷安徽省淮北市第一中学2016-2017学年高二下学期期中考试化学试题辽宁省葫芦岛市2017届高三第二次模拟考试(5月)化学试题山东省泰安市第一中学2016-2017学年高一下学期学情检测化学试题黑龙江省哈尔滨市第六中学2016-2017学年高二6月月考化学试题辽宁省辽源市金鼎高级中学2016-2017学年高二上学期期末考试化学试卷2018版化学(苏教版)高考总复习对接高考精练--氧化还原反应基础黑龙江省哈尔滨市第六中学2018届高三9月阶段检测化学试题辽宁省大连育明高级中学2018届高三人教版选修四同步测试化学试题河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第一次月考化学试题吉林省实验中学2018届高三上学期第二次月考化学试题吉林省长春市2018届高三上学期第二次月考化学试题北京市八一中学2016-2017学年高二上学期期中考试化学试题湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题(实验班)内蒙古巴彦淖尔市第一中学2018届高三12月月考理科综合化学试题江西省抚州市临川区第一中学2017-2018学年高二12月月考化学试题(已下线)学科网2019年高考化学一轮复习讲练测2.3 氧化还原反应的基本概念 练陕西省渭南市尚德中学2019届高三上学期第一次教学质量检测化学试题山西省运城市河津二中2018-2019学年高二上学期9月月考化学试题【全国百强校】四川省彭州中学2018-2019学年高二上学期10月月考化学试题浙江省诸暨中学2018-2019学年高二上学期10月(期中)阶段性考试实验班化学试题【全国百强校】湖南省衡阳市第一中学2018-2019学年高二上学期期中考试化学试题(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)2016年全国普通高等学校招生统一考试化学(北京卷参考版)云南省腾冲市第八中学2018-2019学年高二下学期期中考试化学试题河北省迁西县第一中学2019-2020学年高二10月月考化学试题河北省鹿泉第一中学2019-2020学年高二9月月考化学试题浙江省宁波市北仑中学2019-2020学年高二上学期期中考试化学(2-10班)试题湖北省沙市中学2019-2020学年高二上学期期中考试化学(选考)试题河北省张家口市第一中学2019-2020学年高二12月月考化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的综合分析夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用夯基提能2020届高三化学选择题对题专练——氧化还原反应(强化练习)夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 化学平衡移动及其影响因素(强化练习)专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升山西省临汾市2020届高三上学期第二次月考化学试题河北省保定市2019-2020学年高二上学期期末调研考试化学试题(已下线)专题四 氧化还原反应(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)专题十一 化学反应速率和化学平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训河北省衡水中学2020届高三四月份质量监测理综化学试题湖南长沙长郡中学2020届高三2月份网络教学质量监测卷理综化学试题湖北省武汉市华中师范大学第一附属中学2020届高三2月份网络教学质量监测理综化学试题吉林省长春市东北师大附中2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分山西省运城市新绛中学2021届高三上学期8月月考化学试题河北省衡水市桃城区第十四中学2021届高三上学期一调考试化学试题四川省宜宾翠屏棠湖学校2020-2021学年高二上学期10月月考化学试题山西省太原市第五中学2020-2021学年高二上学期10月月考试题湖南省常德外国语学校2020-2021学年高二上学期期中考试化学试题重庆市第一中学校2020-2021高三上学期第一次月考化学试题北京首都师范大学第二附属中学2021届高三9月月考化学试题山西省太原市2020-2021学年高二上学期期中质量监测化学(理)试题广东实验中学附属天河学校2020--2021学年高二上学期期中考试化学试题四川省成都市金堂县竹篙中学2020-2021学年高二10月月考化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研化学试题上海市嘉定区2021届高三一模化学试题安徽省六安市城南中学2020-2021学年高二上学期期中考试化学试题广东省汕尾市2020-2021学年高二上学期期末学业质量监测化学试题河北省衡水市第十四中学2020-2021学年高二上学期期末考试化学试题广东省韶关市2021届高三综合测试化学试题(已下线)考点32 化学反应条件的控制-备战2022年高考化学一轮复习考点帮(浙江专用)广东省深圳市西乡中学2021-2022学年高二上学期期中考试化学试题上海市徐汇中学2021-2022学年高三上学期期中考试化学试题(已下线)专题05 氧化还原反应-2022年高考化学二轮复习重点专题常考点突破练湖南省株洲市九方中学2022届高三下学期4月月考化学试题第二节 化学平衡 第3课时 影响化学平衡的因素内蒙古包头市第四中学2020-2021学年高二上学期期中考试化学试题黑龙江省哈尔滨市第二十四中学2022-2023学年高二10月月考化学试题新疆维吾尔自治区喀什市喀什第二中学2022-2023学年高三上学期网上11月月考化学试题广东省中山市小榄中学2022-2023学年高三上学期第三次月考化学试题(已下线)专题四 氧化还原反应-实战高考·二轮复习核心突破(已下线)化学预测卷(六)-预测卷(浙江专版)(已下线)化学反应速率与化学平衡——课时5影响化学平衡的因素四川省资阳中学2022-2023学年高二上学期期末考试化学试题(已下线)T13-实验方案的设计与评价(已下线)考点04 氧化还原反应的基本概念和规律(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)四川省绵阳市南山中学实验学校2022-2023学年高二下学期3月月考化学试题广东省肇庆市封开县广信中学、四会中学2023-2024学年高二上学期第一次联考化学试题北京市第一○一中学2023-2024学年高二上学期统练一化学试题北京市首都师范大学附属中学2022-2023学年高三上学期开学测试化学试题北京市日坛中学2023-2024学年高三上学期10月检测化学试题云南省大理市下关第一中学2023-2024学年高二上学期11月期中考试化学试题
7 . 处理工业废水中 和
和 的工艺流程如下:
的工艺流程如下:

已知:(1)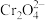 (黄色),
(黄色), (橙色)
(橙色)
(2)常温下, 的溶度积
的溶度积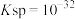
下列说法错误的是
 和
和 的工艺流程如下:
的工艺流程如下:
已知:(1)
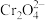 (黄色),
(黄色), (橙色)
(橙色)(2)常温下,
 的溶度积
的溶度积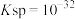
下列说法错误的是
A.第①步存在平衡: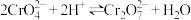 |
B.常温下,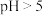 时 时 沉淀完全 沉淀完全 |
C.第②步能说明氧化性: |
D.稀释 溶液时,溶液中各离子浓度均减小 溶液时,溶液中各离子浓度均减小 |
您最近一年使用:0次
2022-01-21更新
|
368次组卷
|
4卷引用:福建省莆田第一中学2021-2022学年高二下学期期中考试化学试题
福建省莆田第一中学2021-2022学年高二下学期期中考试化学试题湖南省长沙市2021-2022学年高三新高考适应性考试化学试题(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)(已下线)题型7 氧化还原反应原理在实际生产中的应用
8 . 粉煤灰是燃煤产生的重要污染物,主要成分有A12O3、Fe2O3、Fe3O4和SiO2等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米Fe2O3等重要物质。

已知:i伯胺R-NH2能与Fe3+反应:3R-NH2+Fe3++SO42-+H2O Fe(NH2-R)(OH)SO4+H+生成易溶于煤油的产物。
Fe(NH2-R)(OH)SO4+H+生成易溶于煤油的产物。
ii Fe3+在水溶液中能与Cl-反应:Fe3++6Cl-⇌[FeCl6]3-
(1)写出过程I中Fe2O3发生反应的离子方程式:____ 。
(2)过程II加入过量H2O2的作用是___ 。
(3)过程II加入伯胺一煤油对浸取液进行分离,该操作的名称是_____ 。
(4)从化学平衡角度解释过程III利用NaCI溶液进行反萃取的原理:_____ 。
(5) N2H4具有碱性,可与H+结合生成N2H5+。过程IV中先用过量的N2H4将水层2中Fe3+转化为Fe2+并生成N2,反应的离子方程式为____ ,得到的Fe2+再被O2氧化为FeOOH。
(6)纳米Fe2O3在常压电化学法合成氨过程中起催化作用。该电解装置如图所示。
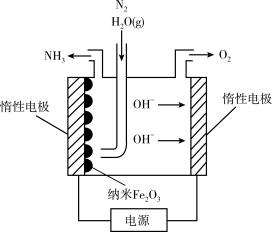
已知熔融NaOH-KOH为电解液,Fe2O3在阴极发生电极反应生成中间体Fe。用化学用语表示Fe2O3在阴极催化生成NH3的反应过程。
第一步:____ ,
第二步:____ 。

已知:i伯胺R-NH2能与Fe3+反应:3R-NH2+Fe3++SO42-+H2O
 Fe(NH2-R)(OH)SO4+H+生成易溶于煤油的产物。
Fe(NH2-R)(OH)SO4+H+生成易溶于煤油的产物。ii Fe3+在水溶液中能与Cl-反应:Fe3++6Cl-⇌[FeCl6]3-
(1)写出过程I中Fe2O3发生反应的离子方程式:
(2)过程II加入过量H2O2的作用是
(3)过程II加入伯胺一煤油对浸取液进行分离,该操作的名称是
(4)从化学平衡角度解释过程III利用NaCI溶液进行反萃取的原理:
(5) N2H4具有碱性,可与H+结合生成N2H5+。过程IV中先用过量的N2H4将水层2中Fe3+转化为Fe2+并生成N2,反应的离子方程式为
(6)纳米Fe2O3在常压电化学法合成氨过程中起催化作用。该电解装置如图所示。

已知熔融NaOH-KOH为电解液,Fe2O3在阴极发生电极反应生成中间体Fe。用化学用语表示Fe2O3在阴极催化生成NH3的反应过程。
第一步:
第二步:
您最近一年使用:0次
2019-06-23更新
|
703次组卷
|
4卷引用:福建省“百校联考”2020届高三7月教学摸底质量检查理科综合化学试题
福建省“百校联考”2020届高三7月教学摸底质量检查理科综合化学试题【区级联考】北京市海淀区2019届高三5月期末练习(二模)理综化学试题江西省丰城中学、高安二中等六校2021届高三1月联考理综化学试题(已下线)大题02 化学工艺流程题(二)-【考前抓大题】备战2021年高考化学(全国通用)



