名校
解题方法
1 . 聚醋酸乙烯酯难溶于水,可用作白乳胶、塑料薄膜和涂料等,用它可得到聚乙烯醇,聚乙烯醇水溶液可用作医用滴眼液。合成路线如下:
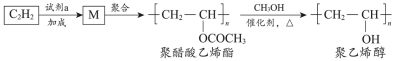
已知: (R’、
(R’、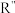 不同的羟基)
不同的羟基)
下列说法不正确 的是

已知:
 (R’、
(R’、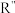 不同的羟基)
不同的羟基)下列说法
| A.试剂a是乙酸 |
| B.通过增加甲醇用量可提高聚乙烯醇的产率 |
| C.由M转化为聚醋酸乙烯酯的过程中发生了缩聚反应 |
| D.由聚醋酸乙烯酯转化为聚乙烯醇过程中还会生成乙酸甲酯 |
您最近一年使用:0次
名校
2 . 氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
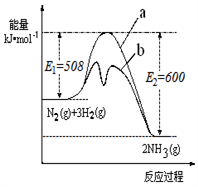
(1)根据下图提供的信息,写出该反应的热化学方程式
_____________________________________________ ,
下图的曲线中____________ (填“a” 或“b”)表示 加入铁触媒(催化剂)的能量变化曲线。
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是_________________ 。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n mol N2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
(4)合成氨的原料气氢气制备时其中一步反应: H2O(g)+CO(g) CO2(g)+H2(g),在850 ℃时,其平衡常数K=1。若850 ℃时向体积为1 L的恒容密闭容器中,同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2,5.0 mol H2,此时反应向
CO2(g)+H2(g),在850 ℃时,其平衡常数K=1。若850 ℃时向体积为1 L的恒容密闭容器中,同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2,5.0 mol H2,此时反应向____________ (填“正反应”或“逆反应”)方向进行,平衡时CO2的物质的量为______________ 。
(1)根据下图提供的信息,写出该反应的热化学方程式
下图的曲线中

(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n mol N2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 | 1/3 | 1 |
ⅱ | 1/3 | 10 | |
ⅲ | 480 | 10 |
(4)合成氨的原料气氢气制备时其中一步反应: H2O(g)+CO(g)
 CO2(g)+H2(g),在850 ℃时,其平衡常数K=1。若850 ℃时向体积为1 L的恒容密闭容器中,同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2,5.0 mol H2,此时反应向
CO2(g)+H2(g),在850 ℃时,其平衡常数K=1。若850 ℃时向体积为1 L的恒容密闭容器中,同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2,5.0 mol H2,此时反应向
您最近一年使用:0次
名校
3 . 气态含氮化合物是把双刃剑,既是固氮的主要途径,也是大气污染物。气态含氮化合物及相关反应是新型科研热点。回答下列问题:
(1)以氨和二氧化碳为原料可合成尿素[CO(NH2)2],反应原理为
 ,利用该反应可以在一定程度上减缓温室效应。向2 L恒容密闭容器中充入3 mol NH3和1 mol CO2,使反应进行,保持温度不变,测得CO2的转化率随时间的变化情况如图所示。
,利用该反应可以在一定程度上减缓温室效应。向2 L恒容密闭容器中充入3 mol NH3和1 mol CO2,使反应进行,保持温度不变,测得CO2的转化率随时间的变化情况如图所示。
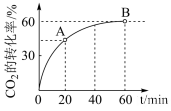
①下列叙述中不能说明该反应达到平衡状态的是_______ (填选项字母)。
A.体系压强不再变化 B.气体密度不再变化
C.气体的体积不再变化 D.NH3的消耗速率和CO2的生成速率之比为2:1
②用CO2的浓度变化表示反应速率,则前20min 反应的平均速率为_______ 。
③按物质的量之比3:1充入NH3和CO2的主要目的是_______ 。
④此温度下,该反应的平衡常数K=_______ (保留2位小数)。
(2)氨不仅应用于化肥生产,也可以应用于能源领域,氨氧燃料电池有性能稳定的独特优势,某研究小组设计的氨氧燃料电池装置如图:

则电极2为_______ 极,电极1的电极反应式为_______ ,A膜为_______ 交换膜 (填 “阳离子”或 “阴离子”)。
(1)以氨和二氧化碳为原料可合成尿素[CO(NH2)2],反应原理为

 ,利用该反应可以在一定程度上减缓温室效应。向2 L恒容密闭容器中充入3 mol NH3和1 mol CO2,使反应进行,保持温度不变,测得CO2的转化率随时间的变化情况如图所示。
,利用该反应可以在一定程度上减缓温室效应。向2 L恒容密闭容器中充入3 mol NH3和1 mol CO2,使反应进行,保持温度不变,测得CO2的转化率随时间的变化情况如图所示。
①下列叙述中不能说明该反应达到平衡状态的是
A.体系压强不再变化 B.气体密度不再变化
C.气体的体积不再变化 D.NH3的消耗速率和CO2的生成速率之比为2:1
②用CO2的浓度变化表示反应速率,则前20min 反应的平均速率为
③按物质的量之比3:1充入NH3和CO2的主要目的是
④此温度下,该反应的平衡常数K=
(2)氨不仅应用于化肥生产,也可以应用于能源领域,氨氧燃料电池有性能稳定的独特优势,某研究小组设计的氨氧燃料电池装置如图:

则电极2为
您最近一年使用:0次
解题方法
4 . 肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料。实验室可用苯甲醛和乙酸酐、醋酸钠等原料经下列反应制取肉桂酸,其中苯甲醛为无色油状液体。已知:
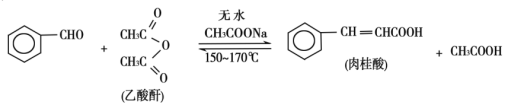
I.合成:反应装置如图所示。向三颈烧瓶中先后加入研细的无水醋酸钠、4.8g苯甲醛和5.6g乙酸酐,振荡使之混合均匀。在150~170℃加热1小时,保持微沸状态。
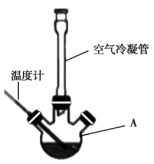
(1)仪器A的名称为____ 。
(2)空气冷凝管的作用是____ ,该装置加热要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是____ 。
(3)不能把无水CH3COONa换成CH3COONa•3H2O的原因是____ 。
II.粗品精制:已知水蒸气蒸馏是分离提纯有机化合物的重要方法之一,在水蒸气蒸馏操作中,水蒸气起到载热体和降低沸点的作用,可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯的目的。
将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
a.在搅拌下,向反应液中加入20mL水
b.再慢慢加入碳酸钠溶液
c.然后进行水蒸气蒸馏
d.待烧瓶内溶液冷却至室温,在搅拌下,加入盐酸酸化,析出大量晶体,过滤,洗涤,干燥。
(4)饱和Na2CO3溶液的作用有____ 。水蒸气蒸馏可除去的杂质是____ ;如何判断蒸馏终点____ 。
(5)若得到的肉桂酸晶体产品不纯,应采用____ 法可得到纯度更高的产品。
(6)若最后得到纯净的肉桂酸5.2g,则该反应中的产率是____ (保留两位有效数字)。

| 苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
| 溶解度(25℃,g/100g水) | 0.3 | 遇水易水解成乙酸 | 0.04 | 互溶 |
| 沸点(℃) | 179.6 | 138.6 | 300 | 118 |
| 相对分子质量 | 106 | 102 | 148 | 60 |

(1)仪器A的名称为
(2)空气冷凝管的作用是
(3)不能把无水CH3COONa换成CH3COONa•3H2O的原因是
II.粗品精制:已知水蒸气蒸馏是分离提纯有机化合物的重要方法之一,在水蒸气蒸馏操作中,水蒸气起到载热体和降低沸点的作用,可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯的目的。
将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
a.在搅拌下,向反应液中加入20mL水
b.再慢慢加入碳酸钠溶液
c.然后进行水蒸气蒸馏
d.待烧瓶内溶液冷却至室温,在搅拌下,加入盐酸酸化,析出大量晶体,过滤,洗涤,干燥。
(4)饱和Na2CO3溶液的作用有
(5)若得到的肉桂酸晶体产品不纯,应采用
(6)若最后得到纯净的肉桂酸5.2g,则该反应中的产率是
您最近一年使用:0次
2022-09-05更新
|
260次组卷
|
2卷引用:山东省泰安市2021-2022学年高二下学期期末考试化学试题
名校
解题方法
5 . 苯甲酸甲酯是重要的化工原料,某化学兴趣小组仿照实验室制乙酸乙酯的原理以苯甲酸和甲醇为原料制备苯甲酸甲酯。有关数据如下:
Ⅰ.合成苯甲酸甲酯粗产品。在圆底烧瓶中加入适量苯甲酸和过量甲醇,再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,在圆底烧瓶上连接冷凝回流装置后,小心加热2小时,得苯甲酸甲酯粗产品。回答下列问题:
(1)该反应的化学方程式为_________ 。
(2)实验中,应选择_______ (填序号)作为冷凝回流装置,该仪器的名称为________ 。__________ 。
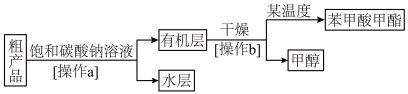
Ⅱ.粗产品的精制。苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用如图流程图进行精制。_________ ,操作b的名称为_______ 。
(5)该实验中制得的甲醇可以在Cu的作用下被氧化为甲醛,方程式为_______ 。
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/( ) ) | 水溶性 | |
| 苯甲酸 | 122 | 122.4 | 249 | 1.2659 | 微溶 |
| 甲醇 | 32 | -97 | 64.6 | 0.792 | 互溶 |
| 苯甲酸甲酯 | 136 | -12.3 | 196.6 | 1.0888 | 不溶 |
Ⅰ.合成苯甲酸甲酯粗产品。在圆底烧瓶中加入适量苯甲酸和过量甲醇,再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,在圆底烧瓶上连接冷凝回流装置后,小心加热2小时,得苯甲酸甲酯粗产品。回答下列问题:
(1)该反应的化学方程式为
(2)实验中,应选择
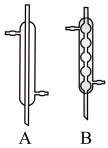
Ⅱ.粗产品的精制。苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用如图流程图进行精制。
(5)该实验中制得的甲醇可以在Cu的作用下被氧化为甲醛,方程式为
您最近一年使用:0次
2020-08-31更新
|
230次组卷
|
2卷引用:山东省枣庄市第三中学2019-2020学年高二下学期期中考试化学试题
名校
6 . 氨是合成硝酸、铵盐和氮肥的基本原料,氮的氧化物是大气的污染物,请问:
(1)氨的水溶液显弱碱性,其原因为___________ (用离子方程式表示),0.1 mol•L-1的氨水中加入少量的NH4Cl固体,溶液的pH ___________ (填“增大”或“减小”);若加入少量的明矾,溶液中的 的浓度
的浓度 ___________ (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为___________ ,平衡常数表达式为___________ ;若有1mol硝酸铵完全分解,转移的电子数为___________ mol。
(3)甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ·mol-1,甲醚可作燃料电池的燃料。已知H2(g)和C(s)的燃烧热分别是285.8 kJ·mol-1、393.5 kJ·mol-1;计算反应4C(s)+ 6H2(g)+ O2(g)=2CH3OCH3(g)的反应热为___________ ;
(4)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+ 2CO2(g) CH3OCH3(g)+ 3H2O(g) △H<0
CH3OCH3(g)+ 3H2O(g) △H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是______ (选填编号,注意大小写)
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将___________ (填“变大”、“变小”或“不变”)。
(1)氨的水溶液显弱碱性,其原因为
 的浓度
的浓度 (2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为
(3)甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ·mol-1,甲醚可作燃料电池的燃料。已知H2(g)和C(s)的燃烧热分别是285.8 kJ·mol-1、393.5 kJ·mol-1;计算反应4C(s)+ 6H2(g)+ O2(g)=2CH3OCH3(g)的反应热为
(4)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+ 2CO2(g)
 CH3OCH3(g)+ 3H2O(g) △H<0
CH3OCH3(g)+ 3H2O(g) △H<0①一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将
您最近一年使用:0次
真题
名校
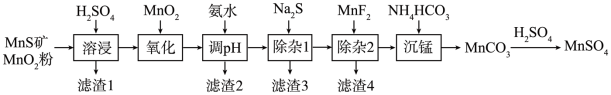
7 . 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
(1)“滤渣1”含有S和__________________________ ;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________ 。
(2)“氧化”中添加适量的MnO2的作用是将________________________ 。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______ ~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________ 。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________ 。
(6)写出“沉锰”的离子方程式___________________________________________________ 。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y= 时,z=
时,z=___________ 。
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和
(2)“氧化”中添加适量的MnO2的作用是将
(3)“调pH”除铁和铝,溶液的pH范围应调节为
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(6)写出“沉锰”的离子方程式
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=
 时,z=
时,z=
您最近一年使用:0次
2019-06-09更新
|
19599次组卷
|
29卷引用:河北省张家口市第四中学2018-2019学年高二下学期6月月考理科综合化学试题
河北省张家口市第四中学2018-2019学年高二下学期6月月考理科综合化学试题 鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三章素养检测2019年全国统一高考化学试题(新课标Ⅲ)河北省辛集中学2020届高三上学期入学考试化学试题安徽省阜阳市颍上二中等三校2020届高三上学期入学考试化学试题甘肃省高台县第一中学2020届高三上学期期中考试化学试题山东省滕州市第一中学2020届高三3月线上模拟考试化学试题(已下线)专题七 工艺流程题(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训河北省承德市围场卉原中学2020届高三模拟自测联考试卷理综化学试卷2020届四川省成都市第七中学高三三月份网络教学质量监测卷化学试题(已下线)专题6.1 无机化工流程题(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升四川省宜宾市叙州区第一中学校2020届高三下学期第四学月考试理综化学试题黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题四川省宜宾市叙州区第二中学校2020届高三第一次高考适应性考试理综化学试题河南省信阳市罗山县2021届高三第一次调研(8月联考)化学试题(已下线)押全国卷理综第27题 工业流程-备战2021年高考化学临考题号押题(课标全国卷)江西省宜春市第九中学2021-2022学年高三上学期10月月考化学试题天津市第二十五中学2021-2022学年高三上学期第一次月考化学试题(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)押全国卷理综第27题 工业流程-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题16工艺流程题-五年(2018~2022)高考真题汇编(全国卷)四川省泸州市泸县第五中学2022届高三高考适应性考试理综化学试题(已下线)专题18 工艺流程题(已下线)T26-工业流程题黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题陕西省西安市周至县第六中学2023-2024学年高三上学期11月期中化学试题河南省济源市高级中学2023-2024学年高三上学期高考模拟检测(10月)理科综合试题-高中化学



