1 . 硫酸是重要的化工原料,它的年产量可以用来衡量一个国家的化工生产水平,以黄铁矿为原
料进行接触法制硫酸的流程如下:___________ (填设备名称)中与氧气反应的方程式,每生成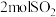 转移
转移___________ mol电子。
(2)在转化阶段,下列条件能使平衡向生成 的方向移动的是_________。
的方向移动的是_________。
(3)硫酸工业生产中 吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收
吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收 所用硫酸的适宜浓度为98.3%,适宜温度为
所用硫酸的适宜浓度为98.3%,适宜温度为___________ ,而工业生产中一般采用60℃的可能原因是___________ 。
料进行接触法制硫酸的流程如下:

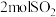 转移
转移(2)在转化阶段,下列条件能使平衡向生成
 的方向移动的是_________。
的方向移动的是_________。| A.不采用常温而加热至400℃-500℃ | B.使用 作为催化剂 作为催化剂 |
| C.向容器中通入过量空气 | D.进入接触室前的混合气体需要先净化 |
(3)硫酸工业生产中
 吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收
吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收 所用硫酸的适宜浓度为98.3%,适宜温度为
所用硫酸的适宜浓度为98.3%,适宜温度为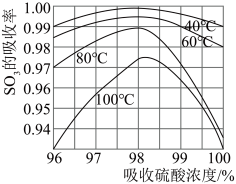
您最近一年使用:0次
名校
2 . Ⅰ.传统的“哈伯法”合成氨原理为: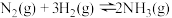
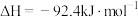
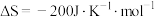
(1)上述反应在常温下___________ (填“能”或“不能”)自发进行。
(2)工业合成氨选择的催化剂是___________ 。
(3)恒温、恒容密闭容器中进行上述反应,一定能说明该反应达到平衡状态的是___________ 。
a. 、
、 、
、 的浓度之比为
的浓度之比为 b.容器内气体压强保持不变
b.容器内气体压强保持不变
c.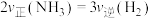 d.混合气体的密度保持不变
d.混合气体的密度保持不变
(4)改变下列条件能加快反应速率,且单位体积内反应物活化分子百分数不变的是___________ 。
a.增大浓度 b.增大压强 c.升高温度 d.使用催化剂
(5)工业合成氨中,下列措施不符合绿色化学理念的是___________ 。
a.将氨气及时液化,分离出反应体系
b.将从反应体系中分离出的 和
和 重新输送到反应器中予以循环利用
重新输送到反应器中予以循环利用
c.氨合成塔中内置热交换器用来预热后续通入的冷的氮气和氢气
d.可采用1000℃的高温使得反应速率更快
Ⅱ.科研小组模拟不同条件下的合成氨反应,向体积可变的密闭容器中充入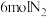 和
和 ,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。
,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。

(6) 、
、 、
、 由小到大的顺序为
由小到大的顺序为___________ 。
(7)在 、
、 条件下,若此时容器体积为
条件下,若此时容器体积为 ,
, 后反应达到平衡,则
后反应达到平衡,则 内
内 的平均反应速率为
的平均反应速率为___________ ,平衡常数
___________ (保留两位有效数字)。
Ⅲ.东南大学王金兰课题组提出合成氨的“表面氢化机理”,在较低的电压下实现氮气的还原合成氨。
已知:第一步: (快)(吸附在催化剂表面的物种用*表示)
(快)(吸附在催化剂表面的物种用*表示)
第二步: (慢)(吸附在催化剂表面)
(慢)(吸附在催化剂表面)
第三步: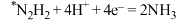 (快)
(快)
(8)较传统工业合成氨法,该方法具有的优点___________ 。
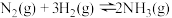
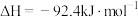
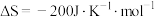
(1)上述反应在常温下
(2)工业合成氨选择的催化剂是
(3)恒温、恒容密闭容器中进行上述反应,一定能说明该反应达到平衡状态的是
a.
 、
、 、
、 的浓度之比为
的浓度之比为 b.容器内气体压强保持不变
b.容器内气体压强保持不变c.
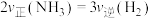 d.混合气体的密度保持不变
d.混合气体的密度保持不变(4)改变下列条件能加快反应速率,且单位体积内反应物活化分子百分数不变的是
a.增大浓度 b.增大压强 c.升高温度 d.使用催化剂
(5)工业合成氨中,下列措施不符合绿色化学理念的是
a.将氨气及时液化,分离出反应体系
b.将从反应体系中分离出的
 和
和 重新输送到反应器中予以循环利用
重新输送到反应器中予以循环利用c.氨合成塔中内置热交换器用来预热后续通入的冷的氮气和氢气
d.可采用1000℃的高温使得反应速率更快
Ⅱ.科研小组模拟不同条件下的合成氨反应,向体积可变的密闭容器中充入
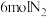 和
和 ,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。
,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。
(6)
 、
、 、
、 由小到大的顺序为
由小到大的顺序为(7)在
 、
、 条件下,若此时容器体积为
条件下,若此时容器体积为 ,
, 后反应达到平衡,则
后反应达到平衡,则 内
内 的平均反应速率为
的平均反应速率为
Ⅲ.东南大学王金兰课题组提出合成氨的“表面氢化机理”,在较低的电压下实现氮气的还原合成氨。
已知:第一步:
 (快)(吸附在催化剂表面的物种用*表示)
(快)(吸附在催化剂表面的物种用*表示)第二步:
 (慢)(吸附在催化剂表面)
(慢)(吸附在催化剂表面)第三步:
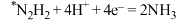 (快)
(快)(8)较传统工业合成氨法,该方法具有的优点
您最近一年使用:0次
3 . CO、NO均能够与血红蛋白(Hb)中Fe2+形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。CO进入血液后有如下平衡: 。
。
(1)C、N、O三种元素,第一电离能由大到小的顺序为___________ 。
(2)在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是___________ 。
(3)高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:___________ 。
 。
。(1)C、N、O三种元素,第一电离能由大到小的顺序为
(2)在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是
(3)高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:
您最近一年使用:0次
名校
解题方法
4 . 1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当时日益增长的人口对粮食的需求。下图是哈伯法的流程图。图中沿X路线到压缩机的物质是
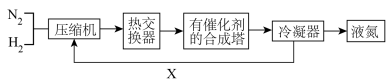

| A.N2和H2 | B.催化剂 | C.N2 | D.H2 |
您最近一年使用:0次
名校
5 . 现代医学证明“痛风”的病因与关节滑液中形成尿酸钠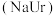 晶体有关,尤其在寒冷季节易诱发关节疼痛。主要原理为:
晶体有关,尤其在寒冷季节易诱发关节疼痛。主要原理为:
①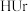 (尿酸)
(尿酸)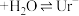 (尿酸离子)
(尿酸离子)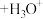
②
下列叙述错误 的是
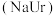 晶体有关,尤其在寒冷季节易诱发关节疼痛。主要原理为:
晶体有关,尤其在寒冷季节易诱发关节疼痛。主要原理为:①
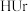 (尿酸)
(尿酸)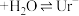 (尿酸离子)
(尿酸离子)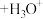
②

下列叙述
| A.①是尿酸的电离方程式 |
B.反应②的 ,因此热敷能减轻关节疼痛 ,因此热敷能减轻关节疼痛 |
| C.饮食中摄入过多食盐,容易诱发痛风 |
| D.“痛风”患者应控制摄入产生较多尿酸的食物 |
您最近一年使用:0次
2023-01-12更新
|
146次组卷
|
3卷引用:上海市七宝中学2022-2023学年高二上学期期末考试化学试题
上海市七宝中学2022-2023学年高二上学期期末考试化学试题(已下线)专题03 化学反应进行的方向和限度-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)课时3影响化学平衡的因素随堂练习
名校
6 . 在 的平衡体系中,当分离出
的平衡体系中,当分离出 时,下列说法正确
时,下列说法正确
 的平衡体系中,当分离出
的平衡体系中,当分离出 时,下列说法正确
时,下列说法正确| A.单位时间单位体积内氮气与氢气的有效碰撞次数增加 | B.平衡向逆反应方向移动 |
| C.正反应速率变化更显著 | D.逆反应速率先变小后变大 |
您最近一年使用:0次
2023-01-11更新
|
138次组卷
|
3卷引用:上海市晋元高级中学2022-2023学年高二上学期1月期末考试(等级考)化学试题
上海市晋元高级中学2022-2023学年高二上学期1月期末考试(等级考)化学试题(已下线)专题03 化学反应进行的方向和限度-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)上海市嘉定区第二中学2022-2023学年高二下学期第一次质量检测化学试题
名校
7 . 下列事实能用勒夏特列原理解释的是
| A.500℃左右高温比室温下更利于合成氨 |
| B.工业制硫酸中SO2氧化为SO3,往往需要使用催化剂 |
| C.H2、I2、HI平衡混合气体加压后颜色加深 |
D.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g),使K变成蒸气从混合体系中分离 NaCl(l)+K(g),使K变成蒸气从混合体系中分离 |
您最近一年使用:0次
2023-01-11更新
|
174次组卷
|
4卷引用:上海市华东师范大学第一附属中学2022-2023学年高二上学期1月期末考试化学试题
上海市华东师范大学第一附属中学2022-2023学年高二上学期1月期末考试化学试题上海市华东师范大学第一附属中学2022-2023学年高二上学期期末考试化学试题(已下线)专题03 化学反应进行的方向和限度-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)四川省自贡市2023-2024学年高二上学期期末考试化学试题
8 . 在密闭容器中进行反应N2(g)+3H2(g)⇌2NH3(g),达到平衡时,若温度保持不变,增加N2的浓度,则
| A.正反应速率一直增大 | B.逆反应速率先减小 |
| C.化学平衡向正反应方向移动 | D.化学平衡向逆反应方向移动 |
您最近一年使用:0次
2022高二·上海·专题练习
名校
9 . 高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g) Fe(s)+CO2(g)ΔH>0
Fe(s)+CO2(g)ΔH>0
其平衡常数可表示为K=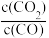 ,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比___________ ,平衡常数K___________ 。(以上均填“增大”“减小”或“不变”)
(2)1100℃时测得高炉中c(CO2)=0.025mol·L-1、c(CO)=0.1mol·L-1,在这种情况下,该反应是否处于化学平衡状态:___________ (填“是”或“否”,若填“是”,则后面问题可不答),此时反应向___________ (填“正反应”或“逆反应”)方向进行,其原因是___________ 。
 Fe(s)+CO2(g)ΔH>0
Fe(s)+CO2(g)ΔH>0其平衡常数可表示为K=
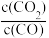 ,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比
(2)1100℃时测得高炉中c(CO2)=0.025mol·L-1、c(CO)=0.1mol·L-1,在这种情况下,该反应是否处于化学平衡状态:
您最近一年使用:0次
名校
10 . 在 溶液中存在平衡
溶液中存在平衡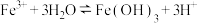 。现要使平衡向逆方向移动且使
。现要使平衡向逆方向移动且使 增大的是
增大的是
 溶液中存在平衡
溶液中存在平衡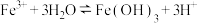 。现要使平衡向逆方向移动且使
。现要使平衡向逆方向移动且使 增大的是
增大的是| A.加热 | B.通入HCl气体 | C.加入NaOH溶液 | D.加水稀释 |
您最近一年使用:0次



