解题方法
1 . 芙蓉洞位于武隆乌江最大支流芙蓉江畔的半山腰上,形成于100万年前,在2007年被列人世界遗产名录,属于武隆喀斯特地质的一部分。某小组研究发现,芙蓉洞内石样质量与温度、日游客流量关系如图所示。

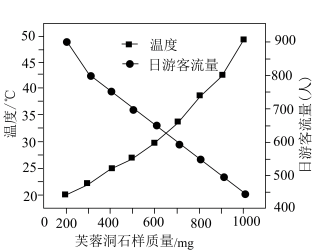
| A.芙蓉洞的形成与气候、地理环境有密切关系 |
| B.芙蓉洞形成与风化过程中只发生了物理变化 |
C.日游客流量增大, 浓度增大导致芙蓉洞石样质量减小 浓度增大导致芙蓉洞石样质量减小 |
| D.芙蓉洞石样质量减小过程中发生了化合反应 |
您最近一年使用:0次
2024-03-12更新
|
45次组卷
|
2卷引用:黑龙江省哈尔滨市2023-2024学年高三上学期六校联考化学试题
名校
2 . 恒容密闭容器中发生反应
 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是A.室温下能自发进行,表明该反应的 |
| B.保持温度一定,充入氩气使反应速率加快 |
| C.加入合适的催化剂,既能改变反应历程又能降低活化能 |
D.其他条件一定,再通入适量 , , 和 和 的转化率都将增大 的转化率都将增大 |
您最近一年使用:0次
2024-02-29更新
|
80次组卷
|
2卷引用:四川省德阳市高中2023-2024学年学年高二上学期期末教学质量检测考试化学试题
名校
3 . 现有一份“将二氧化硫转化为硫酸铵”的资料,摘录如下:
一个典型实例:初步处理后的废气含0.20%的二氧化硫和10%的氧气(体积分数)。在400℃时废气以5 m3·h-1的速率通过五氧化二钒催化剂层与20 L·h-1的速率的氨气混合,再喷水,此时气体温度由400℃降至200℃,在热的结晶装置中得到硫酸铵晶体(气体体积均已折算为标准状况)。利用上述资料,用氨来除去工业废气中的二氧化硫,回答下列问题:
(1)按反应中的理论值,二氧化硫和氧气的物质的量之比为2∶1,该资料中这个比值是___________ ,简述不采用2∶1的理由是___________ 。
(2)通过计算,说明为什么废气以5 m3·h-1的速率与20 L·h-1速率的氨气混合___________ 。
(3)若某厂每天排放1×104 m3这种废气,按上述方法该厂每月(按30天计)可得硫酸铵___________ 吨,消耗氨气___________ 吨。
一个典型实例:初步处理后的废气含0.20%的二氧化硫和10%的氧气(体积分数)。在400℃时废气以5 m3·h-1的速率通过五氧化二钒催化剂层与20 L·h-1的速率的氨气混合,再喷水,此时气体温度由400℃降至200℃,在热的结晶装置中得到硫酸铵晶体(气体体积均已折算为标准状况)。利用上述资料,用氨来除去工业废气中的二氧化硫,回答下列问题:
(1)按反应中的理论值,二氧化硫和氧气的物质的量之比为2∶1,该资料中这个比值是
(2)通过计算,说明为什么废气以5 m3·h-1的速率与20 L·h-1速率的氨气混合
(3)若某厂每天排放1×104 m3这种废气,按上述方法该厂每月(按30天计)可得硫酸铵
您最近一年使用:0次
4 . 甲醇和水蒸气催化重整制取氢气的原理为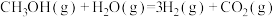 .重整过程中的主要反应为:
.重整过程中的主要反应为:
反应1: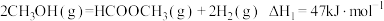
反应2: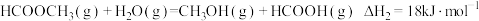
反应3: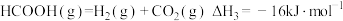
(1)反应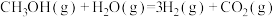 的
的
______________ .
(2)在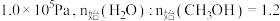 时,密闭容器中发生反应1、2、3.随温度的升高,平衡时容器中
时,密闭容器中发生反应1、2、3.随温度的升高,平衡时容器中 的浓度先增大后减小.过程中
的浓度先增大后减小.过程中 浓度减小的原因是
浓度减小的原因是______________ .
(3)选择膜反应器可提高重整效率.膜反应器中金属膜允许 通过,而
通过,而 气体等不能通过.膜反应器的作用是
气体等不能通过.膜反应器的作用是______________ .
(4)在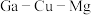 催化剂表面上甲醇与水蒸气重整的机理如图所示.
催化剂表面上甲醇与水蒸气重整的机理如图所示.
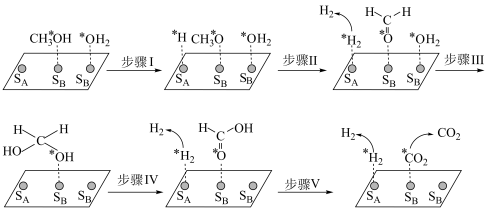
其中“*”表示该微粒吸附在催化剂表面,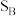 为带有一定电性的吸附位点.
为带有一定电性的吸附位点. 表示微粒从催化剂表面脱附.
表示微粒从催化剂表面脱附.
①用 替换
替换 ,生成氢气的化学式是
,生成氢气的化学式是______________ .
②从电负性的角度分析,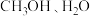 均通过
均通过 原子吸附在催化剂
原子吸附在催化剂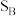 位点上的原因是
位点上的原因是______________ .
③从化学键断裂和形成以及微粒吸附与脱附的角度,步骤Ⅳ的反应过程可描述为______________ .
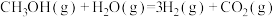 .重整过程中的主要反应为:
.重整过程中的主要反应为:反应1:
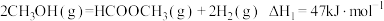
反应2:
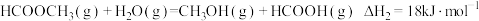
反应3:
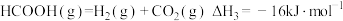
(1)反应
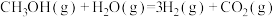 的
的
(2)在
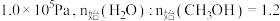 时,密闭容器中发生反应1、2、3.随温度的升高,平衡时容器中
时,密闭容器中发生反应1、2、3.随温度的升高,平衡时容器中 的浓度先增大后减小.过程中
的浓度先增大后减小.过程中 浓度减小的原因是
浓度减小的原因是(3)选择膜反应器可提高重整效率.膜反应器中金属膜允许
 通过,而
通过,而 气体等不能通过.膜反应器的作用是
气体等不能通过.膜反应器的作用是(4)在
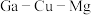 催化剂表面上甲醇与水蒸气重整的机理如图所示.
催化剂表面上甲醇与水蒸气重整的机理如图所示.
其中“*”表示该微粒吸附在催化剂表面,
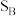 为带有一定电性的吸附位点.
为带有一定电性的吸附位点. 表示微粒从催化剂表面脱附.
表示微粒从催化剂表面脱附. ①用
 替换
替换 ,生成氢气的化学式是
,生成氢气的化学式是②从电负性的角度分析,
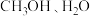 均通过
均通过 原子吸附在催化剂
原子吸附在催化剂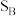 位点上的原因是
位点上的原因是③从化学键断裂和形成以及微粒吸附与脱附的角度,步骤Ⅳ的反应过程可描述为
您最近一年使用:0次
解题方法
5 . 下列说法正确的是
| A.为防止海轮腐蚀,可在其外壳上镶嵌铜块 |
B.高压氧仓治疗 中毒的原理是 中毒的原理是 ,增大 ,增大 有利于反应正向进行 有利于反应正向进行 |
| C.电解精炼铜时,阴极增加的质量与阳极减少的质量相等 |
D. 与 与 在催化剂、 在催化剂、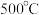 下混合反应生成 下混合反应生成 ,转移电子的数目约为 ,转移电子的数目约为 |
您最近一年使用:0次
6 . 下列说法正确的是
A.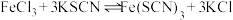 ,向 ,向 与KSCN混合液中加入KCl固体,溶液红色变浅 与KSCN混合液中加入KCl固体,溶液红色变浅 |
B. , , ,加热氯化铜溶液,溶液变成蓝绿色 ,加热氯化铜溶液,溶液变成蓝绿色 |
C.可通过观察气泡产生的快慢,探究影响 与稀硫酸反应速率的因素 与稀硫酸反应速率的因素 |
D.可通过测定单位时间内生成 的体积,比较Zn与不同浓度硫酸溶液反应速率的快慢 的体积,比较Zn与不同浓度硫酸溶液反应速率的快慢 |
您最近一年使用:0次
7 . 一定条件下,可逆反应
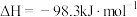 。下列有关叙述错误的是
。下列有关叙述错误的是

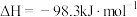 。下列有关叙述错误的是
。下列有关叙述错误的是A.相同条件下, 和 和 反应生成2mol 反应生成2mol ,放出的热量为 ,放出的热量为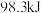 |
B.恒容条件下,向平衡体系中通入一定量 , , 的平衡转化率减小 的平衡转化率减小 |
C.恒压条件下,向平衡体系中通入一定量 ,平衡不移动 ,平衡不移动 |
D.及时分离出 ,平衡正向移动,平衡常数不变 ,平衡正向移动,平衡常数不变 |
您最近一年使用:0次
名校
8 . Ⅰ.传统的“哈伯法”合成氨原理为: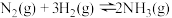
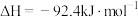
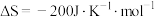
(1)上述反应在常温下___________ (填“能”或“不能”)自发进行。
(2)工业合成氨选择的催化剂是___________ 。
(3)恒温、恒容密闭容器中进行上述反应,一定能说明该反应达到平衡状态的是___________ 。
a. 、
、 、
、 的浓度之比为
的浓度之比为 b.容器内气体压强保持不变
b.容器内气体压强保持不变
c.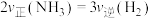 d.混合气体的密度保持不变
d.混合气体的密度保持不变
(4)改变下列条件能加快反应速率,且单位体积内反应物活化分子百分数不变的是___________ 。
a.增大浓度 b.增大压强 c.升高温度 d.使用催化剂
(5)工业合成氨中,下列措施不符合绿色化学理念的是___________ 。
a.将氨气及时液化,分离出反应体系
b.将从反应体系中分离出的 和
和 重新输送到反应器中予以循环利用
重新输送到反应器中予以循环利用
c.氨合成塔中内置热交换器用来预热后续通入的冷的氮气和氢气
d.可采用1000℃的高温使得反应速率更快
Ⅱ.科研小组模拟不同条件下的合成氨反应,向体积可变的密闭容器中充入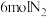 和
和 ,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。
,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。

(6) 、
、 、
、 由小到大的顺序为
由小到大的顺序为___________ 。
(7)在 、
、 条件下,若此时容器体积为
条件下,若此时容器体积为 ,
, 后反应达到平衡,则
后反应达到平衡,则 内
内 的平均反应速率为
的平均反应速率为___________ ,平衡常数
___________ (保留两位有效数字)。
Ⅲ.东南大学王金兰课题组提出合成氨的“表面氢化机理”,在较低的电压下实现氮气的还原合成氨。
已知:第一步: (快)(吸附在催化剂表面的物种用*表示)
(快)(吸附在催化剂表面的物种用*表示)
第二步: (慢)(吸附在催化剂表面)
(慢)(吸附在催化剂表面)
第三步: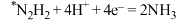 (快)
(快)
(8)较传统工业合成氨法,该方法具有的优点___________ 。
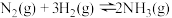
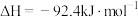
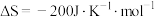
(1)上述反应在常温下
(2)工业合成氨选择的催化剂是
(3)恒温、恒容密闭容器中进行上述反应,一定能说明该反应达到平衡状态的是
a.
 、
、 、
、 的浓度之比为
的浓度之比为 b.容器内气体压强保持不变
b.容器内气体压强保持不变c.
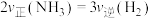 d.混合气体的密度保持不变
d.混合气体的密度保持不变(4)改变下列条件能加快反应速率,且单位体积内反应物活化分子百分数不变的是
a.增大浓度 b.增大压强 c.升高温度 d.使用催化剂
(5)工业合成氨中,下列措施不符合绿色化学理念的是
a.将氨气及时液化,分离出反应体系
b.将从反应体系中分离出的
 和
和 重新输送到反应器中予以循环利用
重新输送到反应器中予以循环利用c.氨合成塔中内置热交换器用来预热后续通入的冷的氮气和氢气
d.可采用1000℃的高温使得反应速率更快
Ⅱ.科研小组模拟不同条件下的合成氨反应,向体积可变的密闭容器中充入
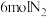 和
和 ,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。
,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。
(6)
 、
、 、
、 由小到大的顺序为
由小到大的顺序为(7)在
 、
、 条件下,若此时容器体积为
条件下,若此时容器体积为 ,
, 后反应达到平衡,则
后反应达到平衡,则 内
内 的平均反应速率为
的平均反应速率为
Ⅲ.东南大学王金兰课题组提出合成氨的“表面氢化机理”,在较低的电压下实现氮气的还原合成氨。
已知:第一步:
 (快)(吸附在催化剂表面的物种用*表示)
(快)(吸附在催化剂表面的物种用*表示)第二步:
 (慢)(吸附在催化剂表面)
(慢)(吸附在催化剂表面)第三步:
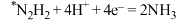 (快)
(快)(8)较传统工业合成氨法,该方法具有的优点
您最近一年使用:0次
9 . 下列说法正确的是
A.将装有 气体的注射器压缩至原体积的一半,压缩后的气体颜色比压缩前深,则说明增大压强, 气体的注射器压缩至原体积的一半,压缩后的气体颜色比压缩前深,则说明增大压强, 平衡向逆反应方向移动 平衡向逆反应方向移动 |
B.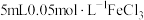 溶液中滴入几滴KSCN溶液,溶液呈红色,再加入少量KCl固体,溶液红色变浅,则说明增大生成物浓度,平衡向逆反应方向移动 溶液中滴入几滴KSCN溶液,溶液呈红色,再加入少量KCl固体,溶液红色变浅,则说明增大生成物浓度,平衡向逆反应方向移动 |
C.加热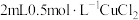 溶液,溶液变为黄绿色,则说明 溶液,溶液变为黄绿色,则说明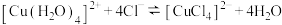 的 的 |
D.对 的平衡体系压缩体积,体系颜色变深,则说明增大压强,平衡向逆反应方向移动 的平衡体系压缩体积,体系颜色变深,则说明增大压强,平衡向逆反应方向移动 |
您最近一年使用:0次
名校
解题方法
10 . 一定温度下,烧杯中有25mL对二甲苯和5mL水,加入bmol HA后充分搅拌并完全溶解,静置平衡后HA在对二甲苯(PX)中浓度为 ,在水(W)中浓度为
,在水(W)中浓度为 。已知:
。已知:
①实验条件下HA在两相间的分配系数: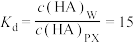 (只与温度有关):
(只与温度有关):
②HA不能在对二甲苯中电离,在水中电离平衡常数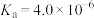 。
。
忽略溶液混合时体积的变化,下列说法错误的是
 ,在水(W)中浓度为
,在水(W)中浓度为 。已知:
。已知:①实验条件下HA在两相间的分配系数:
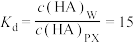 (只与温度有关):
(只与温度有关):②HA不能在对二甲苯中电离,在水中电离平衡常数
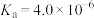 。
。忽略溶液混合时体积的变化,下列说法错误的是
A.水溶液中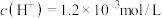 |
B.若向平衡体系中再加入对二甲苯,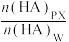 减小 减小 |
C.若向平衡体系中再加入20mL水,平衡后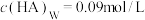 |
D.若向平衡体系中再加入NaOH固体,使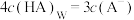 ,平衡后 ,平衡后 |
您最近一年使用:0次
2023-12-05更新
|
298次组卷
|
3卷引用:重庆市巫溪县中学校2023-2024学年高二上学期期末模拟考试化学试题



