1 . 根据下列实验设计,回答问题:
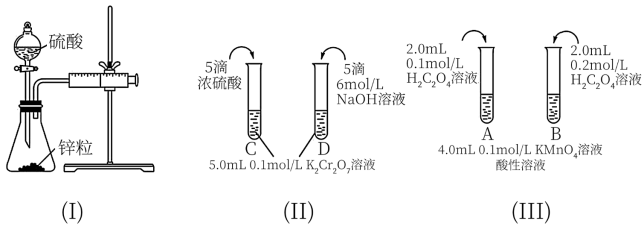
(1)利用实验(Ⅰ)探究锌与0.1 硫酸和2
硫酸和2 硫酸反应的速率,可以测定收集一定体积氢气所用的时间。检查该装置气密性的操作是:
硫酸反应的速率,可以测定收集一定体积氢气所用的时间。检查该装置气密性的操作是:___________ 。
(2)实验(Ⅱ)探究浓度对化学化学平衡的影响。
已知: (橙色)
(橙色) (黄色)
(黄色) 推测D试管中实验现象为
推测D试管中实验现象为___________ ,用平衡移动原理解释原因:___________ 。
(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中反应离子方程式为___________ ,推测该实验设计能否达到实验目的并描述判断理由:___________ 。
(4)某小组也用酸性KMnO4溶液和草酸( )溶液进行实验,实验操作及现象如下表:
)溶液进行实验,实验操作及现象如下表:
①实验i、实验ii可得出的结论是___________ 。
②关于实验ii中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 对反应有催化作用。利用提供的试剂设计实验iii,验证猜想。
对反应有催化作用。利用提供的试剂设计实验iii,验证猜想。
提供试剂:0.01 酸性
酸性 溶液,0.1
溶液,0.1 草酸溶液,3
草酸溶液,3 硫酸,
硫酸, 溶液,
溶液, 固体,蒸馏水。
固体,蒸馏水。
补全实验iii的操作:向试管中先加入5 0.01
0.01 酸性
酸性 溶液,
溶液,___________ ,最后加入5 0.1
0.1 草酸溶液。
草酸溶液。

(1)利用实验(Ⅰ)探究锌与0.1
 硫酸和2
硫酸和2 硫酸反应的速率,可以测定收集一定体积氢气所用的时间。检查该装置气密性的操作是:
硫酸反应的速率,可以测定收集一定体积氢气所用的时间。检查该装置气密性的操作是:(2)实验(Ⅱ)探究浓度对化学化学平衡的影响。
已知:
 (橙色)
(橙色) (黄色)
(黄色) 推测D试管中实验现象为
推测D试管中实验现象为(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中反应离子方程式为
(4)某小组也用酸性KMnO4溶液和草酸(
 )溶液进行实验,实验操作及现象如下表:
)溶液进行实验,实验操作及现象如下表:| 编号 | 实验操作 | 实验现象 |
| i | 向一支试管中先加入5 0.01 0.01 酸性 酸性 溶液,再加入1滴3 溶液,再加入1滴3 硫酸和9滴蒸馏水,最后加入5 硫酸和9滴蒸馏水,最后加入5 0.1 0.1 草酸溶液 草酸溶液 | 前10 内溶液紫色无明显变化,后颜色逐渐变浅,30 内溶液紫色无明显变化,后颜色逐渐变浅,30 后几乎变为无色 后几乎变为无色 |
| ii | 向另一支试管中先加入5 0.01 0.01 酸性 酸性 溶液,再加入10滴3 溶液,再加入10滴3 硫酸,最后加入5 硫酸,最后加入5 0.1m 0.1m 草酸溶液 草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
②关于实验ii中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的
 对反应有催化作用。利用提供的试剂设计实验iii,验证猜想。
对反应有催化作用。利用提供的试剂设计实验iii,验证猜想。提供试剂:0.01
 酸性
酸性 溶液,0.1
溶液,0.1 草酸溶液,3
草酸溶液,3 硫酸,
硫酸, 溶液,
溶液, 固体,蒸馏水。
固体,蒸馏水。补全实验iii的操作:向试管中先加入5
 0.01
0.01 酸性
酸性 溶液,
溶液, 0.1
0.1 草酸溶液。
草酸溶液。
您最近一年使用:0次
2021-11-05更新
|
379次组卷
|
4卷引用:广东省广州市部分学校2021-2022学年高二上学期期中联考化学试题
2 . 盐酸羟胺(化学式为 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
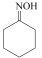 (环己酮肟)
(环己酮肟)
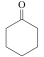 (环己酮)
(环己酮)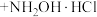
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。
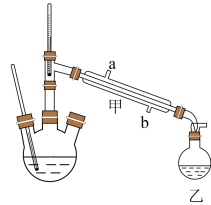
盐酸羟胺在不同温度下的溶解度如下表:
(1)仪器甲中进水口应为___________ 。
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是___________ 。
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
(4)反应后,从三口烧瓶的溶液中获取盐酸羟胺的实验方法为___________。
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵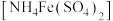 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。
反应原理为:①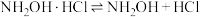
②
③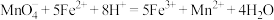
(5)将反应②补充完整,并标出电子转移的方向和数目___________ 。
(6)配制上述盐酸羟胺溶液所需要的定量仪器有___________ 。
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为___________ 。
(7)通过计算判断该产品的纯度级别___________ 。(写出计算过程)
已知:
 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
 (环己酮肟)
(环己酮肟)
 (环己酮)
(环己酮)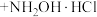
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。

盐酸羟胺在不同温度下的溶解度如下表:
| 温度(℃) | 溶解度(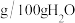 ) ) |
| 20 | 46.7 |
| 40 | 54.9 |
| 60 | 63.2 |
| 80 | 71.1 |
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
| A.共价键 | B.离子键 | C.氢键 | D.范德华力 |
| A.冷却结晶 | B.渗析 | C.蒸馏 | D.萃取、分液 |
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵
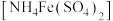 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。反应原理为:①
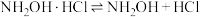
②

③
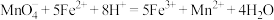
(5)将反应②补充完整,并标出电子转移的方向和数目
(6)配制上述盐酸羟胺溶液所需要的定量仪器有
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为
(7)通过计算判断该产品的纯度级别
| 纯度级别 | 优级纯 | 分析纯 | 化学纯 |
质量分数 | 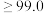 |  |  |

您最近一年使用:0次
2024-01-13更新
|
364次组卷
|
3卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
上海市四区联考2023-2024学年高三上学期化学一模试卷(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
解题方法
3 . 碘化钾用作制有机物及制药原料,医疗上用于防治甲状腺肿大,作祛痰药,还可用于照相制版等。实验小组设计实验制备KI并探究相关性质。
(一)制备KI
某实验小组设计制备一定量KI的实验(加热及夹持装置已省略)如下:
反应I:
反应Ⅱ: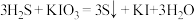
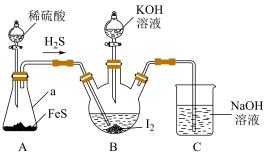
(1)实验开始前,先进行装置气密性检查:将C中导管下端管口浸入液面以下,塞紧瓶塞,微热A装置,若___________ ,则气密性良好。
(2)在装置B中先滴入KOH溶液,待观察到三颈烧瓶中溶液颜色由___________ 色变为___________ 色,停止滴入KOH溶液;然后打开装置A中分液漏斗活塞,待三颈烧瓶和烧杯中产生气泡的速率接近相等时停止通气,反应完成。
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是___________ 。
(4)装置B中所得KI溶液经分离提纯后得到KI粗产品,为测定KI的纯度,称取1.0g样品溶于水,然后用0.0500mol·L-1酸性KMnO4标准溶液滴定( ),杂质不与酸性KMnO4溶液反应。平行滴定三次,滴定到终点平均消耗酸性KMnO4标准溶液20.00mL,则样品的纯度为
),杂质不与酸性KMnO4溶液反应。平行滴定三次,滴定到终点平均消耗酸性KMnO4标准溶液20.00mL,则样品的纯度为___________ (保留两位有效数字)。
(二)实验探究:FeCl3与KI的反应
(5)证明实验I中有I2生成,加入的试剂为(有机溶剂除外)___________ 。
(6)已知在酸性较强的条件下,I-可被空气氧化为I2,为探究实验I中20min后棕黄色变深的原因,甲同学提出假设:该反应条件下空气将I-氧化为I2,使实验I中溶液棕黄色变深。甲同学设计的实验为:___________ ,若20min后溶液不变蓝,证明该假设不成立。(可选试剂:0.1mol·L-1KI溶液、0.1mol·L-1FeCl3溶液、淀粉溶液、稀硫酸)
(7)乙同学查阅资料可知:①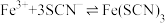 ;②FeCl3与KI反应的平衡体系中还存在反应
;②FeCl3与KI反应的平衡体系中还存在反应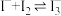 ,
, 呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20min后溶液红色变浅的原因:
呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20min后溶液红色变浅的原因:___________ 。
(一)制备KI
某实验小组设计制备一定量KI的实验(加热及夹持装置已省略)如下:
反应I:

反应Ⅱ:
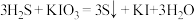

(1)实验开始前,先进行装置气密性检查:将C中导管下端管口浸入液面以下,塞紧瓶塞,微热A装置,若
(2)在装置B中先滴入KOH溶液,待观察到三颈烧瓶中溶液颜色由
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是
(4)装置B中所得KI溶液经分离提纯后得到KI粗产品,为测定KI的纯度,称取1.0g样品溶于水,然后用0.0500mol·L-1酸性KMnO4标准溶液滴定(
 ),杂质不与酸性KMnO4溶液反应。平行滴定三次,滴定到终点平均消耗酸性KMnO4标准溶液20.00mL,则样品的纯度为
),杂质不与酸性KMnO4溶液反应。平行滴定三次,滴定到终点平均消耗酸性KMnO4标准溶液20.00mL,则样品的纯度为(二)实验探究:FeCl3与KI的反应
| 序号 | 操作 | 现象 |
| 实验I | 取5mL0.1mol·L-1KI溶液,滴加0.1mol·L-1 FeCl3溶液5~6滴(混合溶液的pH=5) | 溶液变为棕黄色,20min后棕黄色变深 |
| 实验Ⅱ | 取少量实验I中棕黄色溶液于试管中,滴加2滴KSCN溶液 | 溶液变红,20min后红色变浅 |
(5)证明实验I中有I2生成,加入的试剂为(有机溶剂除外)
(6)已知在酸性较强的条件下,I-可被空气氧化为I2,为探究实验I中20min后棕黄色变深的原因,甲同学提出假设:该反应条件下空气将I-氧化为I2,使实验I中溶液棕黄色变深。甲同学设计的实验为:
(7)乙同学查阅资料可知:①
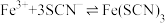 ;②FeCl3与KI反应的平衡体系中还存在反应
;②FeCl3与KI反应的平衡体系中还存在反应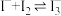 ,
, 呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20min后溶液红色变浅的原因:
呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20min后溶液红色变浅的原因:
您最近一年使用:0次
解题方法
4 . 碘化亚铜(CuI)是重要的有机催化剂。某学习小组用如图装置制备CuI,并设计实验探究其性质。已知:碘化亚铜(CuI)是白色固体,难溶于水,易与KI形成K[CuI2]实验装置如图1所示。
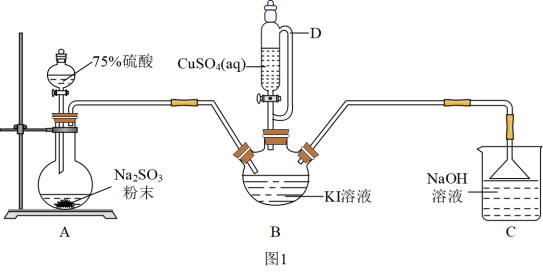
(1)仪器D的名称是________ 。
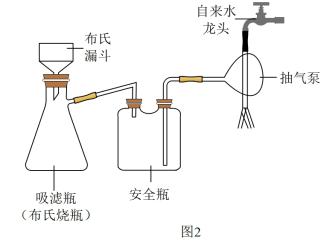
(2)实验完毕后,用图2所示装置分离CuI的突出优点是_______ 。
(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法是:_______ 。
(4)装置B中发生反应的离子方程式是_______ 。
(5)小组同学设计下表方案对CuI的性质进行探究:
①在实验I中“加水,又生成白色沉淀”的原理是_______ 。
②根据实验II,CuI与NaOH溶液反应的化学方程式是_______ 。
(6)测定CuI样品纯度。取a g CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用b mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积为V mL(已知:滴定反应为I2+2 =
= (无色)+2I-)。该样品纯度为
(无色)+2I-)。该样品纯度为_______ (用含a、b、V的代数式表示)。如果其他操作均正确,仅滴定前盛标准液的滴定管用蒸馏水洗净后没有用标准液润洗,测得结果_______ (填“偏高”“偏低”或“无影响”)。

(1)仪器D的名称是
(2)实验完毕后,用图2所示装置分离CuI的突出优点是

(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法是:
(4)装置B中发生反应的离子方程式是
(5)小组同学设计下表方案对CuI的性质进行探究:
| 实验 | 实验操作及现象 |
| Ⅰ | 取少量CuI放入试管中,加入KI溶液,白色固体溶解得到无色溶液;加水,又生成白色沉淀 |
| Ⅱ | 取少量CuI放入试管中,加入NaOH溶液,振荡,产生砖红色沉淀。过滤,向所得上层清液中滴加淀粉溶液,无明显变化;将砖红色沉淀溶于稀硫酸,产生红色固体和蓝色溶液 |
②根据实验II,CuI与NaOH溶液反应的化学方程式是
(6)测定CuI样品纯度。取a g CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用b mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积为V mL(已知:滴定反应为I2+2
 =
= (无色)+2I-)。该样品纯度为
(无色)+2I-)。该样品纯度为
您最近一年使用:0次
5 . 无水氯化亚铁为白色吸湿性粉末,在空气中易被氧化,易溶于水,不溶于氯仿等有机溶剂。实验室常用无水氯化铁和氯苯反应制备无水氯化亚铁,反应原理为:2FeCl3+C6H5Cl=2FeCl2+C6H4Cl2+HCl。实验装置如图所示:

回答下列问题:
(1)装置a的名称是___________ ;连接好装置开始实验前必须进行的操作是___________ 。
(2)搅拌器的作用是___________ 。
(3)从化学平衡的角度解释需要不断蒸出氯化氢的原因是___________ 。
(4)反应结束后,将三颈烧瓶中的固体过滤___________ 、真空干燥后得到纯净的产品,并隔绝空气保存。
(5)氯化亚铁溶液容易被空气中的氧气氧化,反应的离子反应方程式为___________ 。
(6)本次实验共消耗165 g无水氯化铁和225 g氯苯。为测定该反应的转化率,小华同学用2 mol/L的NaOH溶液滴定溶于水的氯化氢,并以甲基橙做指示剂,达到滴定终点时的现象为___________ 。滴定消耗氢氧化钠共250 mL,则氯化铁的转化率为___________ (结果保留三位有效数字)。

回答下列问题:
(1)装置a的名称是
(2)搅拌器的作用是
(3)从化学平衡的角度解释需要不断蒸出氯化氢的原因是
(4)反应结束后,将三颈烧瓶中的固体过滤
(5)氯化亚铁溶液容易被空气中的氧气氧化,反应的离子反应方程式为
(6)本次实验共消耗165 g无水氯化铁和225 g氯苯。为测定该反应的转化率,小华同学用2 mol/L的NaOH溶液滴定溶于水的氯化氢,并以甲基橙做指示剂,达到滴定终点时的现象为
您最近一年使用:0次
名校
解题方法
6 . 根据下列实验设计,回答问题:

(1)利用实验(I)探究锌与 硫酸和
硫酸和 硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):
硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):___________ 。
(2)实验(II)探究浓度对化学化学平衡影响。已知重铬酸钾溶液存在: (橙色)和
(橙色)和 (黄色)的平衡,如图操作,C中溶液颜色变深,D中溶液颜色变浅,
(黄色)的平衡,如图操作,C中溶液颜色变深,D中溶液颜色变浅,
①依据题意写出其中的离子方程式___________ ,
②用平衡移动原理解释D颜色变浅的原因:___________ ;
③加水稀释,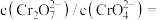
___________ (答“变大”、“变小”或“不变”)
(3)实验(III)目的是探究浓度对反应速率的影响,实验中发生反应: 。某小组也用酸性
。某小组也用酸性 溶液和草酸
溶液和草酸 溶液进行实验,实验操作及现象如下表:
溶液进行实验,实验操作及现象如下表:
①由实验i、实验ii可得出的结论是___________ 。
②关于实验i中 后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的
后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
提供的试剂: 酸性
酸性 溶液,
溶液, 草酸溶液,
草酸溶液, 硫酸,
硫酸, 溶波,
溶波, 固体,蒸馏水。
固体,蒸馏水。
补全实验ⅲ的操作:向试管中先加入 酸性
酸性 溶液,
溶液,___________ ,最后加入 草酸溶液。
草酸溶液。
③基于以上实验与分析,推测实验(III)设计___________ (填“能”或“不能”)达到实验目的。

(1)利用实验(I)探究锌与
 硫酸和
硫酸和 硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):
硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):(2)实验(II)探究浓度对化学化学平衡影响。已知重铬酸钾溶液存在:
 (橙色)和
(橙色)和 (黄色)的平衡,如图操作,C中溶液颜色变深,D中溶液颜色变浅,
(黄色)的平衡,如图操作,C中溶液颜色变深,D中溶液颜色变浅,①依据题意写出其中的离子方程式
②用平衡移动原理解释D颜色变浅的原因:
③加水稀释,
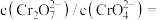
(3)实验(III)目的是探究浓度对反应速率的影响,实验中发生反应:
 。某小组也用酸性
。某小组也用酸性 溶液和草酸
溶液和草酸 溶液进行实验,实验操作及现象如下表:
溶液进行实验,实验操作及现象如下表:| 编号 | 实验操作 | 实验现象 |
| i | 向一支试管中先加入 酸性 酸性 溶液,再加入1滴 溶液,再加入1滴 硫酸和9滴蒸馏水、最后加入 硫酸和9滴蒸馏水、最后加入 草酸溶液 草酸溶液 | 前 内溶液紫色无明显变化,后颜色逐渐变浅, 内溶液紫色无明显变化,后颜色逐渐变浅, 后几乎变为无色 后几乎变为无色 |
| ii | 向另一支试管中先加入 酸性 酸性 溶液,再加入10滴 溶液,再加入10滴 硫酸,最后加入 硫酸,最后加入 草酸溶液 草酸溶液 |  内溶液紫色无明显变化,后颜色迅速变浅,约 内溶液紫色无明显变化,后颜色迅速变浅,约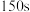 后几乎变为无色 后几乎变为无色 |
②关于实验i中
 后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的
后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。提供的试剂:
 酸性
酸性 溶液,
溶液, 草酸溶液,
草酸溶液, 硫酸,
硫酸, 溶波,
溶波, 固体,蒸馏水。
固体,蒸馏水。补全实验ⅲ的操作:向试管中先加入
 酸性
酸性 溶液,
溶液, 草酸溶液。
草酸溶液。③基于以上实验与分析,推测实验(III)设计
您最近一年使用:0次
名校
解题方法
7 . 根据下列实验设计,回答问题:
(1)利用实验(Ⅰ)探究锌与0.1mol/L硫酸和2mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):_______ 。

(2)实验(Ⅱ)探究浓度对化学化学平衡影响。已知: (橙色)
(橙色) (黄色)
(黄色) 推测D试管中实验现象为
推测D试管中实验现象为_______ ,用平衡移动原理解释原因:______________ 。

(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中发生反应:
 ,某小组也用酸性
,某小组也用酸性 溶液和草酸(
溶液和草酸( )溶液进行实验,实验操作及现象如下表:
)溶液进行实验,实验操作及现象如下表:

①由实验ⅰ、实验ⅱ可得出的结论是_______ 。
②关于实验ⅱ中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
提供的试剂:0.01mol/L酸性 溶液,0.1mol/L草酸溶液,3mol/L硫酸,
溶液,0.1mol/L草酸溶液,3mol/L硫酸, 溶液,
溶液, 固体,蒸馏水。
固体,蒸馏水。
补全实验ⅲ的操作:向试管中先加入5mL 0.01mol/L酸性 溶液,
溶液,_______ ,最后加入5mL 0.1mol/L草酸溶液。
③基于以上实验与分析,推测实验(Ⅲ)设计_______ (填“能”或“不能”)达到实验目的。
(1)利用实验(Ⅰ)探究锌与0.1mol/L硫酸和2mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):

(2)实验(Ⅱ)探究浓度对化学化学平衡影响。已知:
 (橙色)
(橙色) (黄色)
(黄色) 推测D试管中实验现象为
推测D试管中实验现象为
(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中发生反应:

 ,某小组也用酸性
,某小组也用酸性 溶液和草酸(
溶液和草酸( )溶液进行实验,实验操作及现象如下表:
)溶液进行实验,实验操作及现象如下表:
| 编号 | 实验操作 | 实验现象 |
| ⅰ | 向一支试管中先加入5mL 0.01mol/L酸性 溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入5mL 0.1mol/L草酸溶液 溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入5mL 0.1mol/L草酸溶液 | 前10min内溶液紫色无明显变化,后颜色逐渐变浅,30min后几乎变为无色 |
| ⅱ | 向另一支试管中先加入5mL 0.01mol/L酸性 溶液,再加入10滴3mol/L硫酸,最后加入5mL 0.1mol/L草酸溶液 溶液,再加入10滴3mol/L硫酸,最后加入5mL 0.1mol/L草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
②关于实验ⅱ中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的
 对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。提供的试剂:0.01mol/L酸性
 溶液,0.1mol/L草酸溶液,3mol/L硫酸,
溶液,0.1mol/L草酸溶液,3mol/L硫酸, 溶液,
溶液, 固体,蒸馏水。
固体,蒸馏水。补全实验ⅲ的操作:向试管中先加入5mL 0.01mol/L酸性
 溶液,
溶液,③基于以上实验与分析,推测实验(Ⅲ)设计
您最近一年使用:0次
名校
8 . 氯化铁(FeCl3)是一种黑棕色结晶,易升华,易溶于水并且有强烈的吸水性。实验室制备无水氯化铁并探究氯化铁的相关实验如下。
I.利用MnO2粉末、浓盐酸、还原铁粉制备无水氯化铁
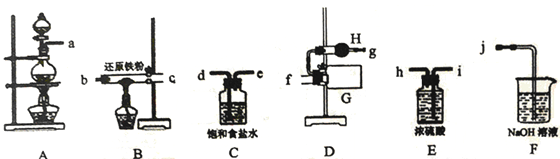
(1)写出装置A中发生的离子方程式_______ 。
(2)整套实验装置接口的连接顺序是_______ ,仪器H的名称是_______ 。
(3)当出现_______ 实验现象时,再点燃B处的酒精灯。
II.探究FeCl3的相关性质
(4)将G中所得固体进行相关实验,完成下列实验,回答问题。
Ⅲ.探究FeCl3与KSCN溶液的反应
(5)向试管中滴加5mL0.01mol/LKSCN溶液,再滴加5mL0.005mol/L FeCl3,溶液显红色,发生反应:Fe3+(aq)+3SCN-(aq)⇌Fe(SCN)3(aq)。将该红色溶液分成2份,分别装于A、B三支试管中,分别完成下列实验。
I.利用MnO2粉末、浓盐酸、还原铁粉制备无水氯化铁

(1)写出装置A中发生的离子方程式
(2)整套实验装置接口的连接顺序是
(3)当出现
II.探究FeCl3的相关性质
(4)将G中所得固体进行相关实验,完成下列实验,回答问题。
| 序号 | 实验操作 | 实验现象 | 问题或结论 |
| ① | 取少量G中固体置于烧杯中,加入适量蒸馏水,搅拌,溶解 | 溶液显浑浊,经过处理,得到澄清溶液。 | 该“处理”的操作是① |
| ② | 取少量①中的澄清溶液于试管中,滴加2滴② | 无明显现象 | 证明原固体中不含FeCl2, 原固体是FeCl3固体 |
| ③ | 将SO2气体通入BaCl2溶液中,再滴入①中的澄清溶液 | 开始无明显现象,后来有白色沉淀生成 | FeCl3表现出③ |
| ④ | 将①中的澄清溶液滴入刚刚做完银镜反应实验的试管中,振荡 | 银镜溶解,溶液显浑浊 | 相关离子方程式是④ |
(5)向试管中滴加5mL0.01mol/LKSCN溶液,再滴加5mL0.005mol/L FeCl3,溶液显红色,发生反应:Fe3+(aq)+3SCN-(aq)⇌Fe(SCN)3(aq)。将该红色溶液分成2份,分别装于A、B三支试管中,分别完成下列实验。
| 序号 | 实验操作 | 实验现象 | 给出合理的解释 |
| ① | 向A试管中滴加5滴1 mol/L KSCN溶液 | 红色溶液变为血红色 | |
| ② | 向B试管中加入lgKCl固体(足量,溶液体积变化忽略不计),振荡,静置 | 固体未完全溶解,红色溶液变浅(接近无色) |
您最近一年使用:0次
名校
解题方法
9 . 根据下列实验设计,回答问题:
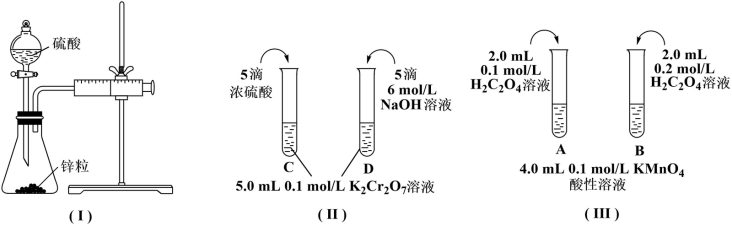
(1)利用实验(Ⅰ)探究锌与0.1mol/L硫酸和2mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):___ 。
(2)实验(Ⅱ)探究浓度对化学化学平衡的影响。
已知:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+推测D试管中实验现象为
(黄色)+2H+推测D试管中实验现象为___ ,用平衡移动原理解释原因:___ 。
(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中反应离子方程式为___ ,推测该实验设计___ (填“能”或“不能”)达到实验目的,判断理由是___ 。
(4)某小组也用酸性KMnO4溶液和草酸(H2C2O4)溶液进行实验,实验操作及现象如下表:
①由实验ⅰ、实验ⅱ可得出的结论是___ 。
②关于实验ⅱ中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的Mn2+对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
提供的试剂:0.01mol/L酸性KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水。
补全实验ⅲ的操作:向试管中先加入5mL0.01mol/L酸性KMnO4溶液,___ ,最后加入5mL0.1mol/L草酸溶液。

(1)利用实验(Ⅰ)探究锌与0.1mol/L硫酸和2mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):
(2)实验(Ⅱ)探究浓度对化学化学平衡的影响。
已知:Cr2O
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+推测D试管中实验现象为
(黄色)+2H+推测D试管中实验现象为(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中反应离子方程式为
(4)某小组也用酸性KMnO4溶液和草酸(H2C2O4)溶液进行实验,实验操作及现象如下表:
| 编号 | 实验操作 | 实验现象 |
| ⅰ | 向一支试管中先加入5mL0.01mol/L酸性KMnO4溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入5mL0.1mol/L草酸溶液 | 前10min内溶液紫色无明显变化,后颜色逐渐变浅,30min后几乎变为无色 |
| ⅱ | 向另一支试管中先加入5mL0.01mol/L酸性KMnO4溶液,再加入10滴3mol/L硫酸,最后加入5mL0.1mol/L草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
②关于实验ⅱ中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的Mn2+对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
提供的试剂:0.01mol/L酸性KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水。
补全实验ⅲ的操作:向试管中先加入5mL0.01mol/L酸性KMnO4溶液,
您最近一年使用:0次
名校
10 . 铁及其化合物在实际生活中应用广泛。
I.一定条件下,Al可以将Fe置换出来,其转化的能量变化如图所示。回答下列问题:

(1)25℃时铝热反应的热化学方程式为________ ,该温度下当有56gFe(s)生成时,转移电子的数目为_______ 。
(2)在1538℃时,反应Fe(s)=Fe(l)的△H值为_______ 。
II.将等体积、低浓度的0.005mol/LFeCl3溶液(已用稀盐酸酸化)和0.01mol/LKSCN溶液混合,静置至体系达平衡,得红色溶液a。各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
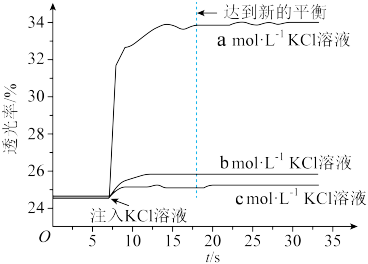
已知:①溶液的透光率与溶液颜色深找有关,颜色深,透光率低。
②FeCl3溶液中存在Fe3++4Cl- [FeCl4]-(黄色)。
[FeCl4]-(黄色)。
(3)工业上通常以FeCl3为腐蚀液,与覆铜板上的Cu反应完成蚀刻。写出蚀刻反应的离子方程式________ 。
(4)采用浓度较低的FeC13溶液制备Fe3+和SCN-平衡体系,是为了避免______ (填离子符号)的颜色对实验干扰。
(5)从实验结果来看,加入KCl溶液使得Fe3++3SCN- Fe(SCN)3,平衡向
Fe(SCN)3,平衡向______ (填“正”或“逆”)反应方向移动。结合实验现象及化学用语分析加入KCl溶液对Fe3+和SCN-平衡体系有影响的原因:________ 。
(6)加入KCl溶液的浓度从大到小排序为_________ (用a、b、c表示)。
I.一定条件下,Al可以将Fe置换出来,其转化的能量变化如图所示。回答下列问题:

(1)25℃时铝热反应的热化学方程式为
(2)在1538℃时,反应Fe(s)=Fe(l)的△H值为
II.将等体积、低浓度的0.005mol/LFeCl3溶液(已用稀盐酸酸化)和0.01mol/LKSCN溶液混合,静置至体系达平衡,得红色溶液a。各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:①溶液的透光率与溶液颜色深找有关,颜色深,透光率低。
②FeCl3溶液中存在Fe3++4Cl-
 [FeCl4]-(黄色)。
[FeCl4]-(黄色)。(3)工业上通常以FeCl3为腐蚀液,与覆铜板上的Cu反应完成蚀刻。写出蚀刻反应的离子方程式
(4)采用浓度较低的FeC13溶液制备Fe3+和SCN-平衡体系,是为了避免
(5)从实验结果来看,加入KCl溶液使得Fe3++3SCN-
 Fe(SCN)3,平衡向
Fe(SCN)3,平衡向(6)加入KCl溶液的浓度从大到小排序为
您最近一年使用:0次



