名校
1 . 在1373K、100kPa反应条件下,H2S可以发生热解反应: △H>0。对于
△H>0。对于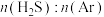 分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示。下列说法错误的是
分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示。下列说法错误的是
 △H>0。对于
△H>0。对于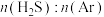 分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示。下列说法错误的是
分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示。下列说法错误的是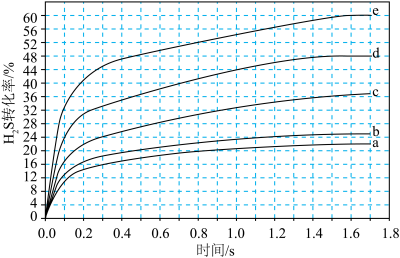
| A.H2S热分解反应的正反应活化能大于逆反应活化能 |
B.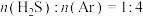 时,在0~0.9s之间,H2S分压的平均变化率为35.6 时,在0~0.9s之间,H2S分压的平均变化率为35.6 |
| C.生成a mol S2,同时形成4a mol H-S键,说明反应已达平衡 |
| D.等温等压下加入惰性气体越多,H2S平衡转化率会提高 |
您最近一年使用:0次
名校
解题方法
2 . 科学家设计了一种新型 金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。
金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。 和另一种材料
和另一种材料 均可用于除去有害气体
均可用于除去有害气体 ,
, 的孔径大小和形状恰能选择性固定
的孔径大小和形状恰能选择性固定 (如图所示)。
(如图所示)。 分子构型与乙烯类似。
分子构型与乙烯类似。
① ;
;
② 。
。
下列关于二者净化气体的说法中,正确的一项是
 金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。
金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。 和另一种材料
和另一种材料 均可用于除去有害气体
均可用于除去有害气体 ,
, 的孔径大小和形状恰能选择性固定
的孔径大小和形状恰能选择性固定 (如图所示)。
(如图所示)。
 分子构型与乙烯类似。
分子构型与乙烯类似。①
 ;
;②
 。
。下列关于二者净化气体的说法中,正确的一项是
A. 捕获的气体所有原子共平面, 捕获的气体所有原子共平面, 捕获的气体空间构型为正四面体 捕获的气体空间构型为正四面体 |
B. 置入废气后,废气颜色变深, 置入废气后,废气颜色变深, 置入废气后,废气颜色变浅 置入废气后,废气颜色变浅 |
C. 适宜在较低温度下净化气体, 适宜在较低温度下净化气体, 适宜在较高温度下净化气体 适宜在较高温度下净化气体 |
D. 适宜在较高压强下净化气体, 适宜在较高压强下净化气体, 适宜在较低压强下净化气体 适宜在较低压强下净化气体 |
您最近一年使用:0次
2024-05-12更新
|
108次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
3 . 钼酸铵是豆科植物的生命素。工业上欲利用废钼催化剂(主要成分为 ,还含少量的
,还含少量的 、CoS、NiO)制备钼酸铵,其具体流程为下:
、CoS、NiO)制备钼酸铵,其具体流程为下:
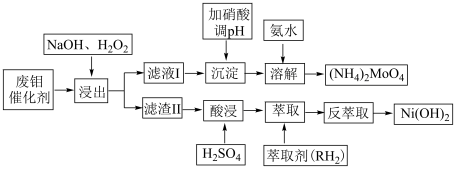
回答下列问题:
(1)为了提高浸出效率,可采取的措施为粉碎、___________ (写出2条)。
(2)写出浸出过程中主要反应的离子方程式___________ 。
(3)钼酸铵溶液经___________ 、过滤、洗涤、干燥可得到钼酸铵晶体,为减小产品损失,应选择下列___________ 试剂洗涤晶体。
A.蒸馏水 B.钼酸铵饱和溶液 C.乙醇水溶液
(4)由萃取过程的方程式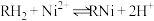 可知反萃取时应向体系中加入
可知反萃取时应向体系中加入___________ (酸性、碱性、中性)溶液。
(5)室温下,为保证反萃取后的溶液中 沉淀完全,应控制
沉淀完全,应控制 在什么范围
在什么范围___________ (已知:离子浓度小于 时可认为完全沉淀;
时可认为完全沉淀; )。
)。
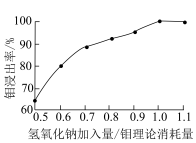
(6) 用量对钼的浸出率的影响如图所示,则浸出时最佳的
用量对钼的浸出率的影响如图所示,则浸出时最佳的 加入量与钼理论消耗量之比为
加入量与钼理论消耗量之比为___________ 。
 ,还含少量的
,还含少量的 、CoS、NiO)制备钼酸铵,其具体流程为下:
、CoS、NiO)制备钼酸铵,其具体流程为下:
回答下列问题:
(1)为了提高浸出效率,可采取的措施为粉碎、
(2)写出浸出过程中主要反应的离子方程式
(3)钼酸铵溶液经
A.蒸馏水 B.钼酸铵饱和溶液 C.乙醇水溶液
(4)由萃取过程的方程式
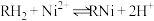 可知反萃取时应向体系中加入
可知反萃取时应向体系中加入(5)室温下,为保证反萃取后的溶液中
 沉淀完全,应控制
沉淀完全,应控制 在什么范围
在什么范围 时可认为完全沉淀;
时可认为完全沉淀; )。
)。(6)
 用量对钼的浸出率的影响如图所示,则浸出时最佳的
用量对钼的浸出率的影响如图所示,则浸出时最佳的 加入量与钼理论消耗量之比为
加入量与钼理论消耗量之比为
您最近一年使用:0次
4 . 通过向烟道内喷入还原剂NH3,然后在催化剂的作用下将烟气中的NOx还原成清洁的N2和H2O。回答下列问题:
(1)已知下列反应的热化学方程式
①2NH3(g)+2NO(g)+ O2(g)⇌2N2(g)+3H2O(g) ΔH1=-813kJ·mol-1
O2(g)⇌2N2(g)+3H2O(g) ΔH1=-813kJ·mol-1
②2NO2(g)+ NH3(g)⇌
NH3(g)⇌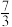 N2(g)+4H2O(g) ΔH2=-912kJ·mol-1
N2(g)+4H2O(g) ΔH2=-912kJ·mol-1
③NO(g)+NO2(g)+2NH3(g)⇌2N2(g)+3H2O(g) ΔH3
④2NH3(g)+ O2(g)⇌N2(g)+3H2O(g) ΔH4=-633kJ·mol-1
O2(g)⇌N2(g)+3H2O(g) ΔH4=-633kJ·mol-1
计算反应③的ΔH3=___________ kJ·mol-1
(2)关于合成氨工艺的下列理解,不正确的是___________(填字母)。
(3)工业上生产NH3过程中,常用Fe作催化剂,控制温度773K,压强3.0×107Pa,原料中N2和H2物质的量之比为1:2.8.分析说明原料气中N2过量的理由:___________ 。
(4)若向容积为1.0L的反应容器中通入5molN2、15molH2,在不同温度下分别达到平衡时,混合气体中NH3的质量分数随压强变化的曲线如图所示。

①温度T1、T2、T3大小关系是___________ 。
②M点的平衡常数K=___________ (可用计算式表示)。
(5)铁和氨气在一定条件下发生置换反应生成氢气和另外一种化合物,该化合物的晶胞结构如图所示,该化合物的化学式为___________ ,若两个最近的Fe原子间的距离为acm,设NA为阿伏加德罗常数的数值,则该晶体的密度是___________ gcm-3(列出表达式即可)

(1)已知下列反应的热化学方程式
①2NH3(g)+2NO(g)+
 O2(g)⇌2N2(g)+3H2O(g) ΔH1=-813kJ·mol-1
O2(g)⇌2N2(g)+3H2O(g) ΔH1=-813kJ·mol-1②2NO2(g)+
 NH3(g)⇌
NH3(g)⇌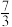 N2(g)+4H2O(g) ΔH2=-912kJ·mol-1
N2(g)+4H2O(g) ΔH2=-912kJ·mol-1③NO(g)+NO2(g)+2NH3(g)⇌2N2(g)+3H2O(g) ΔH3
④2NH3(g)+
 O2(g)⇌N2(g)+3H2O(g) ΔH4=-633kJ·mol-1
O2(g)⇌N2(g)+3H2O(g) ΔH4=-633kJ·mol-1计算反应③的ΔH3=
(2)关于合成氨工艺的下列理解,不正确的是___________(填字母)。
| A.工业实际生产中合成氨反应的ΔH和ΔS都小于零 |
| B.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率 |
| C.基于NH3有较强的分子间作用力可将其液化,不断将液氨移去,利于反应正向进行 |
| D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂“中毒” |
(4)若向容积为1.0L的反应容器中通入5molN2、15molH2,在不同温度下分别达到平衡时,混合气体中NH3的质量分数随压强变化的曲线如图所示。

①温度T1、T2、T3大小关系是
②M点的平衡常数K=
(5)铁和氨气在一定条件下发生置换反应生成氢气和另外一种化合物,该化合物的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次



