1 . 盐酸羟胺(化学式为 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
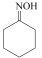 (环己酮肟)
(环己酮肟)
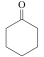 (环己酮)
(环己酮)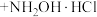
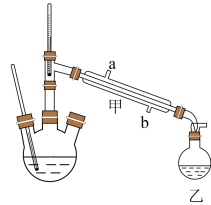
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。
盐酸羟胺在不同温度下的溶解度如下表:
(1)仪器甲中进水口应为___________ 。
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是___________ 。
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
(4)反应后,从三口烧瓶的溶液中获取盐酸羟胺的实验方法为___________。
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵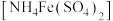 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。
反应原理为:①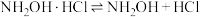
②
③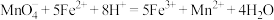
(5)将反应②补充完整,并标出电子转移的方向和数目___________ 。
(6)配制上述盐酸羟胺溶液所需要的定量仪器有___________ 。
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为___________ 。
(7)通过计算判断该产品的纯度级别___________ 。(写出计算过程)
已知:
 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
 (环己酮肟)
(环己酮肟)
 (环己酮)
(环己酮)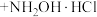
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。

盐酸羟胺在不同温度下的溶解度如下表:
| 温度(℃) | 溶解度(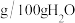 ) ) |
| 20 | 46.7 |
| 40 | 54.9 |
| 60 | 63.2 |
| 80 | 71.1 |
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
| A.共价键 | B.离子键 | C.氢键 | D.范德华力 |
| A.冷却结晶 | B.渗析 | C.蒸馏 | D.萃取、分液 |
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵
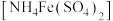 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。反应原理为:①
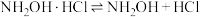
②

③
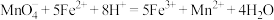
(5)将反应②补充完整,并标出电子转移的方向和数目
(6)配制上述盐酸羟胺溶液所需要的定量仪器有
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为
(7)通过计算判断该产品的纯度级别
| 纯度级别 | 优级纯 | 分析纯 | 化学纯 |
质量分数 | 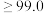 |  |  |

您最近一年使用:0次
2024-01-13更新
|
364次组卷
|
3卷引用:专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)上海市四区联考2023-2024学年高三上学期化学一模试卷上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
2 . 某校化学学习小组探究 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题:
(1)写出实验中制备 的化学方程式
的化学方程式________ 。
(2)配制100mL
 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和________ 。
【实验探究】
向3mL
 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
猜想1: 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;
猜想2: 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。
(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,________ ,证明猜想1不成立。
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。
已知:常温下,溶液中 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。________ (填写微粒符号),依据的实验证据是________ 。
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度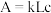 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验结果讨论:若 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若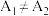 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。
(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如: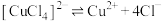 。
。
丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为: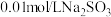 溶液,
溶液,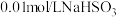 溶液,
溶液, 固体,
固体,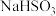 固体
固体
 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题: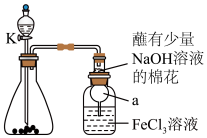
(1)写出实验中制备
 的化学方程式
的化学方程式(2)配制100mL

 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和【实验探究】
向3mL

 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:猜想1:
 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;猜想2:
 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是
 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。组别 | 溶液1(1mL) | 溶液2(2mL) | 现象 |
a |
|
| 溶液1和溶液2混合后,组别a、b、c所得溶液红棕色依次加深。 |
b |  的饱和溶液,用 的饱和溶液,用 固体调节. 固体调节. | ||
c |  的饱和溶液,用 的饱和溶液,用 固体调节 固体调节 |
 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。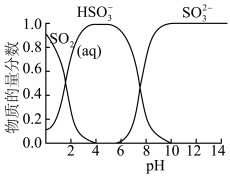
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度
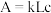 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验序号 | 操作 | 吸光度 |
1 | 把1mL 0.1mol/L 溶液与2mL 溶液与2mL 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 |
|
2 |
|
 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若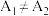 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如:
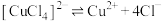 。
。丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为:
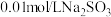 溶液,
溶液,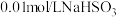 溶液,
溶液, 固体,
固体,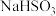 固体
固体实验序号 | 操作 | 吸光度 | 结论 |
3 | 向3mL 0.1mol/L 溶液中通入 溶液中通入 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 |
| |
4 |
  (填“大于”、“小于”或“等于”) (填“大于”、“小于”或“等于”) | 平衡向 |
您最近一年使用:0次
3 . 下列实验方案不能达到相应实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 向盛有 溶液的试管中滴加2滴 溶液的试管中滴加2滴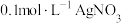 溶液,振荡试管,再向其中滴加4滴 溶液,振荡试管,再向其中滴加4滴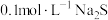 溶液,观察现象 溶液,观察现象 | 证明溶解度  |
| B | 向盛有 溶液的试管中滴加 溶液的试管中滴加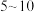 滴 滴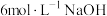 溶液,再继续滴加 溶液,再继续滴加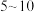 滴 滴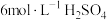 溶液,观察现象 溶液,观察现象 | 证明浓度对化学平衡的影响 |
| C | 向盛有少量蒸馏水的试管中滴加2滴 溶液,再滴加2滴硫氰化钾溶液,观察现象 溶液,再滴加2滴硫氰化钾溶液,观察现象 | 证明 的存在 的存在 |
| D | 室温下,向一定量饱和 溶液中通入足量 溶液中通入足量 气体,观察是否有晶体析出 气体,观察是否有晶体析出 | 证明室温下固体在水中的溶解度: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列实验方案设计、现象和结论正确的是
| 选项 | 实验目的 | 方案与现象 | 结论 |
| A | 探究反应物浓度对化学平衡的影响 | 向 的 的 溶液,再滴加10滴 溶液,再滴加10滴 的 的 溶液,溶液由黄色变为橙色 溶液,溶液由黄色变为橙色 | 说明增大氢离子浓度,平衡向生成 的方向移动 的方向移动 |
| B | 探究其他离子对化学平衡的影响 | 向 溶液中加入2滴 溶液中加入2滴 溶液,产生血红色,再加入少量 溶液,产生血红色,再加入少量 溶液后血红色变浅 溶液后血红色变浅 | 说明钾离子对该平衡有一定的抑制作用 |
| C | 判断水解常数大小: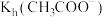 与 与 | 室温下,用 计分别测量等浓度的 计分别测量等浓度的 和 和 溶液的 溶液的 ,前者大于后者 ,前者大于后者 | 水解常数大小: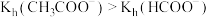 |
| D | 探究 和 和 在水溶液中的反应 在水溶液中的反应 | 向 溶液中滴加 溶液中滴加 溶液,有白色浑浊出现,并产生气体 溶液,有白色浑浊出现,并产生气体 | 说明 和 和 在相互促进水解 在相互促进水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 下列实验设计能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 探究反应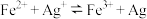 存在限度 存在限度 | 将 AgNO3溶液与 AgNO3溶液与 Fe(NO3)2溶液等体积混合后,取出两份混合液分别滴加KSCN溶液和K3[Fe(CN)6]溶液 Fe(NO3)2溶液等体积混合后,取出两份混合液分别滴加KSCN溶液和K3[Fe(CN)6]溶液 |
| B | 探究浓度对反应速率的影响 | 向两支盛有5mL不同浓度KMnO4溶液的试管中分别加入同浓度同体积的足量草酸溶液,观察实验现象 |
| C | 证明在相同条件下,溶解度Mg(OH)2>Fe(OH)3 | 向1mL NaOH溶液中滴入2滴 NaOH溶液中滴入2滴 MgCl2溶液,产生白色沉淀后,再滴加2滴 MgCl2溶液,产生白色沉淀后,再滴加2滴 FeCl3溶液,又生成红褐色沉淀 FeCl3溶液,又生成红褐色沉淀 |
| D | 测定反应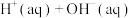 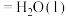 的 的 |  NaHSO4溶液和 NaHSO4溶液和 NaOH溶液进行中和热实验 NaOH溶液进行中和热实验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列实验目的、实验操作及现象与对应结论都正确的是
选项 | 实验目的 | 实验操作及现象 | 结论 |
A | 检验蔗糖是否水解 | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 ,无砖红色沉淀 ,无砖红色沉淀 | 蔗糖未发生水解 |
B | 探究镁和铝的金属活泼性 | 向盛有浓 溶液的两支试管中分别加入除去氧化膜的镁带和铝片,加入镁带的试管中迅速产生红棕色气体,加入铝片试管中无明显现象 溶液的两支试管中分别加入除去氧化膜的镁带和铝片,加入镁带的试管中迅速产生红棕色气体,加入铝片试管中无明显现象 | 金属活泼性: 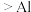 |
C | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向 溶液中缓慢滴加浓硫酸,溶液黄色变为橙红色 溶液中缓慢滴加浓硫酸,溶液黄色变为橙红色 | 增大氢离子浓度,平衡向生成 的方向移动 的方向移动 |
D | 探究在相同条件下 和 和 的溶解度大小 的溶解度大小 | 向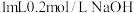 溶液中滴入2滴 溶液中滴入2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同条件下,溶解度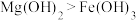 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 下列实验目的对应的实验方案设计、现象和结论都正确的是
| 选项 | 实验方案设计 | 现象和结论 |
| A | 用pH计测量 、 、 的pH,比较溶液pH大小 的pH,比较溶液pH大小 |  的pH比 的pH比 大,说明 大,说明 酸性比 酸性比 强 强 |
| B | 将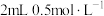 的 的 溶液加热后置于冷水中 溶液加热后置于冷水中 | 溶液由黄绿色变为蓝绿色,说明降低温度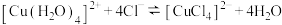 向逆方向移动 向逆方向移动 |
| C | 向平衡体系 中加入适量 中加入适量 固体 固体 | 溶液颜色变浅,说明生成物浓度增大,平衡逆向移动 |
| D | 向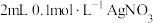 溶液中先滴加4滴 溶液中先滴加4滴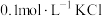 溶液,再滴加4滴 溶液,再滴加4滴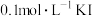 溶液 溶液 | 先产生白色沉淀,再产生黄色沉淀,说明 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-13更新
|
192次组卷
|
2卷引用:06-2023新东方高二上期中考化学
名校
解题方法
8 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确 的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究Fe和S反应特点 | 将适量硫粉和铁粉混合堆成条状。用灼热的玻璃棒触及一端,当混合物呈红热状态时,移开玻璃棒。 | 混合物继续保持红热并持续扩散,粉末呈黑色 | 该反应为放热反应 |
| B | 比较沉淀的Ksp大小 | 向相同浓度和体积的浓氨水中,分别加入等量AgCl和AgI固体,充分搅拌 | 氯化银溶解,碘化银无变化 | Ksp:AgCl>AgI |
| C | 判断平衡移动的方向 | 将装有NO2气体的注射器的活塞缓慢向外拉 | 红棕色逐渐变浅 | 可逆反应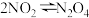 平衡正向移动 平衡正向移动 |
| D | 检验Na2S2O3样品是否含有Na2SO4杂质 | 取少量样品溶于水,先加入过量稀盐酸,过滤,向滤液中滴加少量BaCl2溶液 | 滤液中出现浑浊 | 该样品中含有Na2SO4杂质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 利用下列实验装置不能达到实验目的的是
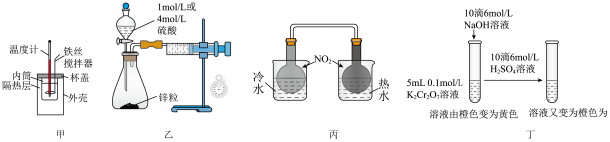

| A.用甲装置准确测定中和热 |
| B.用乙装置测定不同浓度硫酸与锌粒反应速率 |
| C.用丙装置证明温度对平衡移动的影响 |
| D.用丁装置研究溶液的酸碱性对平衡移动的影响 |
您最近一年使用:0次
名校
解题方法
10 . 用下列仪器或装置(部分夹持装置略)进行相应实验,能够达到实验目的的是
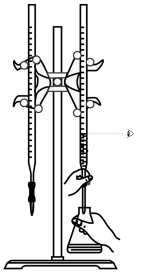 | 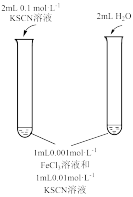 | 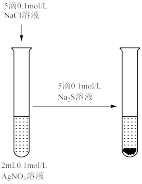 |  |
| A.用标准NaOH溶液滴定锥形瓶中的盐酸 | B.研究浓度对化学平衡的影响 | C.验证沉淀转化:AgCl转化为 | D.检验 溶液是否变质 溶液是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-04更新
|
204次组卷
|
2卷引用:北京市第九中学2023-2024学年高二下学期2月开学考化学试题

 溶液
溶液



