解题方法
1 . 环氧乙烷(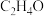 )被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯(
)被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯( )直接氧化法制取环氧乙烷,体系中发生的反应如下:
)直接氧化法制取环氧乙烷,体系中发生的反应如下:
主反应:


副反应: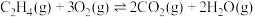

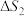
回答下列问题:
(1)已知几种化学键的键能如表所示:
试计算
___________ 。
(2)主反应与副反应的吉布斯自由能变( )与温度T的关系如图所示,则副反应的
)与温度T的关系如图所示,则副反应的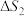
___________ (填“>”“<”或“=”)0,
___________ (填“>”“<”或“=”)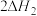 。
。

(3)在250℃、101kPa下,向某密闭容器中充入一定量的 和
和 ,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是
,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是 ,增大压强,
,增大压强, 的含量将
的含量将___________ (填“增大”“减小”或“不变”)。工业生产中常采用的反应条件为250℃、2.0MPa,并选择Ag作催化剂,充分反应后体系中含碳组分含量最高的是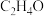 ,则Ag所起的作用可能为
,则Ag所起的作用可能为___________ 。
(4)一定条件下,用富氧空气(只含 和
和 ,且
,且 的体积分数为55%)代替
的体积分数为55%)代替 ,将
,将 、
、 、
、 按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa,
按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa, 的体积分数为31.25%,
的体积分数为31.25%,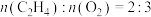 ,则
,则 和
和 的平衡转化率之比为
的平衡转化率之比为___________ ,该条件下主反应的压强平衡常数
___________  (
( 为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
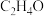 )被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯(
)被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯( )直接氧化法制取环氧乙烷,体系中发生的反应如下:
)直接氧化法制取环氧乙烷,体系中发生的反应如下:主反应:



副反应:
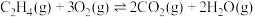

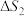
回答下列问题:
(1)已知几种化学键的键能如表所示:
| 化学键 | C-H | C=C | C-C | C-O | O=O |
键能 | 423 | 682 | 368 | 335 | 498 |

(2)主反应与副反应的吉布斯自由能变(
 )与温度T的关系如图所示,则副反应的
)与温度T的关系如图所示,则副反应的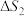

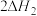 。
。
(3)在250℃、101kPa下,向某密闭容器中充入一定量的
 和
和 ,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是
,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是 ,增大压强,
,增大压强, 的含量将
的含量将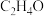 ,则Ag所起的作用可能为
,则Ag所起的作用可能为(4)一定条件下,用富氧空气(只含
 和
和 ,且
,且 的体积分数为55%)代替
的体积分数为55%)代替 ,将
,将 、
、 、
、 按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa,
按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa, 的体积分数为31.25%,
的体积分数为31.25%,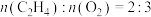 ,则
,则 和
和 的平衡转化率之比为
的平衡转化率之比为
 (
( 为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
您最近一年使用:0次
名校
解题方法
2 . 我国已探明或开发的天然气中含有一定含量的 ,而且随着原油中硫含量的上升,炼油厂中干气及液化气等含硫气体的排放量逐年增加。与此同时,我国汽油、柴油标准不断升级、环保排放要求不断升高,新增的加氢装置也越来越多,气体中
,而且随着原油中硫含量的上升,炼油厂中干气及液化气等含硫气体的排放量逐年增加。与此同时,我国汽油、柴油标准不断升级、环保排放要求不断升高,新增的加氢装置也越来越多,气体中 含量也不断增加。
含量也不断增加。 会引起设备腐蚀,还会威胁生命安全。因此,炼油厂中的干气、液化气、加氨后气体以及气田中的天然气都必须首先进行脱硫净化处理。
会引起设备腐蚀,还会威胁生命安全。因此,炼油厂中的干气、液化气、加氨后气体以及气田中的天然气都必须首先进行脱硫净化处理。
I.胺液脱硫
胺液脱硫系统已成为石油、天然气加工的重要组成部分。含氨基的有机化合物称为胺,现用 表示(R代烃基)。
表示(R代烃基)。
(1)用化学方程式解释胺的水溶液呈碱性原因:_____ 。
(2)用胺液吸收足量 的离子方程式是
的离子方程式是_____ 。
(3)某胺(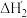 )的
)的 ,
, 的两级电离平衡常数分别为
的两级电离平衡常数分别为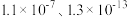 ,则(
,则(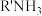 )HS的水溶液呈
)HS的水溶液呈_____ (填标号)。
A.碱性 B.中性 C.酸性
Ⅱ.热分解法脱硫
在密闭容器中模拟工业热分解法脱硫,发生反应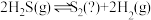 。其他条件不变时,
。其他条件不变时, 的平衡转化率随温度和压强的变化如图。
的平衡转化率随温度和压强的变化如图。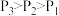 ,反应中
,反应中
_____ (填“是”或“不是")气态,理由是_____ 。
(5)实际反应在高温下进行的原因可能是_____ (答出2条即可)。
 ,而且随着原油中硫含量的上升,炼油厂中干气及液化气等含硫气体的排放量逐年增加。与此同时,我国汽油、柴油标准不断升级、环保排放要求不断升高,新增的加氢装置也越来越多,气体中
,而且随着原油中硫含量的上升,炼油厂中干气及液化气等含硫气体的排放量逐年增加。与此同时,我国汽油、柴油标准不断升级、环保排放要求不断升高,新增的加氢装置也越来越多,气体中 含量也不断增加。
含量也不断增加。 会引起设备腐蚀,还会威胁生命安全。因此,炼油厂中的干气、液化气、加氨后气体以及气田中的天然气都必须首先进行脱硫净化处理。
会引起设备腐蚀,还会威胁生命安全。因此,炼油厂中的干气、液化气、加氨后气体以及气田中的天然气都必须首先进行脱硫净化处理。I.胺液脱硫
胺液脱硫系统已成为石油、天然气加工的重要组成部分。含氨基的有机化合物称为胺,现用
 表示(R代烃基)。
表示(R代烃基)。(1)用化学方程式解释胺的水溶液呈碱性原因:
(2)用胺液吸收足量
 的离子方程式是
的离子方程式是(3)某胺(
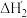 )的
)的 ,
, 的两级电离平衡常数分别为
的两级电离平衡常数分别为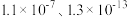 ,则(
,则(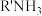 )HS的水溶液呈
)HS的水溶液呈A.碱性 B.中性 C.酸性
Ⅱ.热分解法脱硫
在密闭容器中模拟工业热分解法脱硫,发生反应
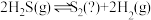 。其他条件不变时,
。其他条件不变时, 的平衡转化率随温度和压强的变化如图。
的平衡转化率随温度和压强的变化如图。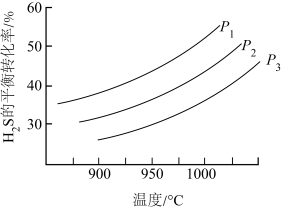
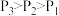 ,反应中
,反应中
(5)实际反应在高温下进行的原因可能是
您最近一年使用:0次
名校
3 . 在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
 2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是| A.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于QkJ |
| B.2min后,向容器中再通入一定量的SO3气体,重新达到平衡时,SO2的含量变小 |
| C.若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO3)大于1.4mol |
| D.若反应开始时容器体积为2L,则v(SO3)=0.7mol·L-1·min-1 |
您最近一年使用:0次
2022-08-24更新
|
1016次组卷
|
3卷引用:黑龙江省哈尔滨市第六中学2021-2022学年高二上学期期末考试化学试题
名校
4 . 气态含氮化合物及相关反应是新型科研热点。
I.工业上主要采用氨催化氧化法生产NO:
主反应: 4NH3(g)+5O2(g) 4NO(g)+6H2O(g ) △H1
4NO(g)+6H2O(g ) △H1
副反应: 4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H2=- 1265kJ·mol-1
2N2(g)+6H2O(g) △H2=- 1265kJ·mol-1
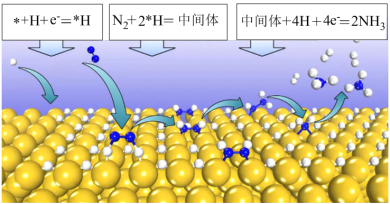
(1)王金兰课题组提出合成氨的“表面氢化机理”如图,在较低的电压下实现氮气还原合成氨。“N2+ 2*H=中间体”是氮气还原合成氨的决速步,“中间体”为___________ (写化学式)。
(2)已知N2(g)+O2(g)= 2NO(g) △H =+180kJ·mol-1,则△H1=___________ kJ·mol -1。
(3)制备NO时,在某种氨的初始含量下,温度升高一段时间后,体系中 减小,可能的原因是
减小,可能的原因是___________ 。
II.已知工业上常利用NO和Cl2反应来制备有机合成中的重要试剂亚硝酰氯(NOC1),化学方程式为2NO(g)+Cl2(g) 2NOCl(g) △H <0。
2NOCl(g) △H <0。
(4)保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比 进行反应,平衡时某反应物的转化率和氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率和氮氯比及不同温度的关系如图所示:
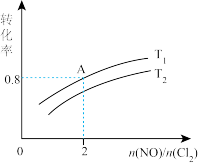
①图中T1、T2的关系为T1___________ T2(填“<”或“=”)
②体系的初始压强为P0,则A点的平衡常数Kp=___________ ; (以分压表示,分压=总压×物质的量分数)
III. NOx是空气污染物之一,用焦炭还原NO2的反应为: 2NO2(g)+2C(s) N2(g)+2CO2(g) △H >0. T°C时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,经t min,测得各容器中NO2的转化率与容器容积的关系如图所示。
N2(g)+2CO2(g) △H >0. T°C时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,经t min,测得各容器中NO2的转化率与容器容积的关系如图所示。
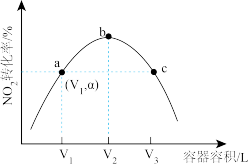
(5)①提高NO2平衡转化率可采取的措施是_____ (答出两种即可)。
②a点对应的容器,t min内v(NO2)=___________ (用含字母的代数式表示)。
③a、b、c三点中,已达平衡状态的有___________ 。
I.工业上主要采用氨催化氧化法生产NO:
主反应: 4NH3(g)+5O2(g)
 4NO(g)+6H2O(g ) △H1
4NO(g)+6H2O(g ) △H1副反应: 4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H2=- 1265kJ·mol-1
2N2(g)+6H2O(g) △H2=- 1265kJ·mol-1(1)王金兰课题组提出合成氨的“表面氢化机理”如图,在较低的电压下实现氮气还原合成氨。“N2+ 2*H=中间体”是氮气还原合成氨的决速步,“中间体”为

(2)已知N2(g)+O2(g)= 2NO(g) △H =+180kJ·mol-1,则△H1=
(3)制备NO时,在某种氨的初始含量下,温度升高一段时间后,体系中
 减小,可能的原因是
减小,可能的原因是II.已知工业上常利用NO和Cl2反应来制备有机合成中的重要试剂亚硝酰氯(NOC1),化学方程式为2NO(g)+Cl2(g)
 2NOCl(g) △H <0。
2NOCl(g) △H <0。(4)保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比
 进行反应,平衡时某反应物的转化率和氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率和氮氯比及不同温度的关系如图所示:
①图中T1、T2的关系为T1
②体系的初始压强为P0,则A点的平衡常数Kp=
III. NOx是空气污染物之一,用焦炭还原NO2的反应为: 2NO2(g)+2C(s)
 N2(g)+2CO2(g) △H >0. T°C时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,经t min,测得各容器中NO2的转化率与容器容积的关系如图所示。
N2(g)+2CO2(g) △H >0. T°C时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2,经t min,测得各容器中NO2的转化率与容器容积的关系如图所示。
(5)①提高NO2平衡转化率可采取的措施是
②a点对应的容器,t min内v(NO2)=
③a、b、c三点中,已达平衡状态的有
您最近一年使用:0次
2022-06-27更新
|
617次组卷
|
3卷引用:四川省雅安市2022届高三下学期第三次诊断性考试理综化学试题
名校
5 . 对于可逆反应mA(s)+nB(g) eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
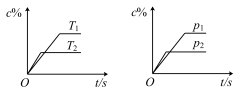
 eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
| A.达到平衡后,若使用催化剂,C的质量分数将增大 |
| B.达到平衡后,增加A的量有利于化学平衡向正方向移动 |
| C.化学方程式中n>e+f |
| D.达到平衡后,若升高温度,化学平衡向逆方向移动 |
您最近一年使用:0次
2019-06-17更新
|
1222次组卷
|
4卷引用:陕西省吴起高级中学2018-2019学年高一下学期第二次月考能力卷化学试题
名校
6 . 在一定温度下,向容积固定不变的密闭容器中充入a mol A,发生反应:2A(g)  B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
 B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )| A.平均相对分子质量增大 |
| B.A的转化率提高 |
| C.A的质量分数增大 |
| D.反应放出的总热量大于原来的2倍 |
您最近一年使用:0次
2019-04-04更新
|
279次组卷
|
2卷引用:【全国百强校】福建省厦门外国语学校2018-2019学年高二下学期第一次月考化学试题
7 . 为了减轻大气污染,可在汽车尾气排放处加装“催化净化器”装置。
(1)通过“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的化学方程式:__ 。
(2)在一定温度下,向1L密闭恒容容器中充入1molNO、2molCO,发生上述反应,10s时反应达到平衡,此时CO的物质的量为1.2mol。请回答下列问题:
①前10s内平均反应速率v(CO)=___ 。
②在该温度下反应的平衡常数K=___ 。
③关于上述反应,下列叙述正确的是___ (填字母)。
A.达到平衡时,移走部分CO2,平衡将向右移动,正反应速率加快
B.扩大容器的体积,平衡将向右移动
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度不变,再向容器中充入0.8molCO和0.4molN2,则此时v正>v逆
④已知上述实验中,c(CO)与反应时间t变化曲线Ⅰ如图:
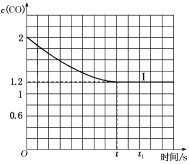
若其他条件不变,将1molNO、2molCO投入2L容器进行反应,请在图中绘出c(CO)与反应时间t1变化曲线Ⅱ___ (不要求标出CO的终点坐标)。
(3)测试某汽车冷启动时的尾气催化处理,CO、NO百分含量随时间变化曲线如图:
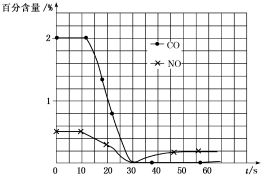
请回答:
前0~10s阶段,CO、NO百分含量没明显变化的原因是___ 。
(1)通过“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的化学方程式:
(2)在一定温度下,向1L密闭恒容容器中充入1molNO、2molCO,发生上述反应,10s时反应达到平衡,此时CO的物质的量为1.2mol。请回答下列问题:
①前10s内平均反应速率v(CO)=
②在该温度下反应的平衡常数K=
③关于上述反应,下列叙述正确的是
A.达到平衡时,移走部分CO2,平衡将向右移动,正反应速率加快
B.扩大容器的体积,平衡将向右移动
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度不变,再向容器中充入0.8molCO和0.4molN2,则此时v正>v逆
④已知上述实验中,c(CO)与反应时间t变化曲线Ⅰ如图:

若其他条件不变,将1molNO、2molCO投入2L容器进行反应,请在图中绘出c(CO)与反应时间t1变化曲线Ⅱ
(3)测试某汽车冷启动时的尾气催化处理,CO、NO百分含量随时间变化曲线如图:

请回答:
前0~10s阶段,CO、NO百分含量没明显变化的原因是
您最近一年使用:0次
名校
8 . 甲、乙、丙三个容器中最初存在的物质及其数量如图所示,三个容器最初的容积相等、温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是
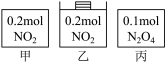
| A.平衡时各容器内c(NO2)的大小顺序为乙>甲>丙 |
| B.平衡时N2O4的百分含量:乙>甲=丙 |
| C.平衡时甲中NO2与丙中N2O4的转化率不可能相同 |
| D.平衡时混合物的平均相对分子质量:甲>乙>丙 |
您最近一年使用:0次
2019-11-06更新
|
2233次组卷
|
28卷引用:山西省朔州市怀仁一中2019-2020学年高二上学期期中考试化学试题
山西省朔州市怀仁一中2019-2020学年高二上学期期中考试化学试题山东省新泰市第二中学2019-2020学年高二上学期期中考试化学试题步步为赢 高二化学寒假作业:作业六 化学平衡中的模型构建与等效平衡辽宁省辽阳市集美中学2020届高二12月月考化学试题江西省万载中学2019-2020学年高二12月月考(创新班)化学试题鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第2节综合训练高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 第二节综合训练黑龙江省哈尔滨三中2021届高三上学期期中考试化学试题天津市第一中学2021届高三上学期第二次月考化学试题(已下线)练习4 化学平衡-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)山西省寿阳县第一中学2020—2021学年高二上学期第二次月考化学试题黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题河南省林州市第一中学2020-2021学年高二下学期第二次月考化学试题选择性必修1 专题2 第三单元综合训练黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期开学考试化学试题(已下线)选择性必修1 期中检测(能力提升卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)山东省临沂市平邑县第一中学实验部2021-2022学年高二上学期第二次月考化学试题湖北省武汉市长虹中学2021-2022学年高二上学期10月月考化学试卷河南省洛阳市2021-2022学年高二上期期中考试化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题江西省新余市2021-2022学年高二上学期期末检测化学试题云南省凤庆县第一中学2021-2022学年高二下学期3月份考试化学试题四川省广安市华蓥中学校2021-2022学年高二上学期11月月考化学试题山西省山西大学附属中学2022-2023学年高二上学期10月考化学试题2.3.1浓度 压强变化对化学平衡的影响 课后安徽省安庆市第二中学2023-2024学年高二上学期期中考试化学试卷山东省青岛第十七中学2023-2024学年高二上学期12月月考化学试题福建师范大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
9 . 在一密闭容器中,可逆反应:aA(g) + bB(g)  cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
 cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是| A.a + b > c | B.平衡向正反应方向移动 |
| C.物质A的转化率降低 | D.物质C的质量分数增加 |
您最近一年使用:0次
2017-11-07更新
|
302次组卷
|
2卷引用:四川省成都市七中实验学校2018届高三上学期入学考试化学试题
10 . 在容积一定的密闭器中发生可逆反应:A(g)+2B(g)  2C(g)
2C(g)  H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是

 2C(g)
2C(g)  H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
A.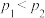 ,纵坐标指A的质量分数 ,纵坐标指A的质量分数 |
B. ,纵坐标指C的质量分数 ,纵坐标指C的质量分数 |
C. ,纵坐标指混合气体的平均摩尔质量 ,纵坐标指混合气体的平均摩尔质量 |
D. ,纵坐标指A的转化率 ,纵坐标指A的转化率 |
您最近一年使用:0次
2017-06-29更新
|
387次组卷
|
5卷引用:江西省玉山县第一中学2016-2017学年高一(19-31班)下学期期中考试化学试题
江西省玉山县第一中学2016-2017学年高一(19-31班)下学期期中考试化学试题北京市第161中学2017-2018学年高二上学期期中适应性训练化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时3 化学平衡图象新疆昌吉州教育共同体2020-2021学年高二上学期期中考试化学试题(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(精讲)-2022年一轮复习讲练测



